Исследование уровня молочной кислоты в крови, цены в Нижнем Новгороде
Лактат – это продукт клеточного метаболизма, производная молочной кислоты. Может находиться в клетках в виде самой молочной кислоты либо в виде ее солей. В норме концентрация лактатов в крови очень низкая. В мышцах, эритроцитах, клетках мозга и в других тканях она повышается при недостатке кислорода в клетке либо если первичный путь производства энергии в клетках нарушен. Основные запасы клеточной энергии производятся в митохондриях, крошечных «энергетических станциях» внутри клеток организма. Митохондрии используют глюкозу и кислород для производства АТФ (аденозинтрифосфата), главного энергетического источника в организме. Это называется аэробным образованием энергии. При падении уровня кислорода в клетке либо при нарушении нормального функционирования митохондрий организм переключается на менее эффективное производство энергии (анаэробное) путем расщепления глюкозы с образованием АТФ. Лактат является основным побочным продуктом этого анаэробного процесса.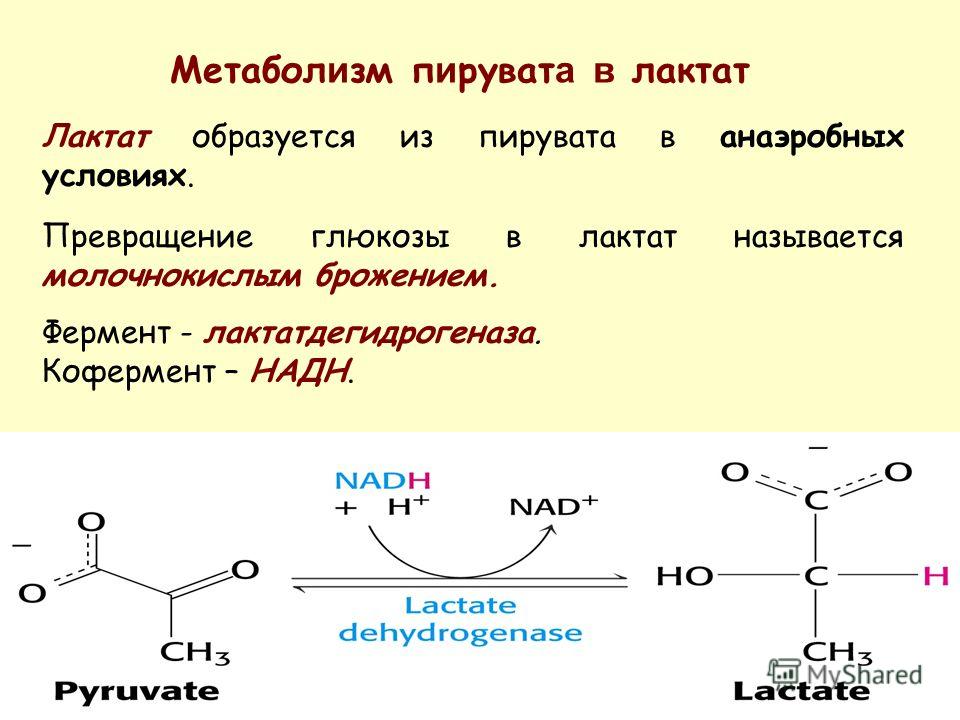
Лактацидоз А-типа наиболее распространен и ассоциирован с факторами, вызывающими недостаточный захват кислорода легкими либо замедленное кровообращение, что приводит к уменьшению снабжения тканей кислородом.
Примеры лактацидоза А-типа:
— шок в результате полученной травмы или сильной кровопотери,
— сепсис,
— инфаркт,
— застойная сердечная недостаточность,
— тяжелые легочные либо респираторные заболевания,
— отек легких,
— тяжелые формы анемии.
Лактацидоз Б-типа не связан с поступлением кислорода к тканям, он является причиной повышенной потребности в кислороде из-за проблем обмена веществ.
Примеры лактацидоза Б-типа:
— болезни печени,
— почечные заболевания,
— сахарный диабет,
— лейкоз,
— СПИД,
— болезни, связанные с сохранением гликогена (например, глюкозо-6-фосфатазная недостаточность),
— лекарства и токсины, такие как салицилаты, цианиды, метанол, метформин,
— различные наследственные митохондриальные и метаболические заболевания, являющиеся формами мышечной дистрофии и затрагивающие синтез АТФ,
— состояние при интенсивных физических нагрузках.
Лактат является метаболическим продуктом пропиленгликоля, входящего в состав растворителя для многих внутривенных препаратов. У пациентов со сниженной функцией почек при продолжительных инфузиях таких растворов может накапливаться повышенное количество лактата.
Для чего используется исследование?
— Для выявления лактацидоза, то есть высокого содержания лактатов.
— Чтобы определить гипоксию и лактацидоз и оценить их тяжесть, если есть факторы, понижающие снабжение кислородом клеток и тканей (лактацидоз чаще всего возникает именно из-за этого), например шок или застойная сердечная недостаточность.
— Для оценки кислотно-щелочного баланса и оксигенации (вместе с анализом на газы в крови).
— При диагностике болезней, которые способны привести к повышенному содержанию лактатов, а также при симптомах ацидоза, поскольку лактацидоз может вызываться факторами, не связанными с уровнем кислорода в тканях.
— Чтобы выяснить, не являются ли сопутствующие заболевания, например болезни печени или почек, причиной лактацидоза (вместе с другими исследованиями, такими как клинический анализ крови или мочи, некоторые биохимические тесты).
— Для обследования больных с подозрением на сепсис. Если уровень лактатов у них падает ниже нормы, лечение им назначается незамедлительно. При своевременной диагностике и безотлагательном лечении сепсиса шансы на успешное выздоровление увеличиваются во много раз.
— Для наблюдения за течением гипоксии и контроля за эффективностью ее лечения в случае обострения таких болезней, как сепсис, инфаркт и застойная сердечная недостаточность.
Когда назначается исследование?
— При симптомах недостатка кислорода (одышка, учащенное дыхание, бледность, потливость, тошнота, слабость в мышцах).
— При подозрении на сепсис, шок, инфаркт, сердечную недостаточность, почечную недостаточность или сахарный диабет.
— При острых головных болях, лихорадке, расстройстве и потере сознания, а также признаках менингита. Оценка кислородного снабжения тканей при шоке, нарушениях кровообращения.
— Оценка причины ацидоза.
— Диагностика причин метаболического ацидоза.
— Оценка уровня перфузии и адекватности доставки кислорода в ткани.
— Исследования в области спортивной физиологии и медицины.
— Дифференциальная диагностика миопатий.
— Дифференциальная диагностика энзимопатий новорожденных.
— Асфиксия новорожденных.
— Сахарный диабет II типа.
Лактат может быть ключом к пониманию механизма развития рака
Новые исследования, опубликованные в журнале Канцерогенез
, анализируют роль лактата в онкогенезе.Лактат является продуктом химического процесса, известного как гликолиз — расщепление сахара (глюкоза), на более мелкие молекулы с целью получения энергии в отсутствии кислорода. Во время интенсивной физической активности лактат накапливается в тканях (сопровождается болью в мышцах и снижением физической работоспособности) и выводится в кровь.
В начале 20 — го века, немецкий ученый Отто Варбург заметил, что раковые клетки потребляют гораздо больше глюкозы, чем нормальные клетки. Так называемый эффект Варбурга относится к тому, что в раковых клетках происходит более интенсивный гликолиз, а значит, образуется больше лактата (по сравнению с нормальными клетками).
Изучение роли лактата в онкогенезе
Сан — Миллан и его коллеги предполагают, что лактат является «единственным метаболическим соединением, которое обязательно участвует» во всех этапах канцерогенеза.
В исследовании рассматривается роль лактата в ангиогенезе (процесс образования кровеносных сосудов внутри опухоли). В этом исследовании описано, что лактат создает кислотную микросреду вне клетки рака, тем самым создает благоприятные условия для распространения раковых клеток (метастазирование).
«Для того, чтобы остановить рак вы должны остановить лактат»
Понимая роль лактата в метаболизме клеток рака можно объяснить, почему люди, регулярно занимающиеся физическими упражнениями, имеют гораздо низкий риск развития рака. У спортсменов и тренированных людей тело «привыкает» эффективно использовать лактат в качестве источника энергии для организма, тем самым предотвращая его накопление.
Основываясь на своих выводах, исследователи предполагают, что сидячий образ жизни в сочетании со слишком большим количеством сахара в пищевом рационе может привести к чрезмерному накоплению молочной кислоты, тем самым подготовив почву для рака.
«С помощью данного исследования мы открываем совершенно новую дверь для понимания рака, показывая впервые, что лактат не только присутствует, но является обязательным для каждого звена в развитии рака».
Иниго Сан-Миллан
В ближайшее время Сан — Миллан планирует сотрудничать с госпиталем Университета Колорадо, чтобы изучить влияние разработанных программ физических упражнений на больных раком. Уже приступили к изучению пациенток с раком молочной железы.
Сан — Миллан надеется, что, в конце концов, его исследование поможет разработать препараты, препятствующие накоплению лактата. «Мы сигнализируем научному сообществу — чтобы остановить рак, вы должны остановить лактат,» — говорит он. «Есть много способов сделать это — например, путем воздействия на транспортеры монокарбоксилата, на которых лактат переносится из клетки в клетку».
Мнение специалиста: Определение лактата, как неспецифического маркера ишемии, распространено в лабораторной диагностике при анализе КЩС. Теперь можно рассматривать и новое клиническое значение исследования лактата – контроль обширности развития опухолевого процесса? Интересный, новый, полезный подход И конечно – здоровый образ жизни, спорт и ни грамма свободного места для развития опухолевого процесса!
Влияние сахарозаменителей на биохимический состав ротовой жидкости
В последние годы значительно возросло число публикаций, посвященных биохимии ротовой жидкости (РЖ), что связано с разработкой инновационных микрометодов анализа и с открытием новых диагностических маркеров [2, 3, 10]. Известно, что ряд биохимических показателей слюны отражают состояние не только полости рта, но и всего организма, однако РЖ все еще является наименее изученной из всех биологических жидкостей организма [4, 11, 13]. Показано, что после аппликации на зубные ряды растворов кариесогенных углеводов (глюкозы и сахарозы) происходит быстрое снижение водородного показателя рН на зубном налете в результате микробного гликолиза с образованием лактата [11]. Это явление нашло применение в прогнозировании кариеса зубов по состоянию кислотно-основного равновесия смешанной слюны, так как при его нарушении изменяется баланс между процессами минерализации и деминерализации в пользу последней. Согласно решению Всемирной федерации стоматологов [7], молекулярные механизмы метаболических сдвигов при применении калорийных и некалорийных подсластителей и их роль в профилактике кариеса нуждаются в дальнейшем изучении.
Известно, что ряд биохимических показателей слюны отражают состояние не только полости рта, но и всего организма, однако РЖ все еще является наименее изученной из всех биологических жидкостей организма [4, 11, 13]. Показано, что после аппликации на зубные ряды растворов кариесогенных углеводов (глюкозы и сахарозы) происходит быстрое снижение водородного показателя рН на зубном налете в результате микробного гликолиза с образованием лактата [11]. Это явление нашло применение в прогнозировании кариеса зубов по состоянию кислотно-основного равновесия смешанной слюны, так как при его нарушении изменяется баланс между процессами минерализации и деминерализации в пользу последней. Согласно решению Всемирной федерации стоматологов [7], молекулярные механизмы метаболических сдвигов при применении калорийных и некалорийных подсластителей и их роль в профилактике кариеса нуждаются в дальнейшем изучении.
Цель работы — изучение активности ферментов, показателей метаболизма белков, углеводов, состояние процессов липопероксидации (ЛПО) в РЖ и ее антиоксидантной активности (АОА) при воздействии кариесогенных сахарсодержаших продуктов и сахарозаменителей.
Материал и методы
Нами проведено клиническое обследование 60 практически здоровых студентов-добровольцев медицинского вуза в возрасте от 18 до 23 лет, которые были распределены на 3 группы по 20 человек. Основные этапы исследования: снятие зубного налета со щечной поверхности моляров с помощью ватного тампона и растворение его в пробирке с дистиллированной водой; скрининговое определение содержания лактата в реакции Уфельмана (по интенсивности желтой окраски с реактивом фенолята железа) до и через 15—20 мин после употребления сахарсодержащих продуктов (карамель, рафинад) — 1-я группа, а также через 10—15 мин после использования жевательной резинки Орбит (2-я группа). Контрольная группа не получала сахарсодержащих продуктов и сахарозаменителей. После полоскания полости рта кипяченой водой комнатной температуры собирали РЖ. Использовали современные спектрофотометрические и фотоэлектроколориметрические методы изучения активности ферментов, метаболитов белкового и углеводного обмена [1, 5, 6, 8].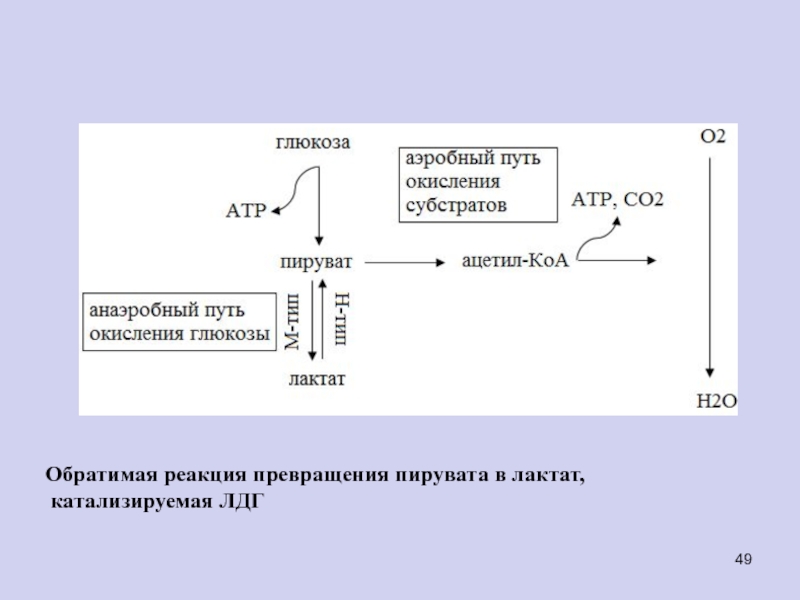 Содержание общего белка (ОБ) определяли методом Лоури, основанным на способности медных производных белка восстанавливать реактив Фолина с образованием окрашенных продуктов реакции, уровень глюкозы — глюкозооксидазным методом, содержание пирувата — динитрофенилгидразиновым методом [1], лактата — энзиматическим колориметрическим методом с помощью набора реактивов «Витал-лактат» (Россия). Активность ферментов трансаминирования — аспартатаминотрансферазы (АСТ) (К.Ф. 2.6.1.1) и аланинаминотрансферазы (АЛТ) (К.Ф. 2.6.1.2) — оценивали с помощью стандартного набора реактивов «Лахема» (Чехия). Активность лактатдегидрогеназы (ЛДГ) (К.Ф. 1.1.1.27) изучали колориметрическим методом с использованием редоксиндикаторов [9]. ЛПО и АОА устанавливали с помощью индуцированной пероксидом водорода и ионами железа хемилюминесценции (ХЛ) [12]. Светосумму ХЛ определяли за 30 с (S30) и 60 с (S60), максимальную вспышку ХЛ (Imax) за исследуемое время — на хемилюминометре «Emilite 1105» (Россия).
Содержание общего белка (ОБ) определяли методом Лоури, основанным на способности медных производных белка восстанавливать реактив Фолина с образованием окрашенных продуктов реакции, уровень глюкозы — глюкозооксидазным методом, содержание пирувата — динитрофенилгидразиновым методом [1], лактата — энзиматическим колориметрическим методом с помощью набора реактивов «Витал-лактат» (Россия). Активность ферментов трансаминирования — аспартатаминотрансферазы (АСТ) (К.Ф. 2.6.1.1) и аланинаминотрансферазы (АЛТ) (К.Ф. 2.6.1.2) — оценивали с помощью стандартного набора реактивов «Лахема» (Чехия). Активность лактатдегидрогеназы (ЛДГ) (К.Ф. 1.1.1.27) изучали колориметрическим методом с использованием редоксиндикаторов [9]. ЛПО и АОА устанавливали с помощью индуцированной пероксидом водорода и ионами железа хемилюминесценции (ХЛ) [12]. Светосумму ХЛ определяли за 30 с (S30) и 60 с (S60), максимальную вспышку ХЛ (Imax) за исследуемое время — на хемилюминометре «Emilite 1105» (Россия).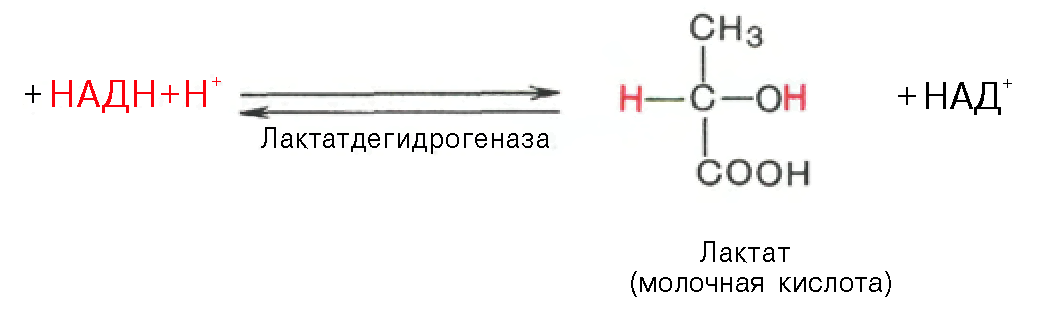 Оценку общей АОА осуществляли методом ХЛ, определяя коэффициент Imax/S30. Устанавливали также содержание в РЖ белка церулоплазмина (ЦП) как одного из основных антиоксидантов. Количество ЦП (КФ 1.16.3.1) измеряли в реакции окисления парафенилендиамина дигидрохлорида по В.С. Камышникову [5]. Активность гамма-глутамилтранспептидазы (ГГТП) (К.Ф. 2.3.2.2) изучали унифицированным методом с субстратом гамма-глутамил-3-карбокси-4-нитроанилидом по А.И. Карпищенко [8]. Полученный цифровой материал обработан методом вариационной статистики на IBM с использованием программы Biostat и Statistica 6.0. с определением M±m; достоверность различий определяли по t-критерию Стьюдента.
Оценку общей АОА осуществляли методом ХЛ, определяя коэффициент Imax/S30. Устанавливали также содержание в РЖ белка церулоплазмина (ЦП) как одного из основных антиоксидантов. Количество ЦП (КФ 1.16.3.1) измеряли в реакции окисления парафенилендиамина дигидрохлорида по В.С. Камышникову [5]. Активность гамма-глутамилтранспептидазы (ГГТП) (К.Ф. 2.3.2.2) изучали унифицированным методом с субстратом гамма-глутамил-3-карбокси-4-нитроанилидом по А.И. Карпищенко [8]. Полученный цифровой материал обработан методом вариационной статистики на IBM с использованием программы Biostat и Statistica 6.0. с определением M±m; достоверность различий определяли по t-критерию Стьюдента.
Результаты и обсуждение
Скрининговое определение лактата показало, что образование молочной кислоты увеличивалось после употребления сахарсодержащих продуктов — фиолетовое окрашивание исходного раствора фенолята железа в реакции Уфельмана сменилось на желтое после добавления раствора, содержащего повторно снятый зубной налет; жевание резинки Орбит, в которой содержатся сахарозаменители — сорбит, аспартат и др.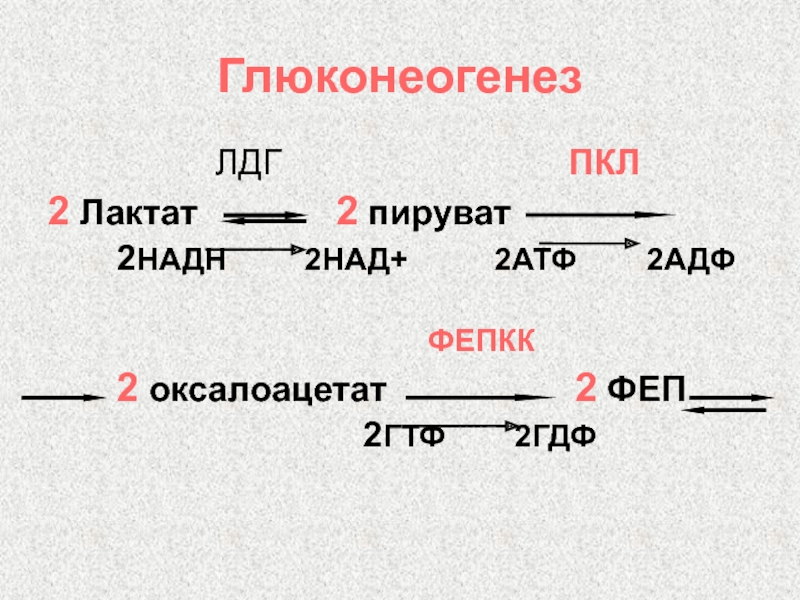 , т.е. вещества, не содержащие сахарозу, снижало образование лактата в зубном налете (желтое окрашивание не появлялось, сохранялась фиолетовая окраска).
, т.е. вещества, не содержащие сахарозу, снижало образование лактата в зубном налете (желтое окрашивание не появлялось, сохранялась фиолетовая окраска).
У лиц, употреблявших сахарсодержащие продукты, установлено достоверное снижение на 57,8% АОА на фоне активации процессов ЛПО в ротовой жидкости (S30 составила 978,4±67,4 кФотон, максимальная вспышка ХЛ — 101,4±4,2 кФотон) по сравнению с таковой в контроле (светосумма ХЛ — 486,6±42,4 кФотон, Imax — 63,9±2,8 кФотон соответственно). Отмечалось адаптивное возрастание количества ЦП — основного антиоксиданта (табл. 1). Эти данные подтверждают значение гематосаливарного барьера [10, 11]. Слюна является не только связующим звеном в обмене низкомолекулярных веществ в системе «кровь — желудочно-кишечный тракт — кровь», но и связующей и «конечной» жидкостью организма, которая позволяет выделить из организма наряду с мочой и потом избыток некоторых веществ и метаболитов.
Применение жевательной резинки Орбит (2-я группа) сопровождалось тенденцией к возрастанию процессов ЛПО, однако эти данные недостоверны. При этом возрастал уровень антиоксиданта ЦП в РЖ и достоверно повышалась энзиматическая активность ГГТП, что в конечном счете направлено на восстановление антиоксиданта глутатиона.
При этом возрастал уровень антиоксиданта ЦП в РЖ и достоверно повышалась энзиматическая активность ГГТП, что в конечном счете направлено на восстановление антиоксиданта глутатиона.
Выявленные нарушения оксидантно-антиоксидантного баланса коррелировали с количественными сдвигами в уровнях ОБ, креатинина, глюкозы, лактата, пирувата, ферментативной активности ЛДГ, АСТ и АЛТ (табл. 2).
Таким образом, нами подтвержден факт усиления процессов гликолиза в РЖ с образованием лактата после употребления сахарсодержащих продуктов, что сопровождается активацией процессов свободнорадикального окисления (СРО) и снижением антиоксидантной защиты. Сахарозаменители не вызывают достоверных сдвигов процессов ЛПО и способствуют повышению содержания ферментов-антиоксидантов в РЖ.
Результаты исследования могут быть рекомендованы для неинвазивной оценки в стоматологической практике процессов СРО и метаболизма.
Лактат (Молочная кислота)
Лактат (Молочная кислота)Лактат или молочная кислота – это показатель кислотно-основного баланса в организме, он указывает на снижение кровотока в тканях и органах.
Лактат образуется в результате анаэробного (бескислородного) метаболизма глюкозы. При достаточном количестве кислорода в тканях превращения глюкозы заканчиваются образованием пирувата, который затем распадается до углекислоты и воды. Но при недостаточном поступлении кислорода с током крови (анаэробные условия) пируват превращается в лактат под контролем фермента лактатдегидрогеназы. Наибольшее количество молочной кислоты образуется в поперечнополосатой мускулатуре (мышцы скелета), в клетках головного мозга и эритроцитах.
Чем больше накапливается молочной кислоты в мышцах при физической нагрузке, тем сильнее человек чувствует усталость. Из крови лактат выводят печень и почки. Печень может поглощать молочную кислоту только до определённого предела, который называется «лактатный порог». Если после его достижения образование лактата продолжается, его концентрация в крови увеличивается импульсно, а не постепенно.
Накопление в организме лактата приводит к закислению крови, сдвигу её рН в кислую сторону, что называется лактатный ацидоз. Он развивается при снижении поступления кислорода к органам и тканям, при уменьшении кровотока (сепсис, шок при отёке лёгких или при сердечной недостаточности). Причиной лактатного ацидоза может стать и избыточное образование молочной кислоты при чрезмерных физических нагрузках, судорожных припадках, при некоторых опухолях (лимфома), при алкогольной интоксикации вследствие нарушения функции печени. Выработка молочной кислоты усиливается при дефиците витамина В1 (тиамина). Лекарственные препараты, провоцирующие развитие лактатацидоза, — адреналин и нитропруссид натрия.
Он развивается при снижении поступления кислорода к органам и тканям, при уменьшении кровотока (сепсис, шок при отёке лёгких или при сердечной недостаточности). Причиной лактатного ацидоза может стать и избыточное образование молочной кислоты при чрезмерных физических нагрузках, судорожных припадках, при некоторых опухолях (лимфома), при алкогольной интоксикации вследствие нарушения функции печени. Выработка молочной кислоты усиливается при дефиците витамина В1 (тиамина). Лекарственные препараты, провоцирующие развитие лактатацидоза, — адреналин и нитропруссид натрия.
Изменение рН крови в кислую сторону (ацидоз) требует проведения лечебных мероприятий, поскольку представляет опасность для организма.
Для подтверждения лактатного ацидоза необходимо наличие двух параметров:
- повышение концентрации молочной кислоты в крови,
- показатель соотношения лактат/пируват больше 10/1.
Показания к выполнению анализа
Оценка кислотно-основного состояния у пациентов реанимации.
Диагностический поиск причины метаболического ацидоза (лактатный ацидоз является одним из его видов).
Оценка снабжения тканей кислородом при шоке.
Дифференциальная диагностика миопатий.
Диагностика энзимопатии новорождённых.
Диагностика асфиксии новорождённых.
Подготовка к исследованию
За сутки до исследования не принимать спиртные напитки, жирную пищу, ограничить физические нагрузки.
Кровь на исследование сдают утром натощак, исключается даже чай или кофе. Допустимо пить обычную воду.
Временной интервал между последним приёмом пищи и взятием крови на исследование – не менее восьми часов.
Взятие крови желательно выполнять без использования жгута либо накладывать жгут не дольше, чем на 30 секунд.
Центрифугирование крови выполняется в максимально короткие сроки после взятия материала на исследование, плазму нужно быстро отделить от клеток.
Материал для исследования
Венозная кровь или артериальная кровь.
Интерпретация результатов
Норма:
- в венозной крови — 0,63 – 2,44 ммоль/л;
- в артериальной крови — 0,56 – 1,67 ммоль/л.
Повышение:
1. Большая физическая нагрузка (у спортсменов).
2. Нарушение кровообращения: кардиогенный шок, выраженная сердечно-сосудистая недостаточность.
3. Сахарный диабет 2 типа.
4. Столбняк, тетания, эпилептический припадок и другие судорожные состояния.
5. Нарушения функции печени: острый гепатит, терминальная стадия цирроза печени.
6. Злокачественные опухоли (лимфома, лейкемия).
7. Анемия.
8. Хронический алкоголизм.
9. Дефицит витамина В1.
10. Приём лекарственных препаратов – адреналина, нитропруссида натрия.
Практическое значение уровня лактата в крови плода при неотложном его состоянии
HEALTH OF WOMAN.2017.1(117):120–122; doi 10.15574/HW.2017.117.120
Пехньо Н. В.
Национальная медицинская академия последипломного образования имени П. Л. Шупика, г. Киев
Л. Шупика, г. Киев
Цель исследования: установить, может уровень лактата в крови плода быть достоверным критерием его страдания и показанием к изменению тактики ведения родов.
Материалы и методы. В исследование были включены 511 беременных. Критерии включения в исследование: роды при доношенной одноплодной беременности, головное предлежание плода, отсутствие плодных оболочек, раскрытие шейки матки 3 см и более, сомнительное состояние плода по данным КТГ. Включены в исследование беременные рандомизированы на 2 группы.
В основную группу вошли 253 роженицы, у которых состояние плода при КТГ оценено как сомнительное и определен уровень лактата в крови, взятой из кожи предлежащей головки плода. Уровень лактата определяли малообъемным методом с использованием коммерческих стрип-тестов (Lactate Pro, Arkray, Kyoto, Japan). Тактику родов определяли в зависимости от уровней лактата: при <4,2 ммоль/л – ведение родов согласно акушерской ситуацией; 4,2-4,8 ммоль/л – исследование повторить через 20 мин; если уровень лактата нормализовался – ведение родов согласно акушерской ситуации; при отсутствии нормализации или повышение — оперативное родоразрешение; при уровне >4,8 ммоль/л – экстренное оперативное родоразрешение.
В группу сравнения вошли 258 рожениц с сомнительным состоянием плода, у которых определение уровня лактата не проводили. Тактику родов у пациенток этой группы определяли в соответствии с рекомендациями и нормативными документами МОЗ Украины.
Результаты. Апробирована методика определения уровня лактата крови плода технически проста, позволяет быстро получить результаты, хорошо переносится роженицами. не имеет существенных осложнений. Уровень лактата крови плода является чувствительным маркером неотложного состояния плода и поэтому является полезным критерием для изменения тактики ведения родов. В результате применения апробированного метода удалось улучшить состояние новорожденных при снижении частоты оперативного родоразрешения, что составило 18,2% у рожениц основной группы и 33,72% в группе сравнения (р <0,01).
Заключение. 1. Определение уровня лактата в крови, взятой из кожи предлежащей головки плода малообъемным методом с использованием коммерческих стрип-тестов (Lactate Pro, Arkray, Kyoto, Japan), позволяет быстро получить данные о наличии ацидоза у плода.
2. Уровень лактата в крови плода может служить диагностическим критерием его страдания и показанием к изменению тактики ведения родов в этой связи.
3. Простота и скорость выполнения данной методики позволяет рекомендовать ее к применению в акушерской практике.
Ключевые слова: неотложное состояние плода, лактат крови плода, тактика ведения родов.
Литература:
1. East CE, Leader LR, Sheehan P, Henshall NE, Colditz PB. Intrapartum fetal scalp lactate sampling for fetal assessment in the presence of a non-reassuring fetal heart rate trace. Cochrane Database Syst Rev 2010; (3): CD 006174.
2.Kruger K, Hallberg B, Blennow M, Kublickas M, Westgren M. Predictive value of fetal scalp blood lactate concentration and pH as markers of neurologic disability. Am J Obstet Gynecol 1999;181:1072–8. https://doi.org/10.1016/S0002-9378(99)70083-9
3. Ramanah R., Martin A., Rieth-muller D. Value of fetal scalp lactate sampling during labour: a comparative study with scalp pH // Gynecol. Obstet. Fertil. – 2005. – Vol. 33, 3. – P. 107–112. https://doi.org/10.1016/j.gyobfe.2005.01.004; PMid:15848081
Obstet. Fertil. – 2005. – Vol. 33, 3. – P. 107–112. https://doi.org/10.1016/j.gyobfe.2005.01.004; PMid:15848081
4. Chandraharan E. Fetal scalp blood sampling during labour: is it a useful diagnostic test or a historical test that no longer has a place in modern clinical obstetrics BJOG 2014;121:1056–62. https://doi.org/10.1111/1471-0528.13162; https://doi.org/10.1111/1471-0528.12614; https://doi.org/10.1111/1471-0528.13125
5. National Institute for Health and Care Exellence. Inpartum care: case of healthy women and their babies during child-bihrth. NICE clinical guideline 190, (Manchester): NICE; 2014.
6. Martin A. Fetal heart rate during labour: definitions and interpretations // J/ Gynecolog. Obstet. Biol. Reprod. (Paris). – 2003. – Vol. 37 (Suppl. 1). – S34–S35. https://doi.org/10.1016/j.jgyn.2007.11.009; PMid:18191915
7. Holzmann M, Wretler S, Cnat-tingius S, Nordstrim L. Cardio tocography patterns and risk of inpartum fetal fcidemiya. J. Perinat. Med 2014. Jun 10.
Med 2014. Jun 10.
8. MacLennan A. A template for defining a causal relation between acute intrapartum events and cerebral palsy: international consensus statement // Br. Med. J. – 1999. – Vol. 319. – P. 1054–1059. https://doi.org/10.1136/bmj.319.7216.1054
Новые представления о роли лактата при шоке (обзор литературы) Текст научной статьи по специальности «Фундаментальная медицина»
НОВЫЕ ПРЕДСТАВЛЕНИЯ О РОЛИ ЛАКТАТА ПРИ ШОКЕ (ОБЗОР ЛИТЕРАТУРЫ)
NEW PERCEPTIONS ABOUT THE ROLE OF LACTATE IN SHOCK (LITERATURE REVIEW)
Устьянцева И.М. Ustyantseva I.M.
Хохлова О.И. Khokhlova O.I.
Федеральное государственное Federal State
лечебно-профилактическое учреждение Medical Prophylactic Institution
«Научно-клинический центр охраны здоровья шахтеров», «Scientific Clinical Center of Miners’ Health Protection»,
г. Ленинск-Кузнецкий, Россия Leninsk-Kuznetsky, Russia
Ленинск-Кузнецкий, Россия Leninsk-Kuznetsky, Russia
Определение содержания лактата в крови — важный метод мониторинга состояния пациентов с тканевой гипоксией. Однако при эндотоксикозе/сепси-се производимый лактат является не только результатом гипоксии тканей, но его формирование также связано с повышенным аэробным гликолизом, стимулируемым эпинефрином через активирование №+/К+-АТФазы. Усиленное образование молочной кислоты можно рассматривать как адаптивное явление, нацеленное на противодействие энергетическому кризису. При этом молочная кислота выступает в качестве энергетического субстрата, прежде всего, для сердечной мышцы. Переход с главных энергетических субстратов миокарда к гликолизу может сохранить или даже улучшить функционирование сердца.
Ключевые слова: лактат; шок; сепсис; биоэнергетика миокарда.
Definition of lactate concentrations in blood is an important method for monitoring of condition of patients with tissue hypoxia. However, during en-dotoxicosis/sepsis, produced lactate is not only the result of tissue hypoxia, but its formation is also connected to increased aerobic glycolysis stimulated by epinephrine through Na+/K+-ATPase activation. The increased lactate production can be considered as adaptive event aimed at counterwork to energy crisis. At that, lactate acts as energetic substrate, first of all for cardiac muscle. Transition from the main myocardium energetic substrates to glycolysis can save or even improve cardiac function.
However, during en-dotoxicosis/sepsis, produced lactate is not only the result of tissue hypoxia, but its formation is also connected to increased aerobic glycolysis stimulated by epinephrine through Na+/K+-ATPase activation. The increased lactate production can be considered as adaptive event aimed at counterwork to energy crisis. At that, lactate acts as energetic substrate, first of all for cardiac muscle. Transition from the main myocardium energetic substrates to glycolysis can save or even improve cardiac function.
Key words: lactate; shock; sepsis; myocardium bioenergetics.
Лактат (молочная кислота) — один из метаболитов окислительных превращений глюкозы. Он был открыт шведским химиком Карлом Вильгельмом Шееле в 1780 г. [9]. С тех пор роль лактата интенсивно изучается физиологами, биохимиками, а также врачами отделений интенсивной терапии. Определение содержания лактата в крови представляет собой важный метод мониторинга пациентов с тканевой гипоксией. Его широко используют в качестве экспресс-теста у больных в критическом состоянии или с высоким риском декомпенсации.
Его широко используют в качестве экспресс-теста у больных в критическом состоянии или с высоким риском декомпенсации.
Уровень лактата в крови — результат динамического равновесия образования и утилизации этого метаболита. Его повышение может быть обусловлено усиленной продукцией и/или пониженным расходованием [5]. Хотя лактат продуцируют все органы и ткани, основное его количество образуется в мозге, эритроцитах, скелетных мышцах и коже, откуда он поступает в кровь. Утилизируется же лактат, главным образом, в печени,
почках и сердечной мышце, где он используется на энергетические цели и синтез глюкозы (глюконеоге-нез). При достаточном снабжении тканей кислородом глюкоза окисляется до СО2 и воды с выделением энергии. В условиях недостаточного поступления кислорода в тканях усиливаются анаэробные процессы, сопровождающиеся образованием значительно большего количества лактата, который накапливается в тканях и крови с последующим развитием лактат-ацидоза [1].
Гиперлактатемия — одно из самых распространенных метаболических нарушений у больных в критическом состоянии. Многочисленными исследованиями установлено, что уровень лактата в крови и/или лактатный клиренс является диагностическим, терапевтическим и прогностическим маркером тканевой гипоксии при циркуляторном шоке [8, 17, 23]. При определенных расстройствах источник высокого содержания молочной кислоты в крови не вызывает сомнений. Например, показано, что уровень лактата в плазме может временно
находиться на отметке 15 мМоль/л при большом эпилептическом припадке [20], а также пропорционально отражать суммарный дефицит кислорода при геморрагическом шоке [26]. В этом контексте лактат традиционно рассматривается как конечный метаболический продукт гликолиза по причине гипоксии. Однако недавно система понятий о молочной кислоте изменилась, а источник продукции лактата и его роль в качестве энергетического субстрата исследовали повторно [14, 15], в частности, при системном воспалении и сепсисе [16, 21]. Так, рядом авторов предполагается, что чрезмерная продукция молочной кислоты при сепсисе не обязательно связана с анаэробным метаболизмом, она может быть также обусловлена недостаточной доставкой кислорода вследствие воздействия эпинефрина (адреналина) на активность мембранного фермента №+/К+-АТФазу [6, 21, 22]. В этом процессе АДФ, генерируемая №+/К+-АТФазой, ускоряет аэробный гликолиз и, как следствие, увеличивает концентрацию молочной
Так, рядом авторов предполагается, что чрезмерная продукция молочной кислоты при сепсисе не обязательно связана с анаэробным метаболизмом, она может быть также обусловлена недостаточной доставкой кислорода вследствие воздействия эпинефрина (адреналина) на активность мембранного фермента №+/К+-АТФазу [6, 21, 22]. В этом процессе АДФ, генерируемая №+/К+-АТФазой, ускоряет аэробный гликолиз и, как следствие, увеличивает концентрацию молочной
ПОЛИТРАВМА
кислоты. Еще одно важное открытие — распознание действия лакта-та как подвижного метаболита, распределяемого через системный кровоток к различным органам, тканям и клеткам для окисления или переработки, что позволяет поддерживать доставку энергии в виде АТФ [14-16]. В конечном счете, лактат можно рассматривать как сигнальную молекулу, участвующую в регуляции окислительно-восстановительного состояния клетки и окислительной защите [3].
Представляет несомненный интерес комплексное экспериментальное исследование Levy В. et al. (2007), проводимое на краткосрочной летальной модели эндотоксического шока у анестезируемых и вентилируемых крыс, в котором авторы попытались определить, связана ли продукция молочной кислоты в мышцах с Р2-адренергической стимуляцией, и изменяет ли ограниченная системная доступность лактата деятельность сердечно-сосудистой системы [19]. Первую гипотезу проверяли с помощью выборочной блокады Р2-адренер-гического пути в тканях при введении ICI-118551 через катетеры для микродиализа; это позволило авторам установить, что местная продукция молочной кислоты в мышцах связана со стимуляцией эпинефрином аэробного гликолиза (опосредованного Na+/IK+-AT-Фазой через Р2-адренорецепторы). Для проверки второй гипотезы достигали системного отклонения лактата через внутривенное введение или, выборочно, Р2-ингибитора (ICI-118551), или активатора пиру-ватдегидрогеназы (дихлорацетата), или с помощью комбинации этих двух веществ.
et al. (2007), проводимое на краткосрочной летальной модели эндотоксического шока у анестезируемых и вентилируемых крыс, в котором авторы попытались определить, связана ли продукция молочной кислоты в мышцах с Р2-адренергической стимуляцией, и изменяет ли ограниченная системная доступность лактата деятельность сердечно-сосудистой системы [19]. Первую гипотезу проверяли с помощью выборочной блокады Р2-адренер-гического пути в тканях при введении ICI-118551 через катетеры для микродиализа; это позволило авторам установить, что местная продукция молочной кислоты в мышцах связана со стимуляцией эпинефрином аэробного гликолиза (опосредованного Na+/IK+-AT-Фазой через Р2-адренорецепторы). Для проверки второй гипотезы достигали системного отклонения лактата через внутривенное введение или, выборочно, Р2-ингибитора (ICI-118551), или активатора пиру-ватдегидрогеназы (дихлорацетата), или с помощью комбинации этих двух веществ.
Авторы обнаружили, что подавление Р2-адренорецепторов значительно снижает вызванное эн-дотоксикозом увеличение местной мышечной продукции молочной кислоты; это подтверждает утверждение, что стимуляция лактатной продукции эпинефрином является вторичной по отношению к активации №+/К+-АТФазы. Наиболее поразительно, что ограниченная доступность в циркулирующих концентрациях молочной кислоты, вызванная и ICI-118551, и дихло-
Наиболее поразительно, что ограниченная доступность в циркулирующих концентрациях молочной кислоты, вызванная и ICI-118551, и дихло-
рацетатом, ассоциировалась с измененной биоэнергетикой сердца, что подтверждалось пониженным содержанием АТФ и фосфокреатина в сердце. Кроме того, дальнейшее уменьшение доступности молочной кислоты, возникающее в результате комбинированного введения Ю-118551 и дихлорацетата, вызывало состояние низкого кровотока с выраженной гипотензией и раннюю летальность. Коррекция же системного лактатного дефицита при добавлении лактата натрия к Ю-118551 или дихлорацетату прекращала гемодинамические нарушения; это поддерживает выводы авторов, что полученные результаты действительно связаны с потерей молочной кислоты.
Таким образом, приведенные данные показывают, что, во-первых, при эндотоксикозе/сепсисе производимый лактат является не только результатом гипоксии тканей, но его формирование также связано с повышенным аэробным гликолизом, стимулируемым эпинефрином (адреналином) через активирование №+/К+-АТФазы.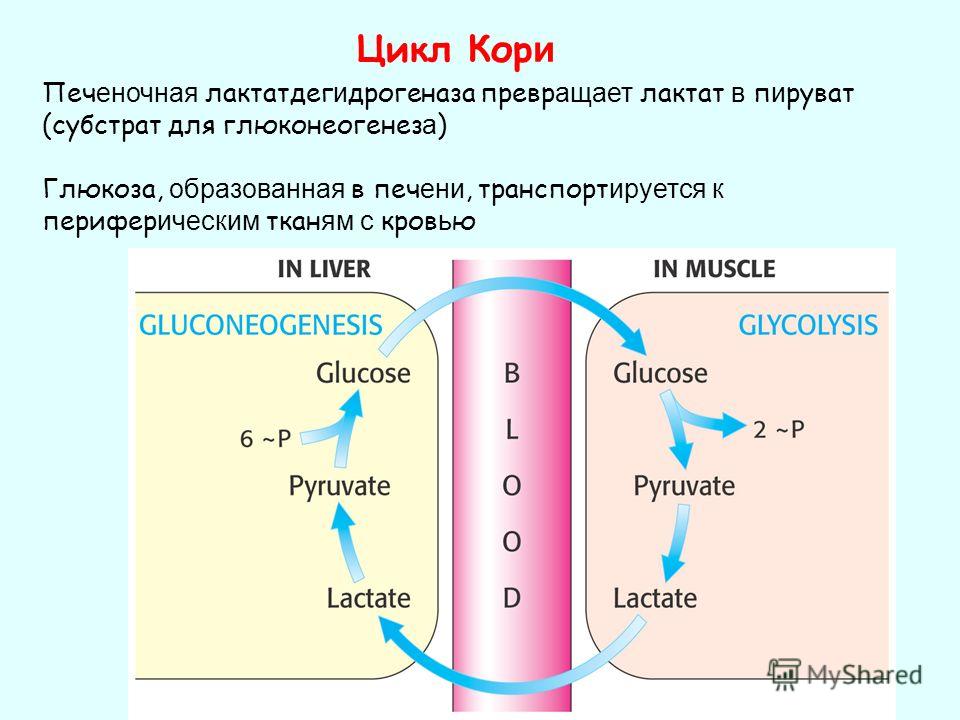 Во-вторых, наблюдаемые пагубные воздействия лактатного голодания на энергетический метаболизм сердца и гемодинамику четко поддерживают роль молочной кислоты как важного топлива для энергетики тканей, и усиленное образование молочной кислоты можно рассматривать как адаптивное явление, нацеленное на противодействие энергетическому кризису [15].
Во-вторых, наблюдаемые пагубные воздействия лактатного голодания на энергетический метаболизм сердца и гемодинамику четко поддерживают роль молочной кислоты как важного топлива для энергетики тканей, и усиленное образование молочной кислоты можно рассматривать как адаптивное явление, нацеленное на противодействие энергетическому кризису [15].
Сердце является органом, чрезвычайно подверженным нарушениям доставки субстратов. Сердечная мышца (миокард) — высоко окислительная ткань, которая производит более 90 % энергии за счет митохондриального дыхания. Оптимальный энергетический обмен и сократительная способность сердца определяются многими факторами, среди которых достаточная доставка кислорода и субстратов, окислительная способность митохондрий, достаточное количество высоко энергетического фосфата и соотношение фосфокреатин/АТФ. При физиологических состояниях сердце является метаболически всеядным органом, способным использовать широкий спектр субстратов:
жирные кислоты, глюкозу, лактат и другие окисляемые субстраты [4, 24]. В здоровом сердце 60-90 % ацетил-коэнзима А образуется в результате р-окисления жирных кислот, а 10-40 % — в результате окисления пирувата, образующегося в процессе гликолиза и окисления лактата [24].
В здоровом сердце 60-90 % ацетил-коэнзима А образуется в результате р-окисления жирных кислот, а 10-40 % — в результате окисления пирувата, образующегося в процессе гликолиза и окисления лактата [24].
К сожалению, имеется ограниченное количество данных относительно предпочтительного использования или лактата, или глюкозы, или жирных кислот, или других субстратов сердечной мышцей при сепсисе, особенно, когда доступны все эти потенциальные субстраты. Благодаря работам Levy В. et al, мы имеем представление о том, что происходит с животными, в организме которых содержатся эндотоксины, и которые не способны повысить продукцию молочной кислоты [19]. Имеются также данные, показывающие, что переход с главных энергетических субстратов миокарда к гликолизу может сохранить или даже улучшить функционирование миокарда [10, 11]. Переход от липидного к избирательному углеводному окислению позволяет улучшить взаимосвязь между потреблением миокардом кислорода и механической работой [12].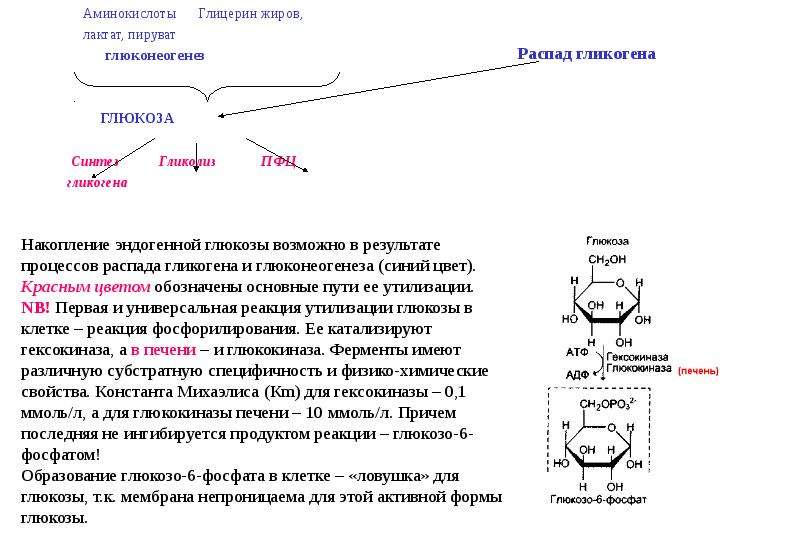 Это отражает высокую степень митохон-дриального дыхания, когда глюкоза используется в качестве топлива, что является метаболической адаптацией к условиям ограниченной доступности кислорода [7].
Это отражает высокую степень митохон-дриального дыхания, когда глюкоза используется в качестве топлива, что является метаболической адаптацией к условиям ограниченной доступности кислорода [7].
Кроме того, повышенная экспрессия переносчика лактата МСТ1 (т.е. система монокарбоксилат-транс-портного белка, позволяющая вводить лактат в клетки) в экспериментальной модели сердечной недостаточности также указывает на то, что такая метаболическая адаптация благоприятствует избирательному метаболизму молочной кислоты [23]. В конце концов, утверждение, что лактат является важным субстратом для энергетического обмена в миокарде, подтверждается как экспериментальными данными, так и результатами исследования людей: высокие уровни молочной кислоты сохраняли гемодинамические функции у крыс и собак с кровотечением [2, 13], а экзогенный лактат повышал
№ 2 [июнь] 2009
сердечный индекс у пациентов после операций на сердце [18].
Результаты исследования Levy В. et al. [19] важны и перспективны, однако без полноценной оценки сердечной функции и точных знаний о действительном цикле образования энергии АТФ и метаболическом пути молочной кислоты в миокарде невозможно интерпрети-
Литература:
ровать полученные данные. Необходимы дальнейшие исследования для определения точных молекулярных механизмов, ответственных за изменения метаболического фенотипа миокарда, которые происходят при сепсисе и шоке.
Таким образом, исследование Levy В. et al. (2007) открывает новую концепцию действия молочной
кислоты как важного энергетического субстрата при шоковых состояниях. Мы только начинаем понимать многогранную роль лактата у больных в критическом состоянии, что может, в конечном счете, привести к новым подходам, нацеленным на увеличение энергетической эффективности работы сердца и других органов.
1. Биохимия человека. В 2-х т. Т. 1: пер. с англ. /Р. Мари, Д. Грен-нер, П. Мейес, В. Родуэлл. — М.: Мир, 2004. — 381 с.
2. Barbee, R.W. Depletion of lactate by dichloroacetate reduces cardiac efficiency after hemorrhagic shock /R.W. Barbee, J.A. Kline, J.A. Watts //Shock. — 2000. — Vol. 14. — P. 208-214.
3. Brooks, G.A. Laclale shuttles in nature /G.A. Brooks //Biochem. Soc. Trans. — 2002. — Vol. 30. — P. 258-264.
4. Chatham, J.C. Lactate-the forgotten fuel! /J.C. Chatham //J. Physi-ol. — 2002. — Vol. 542. — P. 333.
5. De Backer, D. Lactic acidosis /D. De Backer //Intensive Care Med.
— 2003. — Vol. 29. — P. 699-702.
6. Endoloxemia stimulates skeletal muscle Na+K+-ATPase and raises blood lactate under aerobic conditions in humans /H. Bundgaard, K. Kjeldsen, K. Suarez Krabbe [et al.] //Am. J. Physiol. Heart Circ. Physiol. — 2003. — Vol. 284. — P. h2028-h2034.
Endoloxemia stimulates skeletal muscle Na+K+-ATPase and raises blood lactate under aerobic conditions in humans /H. Bundgaard, K. Kjeldsen, K. Suarez Krabbe [et al.] //Am. J. Physiol. Heart Circ. Physiol. — 2003. — Vol. 284. — P. h2028-h2034.
7. Enhanced cardiac metabolism of plasma glucose in high-altitude natives: adaptation against chronic hypoxia /J.E. Holden, C.K. Stone, C.M. Clark [et al.] //J. Appl. Physiol. — 1995. — Vol. 79. — P. 222-228.
8. Hemodynamic variables related to outcome in septic shock /M. Varpula, M. Tallgren, K. Saukkonen [et al.] //Intensive Care Med. — 2005. — V. 231. — P. 1066-1071.
9. Holten, C.H. Lactic acid: property and chemistry of lactic acid and derivates /C.H. Holten, A. Muller, D. Rehbinder. — Verlag Chemie, Weinheim, 1971.
10. Improved systolic and diastolic myocardial function with intracoro-nary pyruvate in patients with congestive heart failure /H. P. Hermann, J. Arp, B. Pieske [et al.] //Eur. J. Heart Fail. — 2004. — Vol. 6.
P. Hermann, J. Arp, B. Pieske [et al.] //Eur. J. Heart Fail. — 2004. — Vol. 6.
— P. 213-218.
11. Influence of pyravate on contractile performance and Ca (2+) cycling in isolated failing human myocardium /G. Hasenfuss, L.S. Maier, H.P. Hermann [et al.] //Circulation. — 2002. — Vol. 105. — P. 194-199.
12. Korvald, C. Myocardial substrate metabolism influences left ventricular energetics in vivo /C. Korvald, O.P. Elvenes, T. Myrmel //Am. J. Physiol. Heart Circ. Physiol. — 2000. — Vol. 278. — P. h2345-h2351.
13. Lactate improves cardiac efficiency after hemorrhagic shock /J.A. Kline, L.R. Thornton, G.D. Lopaschuk [et al.] //Shock. — 2000.
— Vol. 14. — P. 215-221.
14. Lactate metabolism in acute uremia /X. Leverve, I. Mustafa, I. Novak [et al.] //J. Ren. Nutr. — 2005. — Vol. 15. — P. 58-62.
Lactate metabolism in acute uremia /X. Leverve, I. Mustafa, I. Novak [et al.] //J. Ren. Nutr. — 2005. — Vol. 15. — P. 58-62.
15. Leverve, Х.М. Energy metabolism in critically ill patients: lactate is a major oxidizable substrate /Х.М. Leverve //Curr. Opin. Clin. Nutr. Metab. Care. — 1999. — Vol. 2. — P. 165-169.
16. Levy, В. Lactate and shock state: the metabolic view /В. Levy //Curr. Opin. Crit. Care. — 2006. — Vol. 12. — P. 315-321.
17. Low exogenous lactate clearance as an early predictor of mortality in normolactatemic critically ill septic patients /J. Levraut, С. Ichai, I. Petit [et al.] //Crit. Care Med. — 2003. — Vol. 31. — P. 705-710.
ПОЛИТРАВМА
18. Mustafa, I. Metabolic and hemodynamic effects of hypertonic solutions: sodium-lactale versus sodium chloride infusion in postoperative patients /I.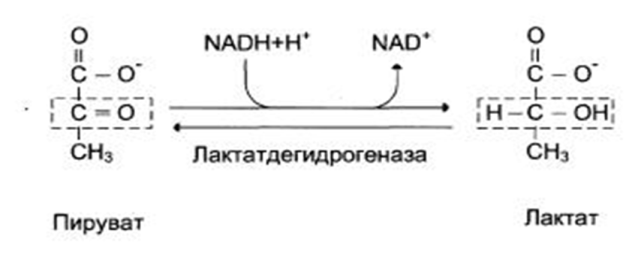 Mustafa, X.M. Leverve //Shock. — 2002. — Vol. 18.
Mustafa, X.M. Leverve //Shock. — 2002. — Vol. 18.
— P. 306-310.
19. Myocardial lactate deprivation is associated with decreased cardiovascular performance, decreased myocardial energetics, and early death in endoloxic shock /B. Levy, A. Mansart, C. Montemont [et al.] //Intensive Care Med. — 2007. — Vol. 33, N 3. — P. 595-502.
20. Natural history of lactic acidosis after grand-mal seizures. A model for the study of an union-gap acidosis not associated with hyperkalemia /C.E. Orringer, J.C. Eustace, C.D. Wunsch, L.B. Gardner //N. Engl. J. Med. — 1977. — Vol. 297. — P. 796-799.
21. Relation between muscle Na+K+-ATPase activity and raised lactate concentrations in septic shock: a prospective study /B. Levy, S. Gibot, P. Franck [et al.] //Lancet. — 2005. — Vol. 365. — P. 871-875.
22. Role of skeletal muscle Na+K-t-ATPasc activity in increased lactate production in sub-acute sepsis /F.D. McCarter, S.R. Nierman, J.H. James [et al.] //Life Sci. — 2002. — Vol. 70. — P. 1875-1888.
23. Serum lactate and base deficit as predictors of mortality and morbidity /F.A. Hussain, M.J. Martin, P.S. Mullenix [et al.] //Am. J. Surg.
— 2003. — Vol. 185. — P. 485-491.
24. Stanley, W.C. Myocardial substrate metabolism in the normal and failing heart /W.C. Stanley, F.A. Recchia, G.D. Lopaschuk //Physiol. Rev. — 2005. — Vol. 85. — P. 1093-1129.
25. Upregulation of the cardiac monocarboxylate transporter MCT1 in a rat model of congestive heart failure /E. Johannsson, P.K. Lunde, C. Heddle [et al.] //Circulation. — 2001. — Vol. 104. — P. 729-734.
26. Weil, M.H. Experimental and clinical studies on lactate and pyruvate as indicators of the severity of acute circulatory failure (shock) /M.H. Weil, A.A. Afifi //Circulation. — 1970. — Vol. 41. — P. 9891001.
Сведения об авторах:
Хохлова О.И., д.м.н., врач клинической лабораторной диагностики, Федеральное государственное лечебно-профилактическое учреждение «Научный клинический центр охраны здоровья шахтеров», г. Ленинск-Кузнецкий, Россия.
Устьянцева И.М., д.б.н., профессор, заместитель директора по клинической лабораторной диагностике, Федеральное государственное лечебно-профилактическое учреждение «Научный клинический центр охраны здоровья шахтеров», г. Ленинск-Кузнецкий, Россия.
Адрес для переписки:
Хохлова О.И., 7-й микрорайон, № 9, ФГЛПУ «НКЦОЗШ», Ленинск-Кузнецкий, Кемеровская область, Россия, 652509
8 (38456) 2-54-52, 9-54-57
E-mail: [email protected]
Information about authors:
Khokhlova O.I., PhD, physician of clinical laboratory diagnostics, Federal state medical prophylactic institution «Scientific clinical center of miners’ health protection», Leninsk-Kuznetsky, Russia.
Ustyantseva I.M., Doctor of Biological Science, professor, deputy director of clinical laboratory diagnostics, Federal state medical prophylactic institution «Scientific clinical center of miners’ health protection», Leninsk-Kuznetsky, Russia.
Adress for correspondence:
Khokhlova O.I., 7th district, 9, Federal state medical prophylactic institution «Scientific clinical center of miners’ health protection», Len-insk-Kuznetsky, Kemerovo region, Russia, 652509
8 (38456) 2-54-52, 9-54-57
E-mail: [email protected]
m
№ 2 [июнь] 2009
Обмен глюкозы и зачатие | Махмудов
1. Алимухамедов А. А. // Съезд физиологов Узбекистана, 4-й: Тезисы науч, сообщений.— Ташкент, 1988.— С. 39.
2. Вельтищев Ю. Е., Ермолаев М. В., Аноненко В. А., Князев Ю. А. Обмен веществ у детей.— М., 1983.
3. Воробьев Н. Н. // Изв. АН СССР. Сер. биол.— 1985,— № 1,— С. 61—70.
4. Држевецкая И. А. Эндокринная система растущего организма.— М., 1987.
5. Зыбина Т. Г. // Цитология.— 1983.— Т. 30, № 10.— С. 1180.
6. Каминский Ю. Г., Косенко Е. А. Парадоксы углеводного обмена.— Пущино, 1988.
7. Колесников С. И., Морозова Л. М. Генетико—физиологические взаимоотношения матери и плода.— Новосибирск, 1985.
8. Косенко Е. А., Каминский Ю. Г. Углеводный обмен, печень и алкоголь.— Пущино; 1988.
9. Махмудов Э. С., Алимухамедов А. А., Рахимов К. Р., Садыков Б. А. Рекомендации по снижению яловости коров и сохранению молодняка крупного рогатого скота в условиях Узбекистана. Информ, сообщение № 442.— Ташкент, 1988.
10. Махмудов Э. С., Ахмеров Р. Н., Алимухамедов А. А., Бабаева Р. Н. Реакция беременной самки и ее потомства на введение глюкозы и инсулина. Депонир. в ВИНИТИ 29.03.91 № В 82 — В 71.
11. Рахимов К. Р., Демидова А. И. Углеводы и механизмы их усвоения.— Ташкент, 1986.
12. Репин В. С. // Успехи соврем, биол.— 1976.— Т. 81,— С. 106—125.
13. Репин В. С. Критические факторы химической регуляции развития.— М., 1980.
14. Шевченко Т. К., Абдуллаев Н. X., Шамирзаев Н. X. Беременность и сахарный диабет.— Ташкент, 1988.
15. Юдаев М. А., Афиногенова С. А., Булатов А. А. и др. Цит. по Воробьеву Н. Н. // Изв. АН СССР. Сер. биол.— 1985,— № 1,— С. 61—70.
16. Anand R. S., Languli S., Sperling М. А. // Amer. J. Physiol.— 1980,— Vol. 238, N 6,— Р. 524—532.
17. Barz S., Jeige A., Mitzkat H. J. // Med. Klin.— 1985.— Bd 80, N 18.— S. 483—487.
18. Britta A., Mattson J. V., Rosenblum R. M. et al. .// Diabetes.— 1988,— Vol. 37, N 5,— P. 585—589.
19. Buch L., Hornes P. J., Kuhl C. // Acta endocr. (Kbh.).— 1986,— Vol. 112, N 2 — P. 263—266.
20. Buchanan T. A., Schemmer J. K., Frelnker N. // J. clin. Invest.— 1986,— Vol. 78, N 3.— P. 643—649.
21. Chovez D. J. // Europ. J. Cell Biol.— 1986.— Vol. 42, Suppl. 15.— P. 69.
22. Dieguez C., Page M. D., Peters T. R., Seaulon M. F. // J. roy. Coll. Phycns bond.— 1988.— Vol. 22, N 2,— P. 84—91.
23. Flood M. R„ Wiebold J. L. // J. Reprod. Fertil.—, 1988,— Vol. 84, N 1.— P. 7—12.
24. Galt A. L., Hardy K., Winston R. M. Z., Leess H. I. // Hum. Reprod.— 1990.— Vol. 5, N I.— P. 104—108.
25. Greengard O., Dowey H. K. // J. biol. Chem.— 1967.— Vol. 242,— P. 2968—2991.
26. Gilbert M., Hauguel S., Bouisset M. // Amer. J. Physiol.— 1981 — Vol. 247, N 5,— P. 574—580.
27. Gilbert M., Sparks 1. W., Girard J., Battaglia J. C. // Biol. Neonat.— 1985,— Vol. 48, N 2.— P. 90—99.
28. Girard J. R., Guillet J., Marty J. et al. // Diabetologia.— 1976,— Vol. 12, N 4,— P. 327—337.
29. Gonzalez- Willamer G., Argota-Espinosa R., Niz-Rames J. // Arch, invest. Med.— 1982,— Vol. 13, N 4,— P. 239— 244.
30. Hainz E. T., Nguyen V. V., Fussgahet R. D. // Biol. Neonate.—1982.— Vol. 41, N 5—6.— P. 240—245.
31. Hay W. W., Sparks J. W., Wilkening R. B. et al. // Amer. J. Physiol.— 1983,— Vol. 245, N 4,— P. E347—E350.
32. Horst C. J. G. // Cytobios.— 1986,— Vol. 45, N 181,— P. 85—95.
33. Itskovitz J., Hodgen G. D. // Psychoneuroendocrino— logy.— 1988,— N 1—2,— P. 155—170.
34. Jeung D., Oliver J. T. // Biochem. J.—1968.— Vol. 108, N 2,— P. 325—327.
35. Josimovich J. B. // Comparative Aspects of Reproductive Failure.— Berlin, 1967.— P. 176—185.
36. Khurana N. K., Wales R. G. // Aust. J. biol. Sci.— 1987 — Vol. 40, N 4,— P. 389—395.
37. Koski K. G„ Hill F. W., Harley L. S. // J. Nutr.— 1986,— Vol. 116, N 10,— P. 1922—1937.
38. Ktorra A., Nurjhan N., Girard J. R., Picon L. // Reprod. Nutr. Develop.— 1983.— Vol. 32, N 2.— P. 332—339.
39. Kozaric Z., Peternal P., Labunzija M. // Vet. Arch.— 1988 —Vol. 58, N 1,—P. 33—39.
40. Leturgue A., Hauguel S., Ferra P., Girard J. // Biol. Neonat.— 1987.— Vol. 51, N 2,— P. 64—69.
41. Leturgue A., Revelli J. P., Hauguel S. et al. // Amer. J. Physiol.— 1987,— Vol. 253, N 6,— Pt 1,— P. 616—620.
42. Manuelle P., Вис H. A., Plas Ch. // Biochim. biophys. Acta. Molec. Cell Res.— 1987,— Vol. 298, N 3,— P. 332—340.
43. Milner R. D., Hill D. I. // Clin. Endocr.— 1984.— Vol. 21, N 4,— P. 415—433.
44. Naismith D. J., Richardson D. P., Pritchard A. E. // Brit. J. Nutr.— 1982,— Vol. 48.— P. 433—441.
45. Nilsson В. O., Ostensson C. G., Eide S., Hellestrom С. // Endocrinology.— 1980.— Vol. 76, N 1,— P. 82—93.
46. Nitzan M. // Isr. J. med. Sci.— 1981.— Vol. 17, N 5.— P. 378—380.
47. Pinget M., Gander R., Jacques C. et al. // Path Biol.— 1982,— Vol. 30, N 1.— P. 43—48.
48. Rancin J. H. G., Sadarski G., Shanchan M. R. // J. Develop. Physiol.— 1986,— Vol. 8, N 4,— P. 247—253.
49. Singh V. H., Sabnis J. H. // Physiol, and Ecol.— 1986.— Vol. II, N 2,— P. 95—97.
50. Sitianou K., Henrichs J., Teller W. A. // Acta endocr. (Kbh.).— 1988,— Vol. 117, Suppl. 287,— P. 55—56.
51. Sutter-Dub M. T., Dozey B., Vergnaud M. Th., Modes A. M. // Horm. Metab. Res.— 1984.— Vol. 13, N 3.— P. 181 — 184.
52. Toyoda N., Murata K., Sugiama J. // Endocrinology.— 1982 — Vol. 116, N 3,— P. 998—1002.
53. Vilar R. C., Hicke Z. R. // Arch, invest. Med.— 1988,— Vol. 19, N 3.— P. 283—289.
54. Young A. A., Bogardus E., Stone K., Molt D. M. // Amer. J. Physiol.— 1988,— Vol. 254, N 2,— Pt I.— P. 231—236.
55. Zorzano A., Josuncion M. A., Herrera E. // Metabolism.— 1983 — Vol. 35, N 4,— P. 297—303.
Лактатный и лактоацидоз
Нормальное производство и метаболизм лактата [1]
Лактат, анион, образующийся в результате диссоциации молочной кислоты, является продуктом метаболизма глюкозы; в частности, это конечный продукт анаэробного гликолиза. Гликолитический путь (рис. 1), который может протекать анаэробно в цитоплазме всех клеток, представляет собой последовательность из 13 ферментативных реакций, в которых глюкоза превращается в пируват.
Во время этого преобразования богатый энергией аденозинтрифосфат (АТФ) вырабатывается из аденозиндифосфата (ADP), а восстановленный никотинамидадениндинуклеотид (NADH) вырабатывается из окисленного NAD (NAD + ).
Заключительным этапом анаэробного гликолиза является превращение пирувата в лактат под действием фермента лактатдегидрогеназы. Эта последняя реакция обеспечивает источник NAD + , необходимый для протекания анаэробного гликолиза. Производство лактата — единственное средство для утилизации глюкозы и производства АТФ в эритроцитах (у которых нет митохондрий) и в тренированных мышечных клетках (у которых есть кислородная задолженность).
В хорошо насыщенных кислородом тканевых клетках, содержащих митохондрии, пируват не преобразуется в лактат, а скорее метаболизируется в диоксид углерода и воду в митохондриях посредством двух интегрированных метаболических путей: цикла лимонной кислоты и окислительного фосфорилирования.
Превращение молекулы глюкозы в лактат (анаэробный гликолиз) дает всего две молекулы АТФ, тогда как преобразование в диоксид углерода и воду (аэробный гликолиз) дает гораздо более высокий выход энергии — 38 молекул АТФ.
РИС.1: Лактат — продукт анаэробного гликолиза
Хотя лактат может вырабатываться во всех тканях, скелетные мышцы, эритроциты, ткани головного мозга и мозгового вещества почек являются основными производственными участками здоровья. Нормальная суточная выработка лактата составляет порядка 1500 ммоль [1].Существует два основных пути удаления лактата: преобразование в пируват или выведение с мочой (рис. 2).
Хотя лактат свободно фильтруется в клубочках, он почти весь реабсорбируется и обычно
У этого пирувата две главные судьбы. Первый — это окисление до ацетил-КоА ферментом пируватдегидрогеназой для окончательного метаболизма до диоксида углерода и воды через цикл лимонной кислоты и окислительное фосфорилирование. Второй — это преобразование в глюкозу, процесс, называемый глюконеогенезом.Окисление пирувата через цикл лимонной кислоты потенциально может происходить во всех клетках с митохондриями, но глюконеогенез ограничен клетками печени и коры головного мозга почек.
По этой причине печень и почки являются наиболее важными органами для выведения лактата, на печень приходится около 60% циркулирующего лактата [4], а на почки — 25–30% [5]. В целом, организм обладает огромной способностью к удалению лактата, которая при необходимости (например, после экстремальных упражнений) может подняться до 500 ммоль / час, что значительно превышает базальную скорость выработки.
Рис. 2: Основные механизмы удаления лактата
Лактат, вырабатываемый эритроцитами, не может подвергаться дальнейшему метаболизму и попадает в кровоток. В некоторых тканях (например, в скелетных мышцах) лактат может вырабатываться более быстрыми темпами, чем он может метаболизироваться, и в этих обстоятельствах лактат также будет поступать в кровоток.
В здоровом состоянии концентрация лактата в крови поддерживается приблизительно в пределах 0.5-1,5 ммоль / л [6]. Это отражает баланс между скоростью высвобождения лактата в кровь из эритроцитов и других тканевых клеток и скоростью выведения лактата из крови, в основном печенью и почками.
Физические упражнения представляют собой физиологический процесс, в котором этот баланс временно нарушается из-за быстрого увеличения выработки лактата мышечными клетками при временной кислородной недостаточности. При тяжелых физических нагрузках уровень лактата в крови может повышаться до уровня, превышающего 20 ммоль / л, но из-за способности быстро выводить лактат для здоровья это повышение является временным.
Гиперлактатемия и лактоацидоз
Гиперлактатемия — это патологическое состояние, при котором концентрация лактата в крови в состоянии покоя аномально высока (> 1,5 ммоль / л). Умеренная или тяжелая гиперлактатемия (от> 3,0 до> 5,0 ммоль / л) связана с аномальным накоплением ионов водорода (H + ) и, как следствие, склонностью к ацидозу.
Эти ионы водорода являются продуктом гидролиза АТФ до АДФ [2]. В присутствии кислорода ионы водорода, образующиеся во время гидролиза АТФ, используются в митохондриальном процессе окислительного фосфорилирования, но это часто невозможно в контексте анаэробного гликолиза, связанного с образованием гиперлактата.
Вместо этого ионы водорода накапливаются в крови, в конечном итоге подавляя бикарбонат и другие буферные системы, которые поддерживают pH крови в пределах нормы (7,35-7,45). Комбинация гиперлактатемии и ацидоза называется лактоацидозом, и, хотя универсального согласия для определения лактоацидоза нет, наиболее широко используется лактат крови> 5,0 ммоль / л в сочетании с pH.
Лактоацидоз — наиболее частая причина метаболического ацидоза [8].
Причина гиперлактатемии и лактоацидоза — общие соображения
Гиперлактатемия развивается, когда скорость, с которой лактат выделяется из клеток периферической ткани в кровоток, превышает скорость, с которой он удаляется из кровотока печенью и почками.Причиной могут быть как повышенное производство лактата, так и снижение его выведения / метаболизма.
С биохимической точки зрения центральной проблемой обычно является снижение использования пирувата в окислительных или глюконеогенных путях. В этих условиях пируват может быть преобразован только в лактат. Например, поскольку кислород необходим для окисления пирувата, любое состояние, лишающее ткани кислорода, может привести к увеличению выработки лактата, который затем накапливается в крови с большей скоростью, чем может быть удален печенью и почками.
Проблема усугубляется ацидозом, потому что способность печени удалять лактат из кровотока зависит от pH и сильно ухудшается из-за пониженного pH крови. Фактически, экспериментальные данные свидетельствуют о том, что при pH крови 7,0 или ниже поглощение лактата настолько нарушено, что печень производит больше лактата, чем потребляет [9].
Существует некоторая компенсация со стороны почек, поскольку ацидоз увеличивает поглощение лактата почками [5]. Однако это может компенсировать только около 50% печеночной потери, а ацидоз, независимо от его причины, может быть основным фактором патогенеза гиперлактатемии.
Конкретные причины лактоацидоза
Традиционно лактоацидоз подразделяют на две широкие этиологические категории; Тип A и тип B. Тип A — это лактоацидоз, возникающий в результате гипоксии тканей (биохимический механизм, описанный выше), а тип B — это лактоацидоз, возникающий в контексте нормальной тканевой перфузии и адекватной глобальной оксигенации тканей.
Лактоацидоз типа А
Гипоксия тканей и лактоацидоз типа А возникают в результате недостаточной перфузии тканей при геморрагическом, кардиогенном и септическом шоке.Эти состояния, связанные с истощением объема и / или тяжелой гипотонией, могут быть результатом серьезной травмы / операции или острых заболеваний (например, инфаркт миокарда, системная инфекция), вызывающих сердечно-сосудистый коллапс.
Лактоацидоз типа А является признаком острого, опасного для жизни (критического) заболевания. Традиционно распространенное мнение о том, что лактоацидоз, возникающий в контексте сепсиса и септического шока, является единственным результатом гипоксии тканей, в настоящее время оспаривается (см. Ниже), и для тяжелобольных пациентов, состояние которых вызвано или осложнено инфекцией, различие между типом А и лактоацидоз типа B нечеткий и неприемлемый.
Перфузия — не единственный фактор, определяющий оксигенацию тканей, которая также зависит от достаточного количества кислорода в крови. Гипоксия тканей и, как следствие, лактоацидоз типа А могут, таким образом, возникать, несмотря на адекватную перфузию, если содержание кислорода в крови или способность крови переносить кислород в достаточной степени снижены.
Это механизм лактоацидоза типа А, который может возникать у пациентов с тяжелой анемией [10], тяжелой гипоксемией (например, дыхательной недостаточностью) [11] и отравлением угарным газом [12].На практике анемия и гипоксемия редко являются единственными причинами лактоацидоза типа А. Чаще они являются факторами, способствующими развитию лактоацидоза типа А у пациентов, которые уже предрасположены из-за недостаточной перфузии.
Сильное увеличение мышечной активности, которое происходит во время судорог, может вызвать лактоацидоз типа А из-за локальной гипоксии мышечной ткани, возникающей в результате временного несоответствия между потребностью в кислороде и поставкой кислорода (очень похоже на физиологический лактоацидоз, который возникает во время упражнений).Как и лактоацидоз, вызванный физической нагрузкой, лактоацидоз, вызванный судорогами, проходит самостоятельно, спонтанно разрешаясь в течение нескольких часов после прекращения судорог [13].
Лактоацидоз типа B
Если лактоацидоз возникает в контексте очевидной адекватной оксигенации тканей и нормальной гемодинамики (т. Е. Нормального артериального давления, отсутствия истощения объема, нормального содержания кислорода в крови и способности переносить кислород), его традиционно называют лактоацидозом типа B.
Жизненно важная роль печени и почек в поглощении лактата из кровотока и последующем метаболизме через цикл лимонной кислоты и глюконеогенез определяет, что заболевание печени и почек, независимо от его причины, предрасполагает к легкой гиперлактатемии и редко к лактоацидозу типа B.Злокачественное заболевание может быть связано с лактоацидозом, в большинстве случаев лактоацидоз типа B возникает при гематологических злокачественных новообразованиях (лейкоз, лимфома) [14].
Лактоацидоз типа B является признаком нескольких индивидуально очень редких наследственных заболеваний, которые характеризуются дефицитом определенных ферментов, участвующих в метаболизме лактата (глюконеогенез или окисление пирувата). К ним относятся дефицит пируваткарбоксилазы [15], дефицит глюкозо-6-фосфатдегидрогеназы (G6PD), дефицит фруктозо-1,6-дифосфатазы [16] и дефицит пируватдегидрогеназы, наиболее распространенные [17].Эти состояния вместе называются врожденным лактоацидозом.
Длинный список лекарств и токсинов может вызывать лактоацидоз (Таблица I), и вместе они представляют собой наиболее частую причину лактоацидоза типа B. Бигуаниды — это класс препаратов, снижающих уровень глюкозы в крови, используемых при лечении диабета; Метформин, который назначают чаще всего, был связан с лактоацидозом [18]. Однако в большинстве случаев метформин-ассоциированного лактоацидоза есть некоторые свидетельства нарушения функции печени или почек, которые предрасполагают к гиперлактатемии.
Бигуаниды (например, метформин) |
ТАБЛИЦА I: Некоторые препараты и токсины, которые могут вызывать лактоацидоз.
Метаболизм этанола связан с повышенным соотношением НАДН / НАД + , способствующим превращению пирувата в лактат [2].Глюконеогенез также подавляется, поэтому сочетание умеренной гиперлактатемии и гипогликемии является нередкой находкой у пациентов, страдающих острыми последствиями злоупотребления алкоголем.
Существовавшая ранее алкогольная болезнь печени усугубляет острую гиперлактатемию, вызывающую лактоацидоз типа B. Передозировка салицилата может быть связана с лактоацидозом из-за ингибирующего действия салицилата на окислительное фосфорилирование.
Подобный митохондриальный эффект объясняет лактоацидоз, возникающий при отравлении цианидом.У большинства пациентов с ВИЧ, которым прописаны антиретровирусные препараты, развивается легкая хроническая гиперлактатемия (лактат в сыворотке 1,5–3,5 ммоль / л) [19], а у небольшого непредсказуемого меньшинства она переходит в тяжелый лактоацидоз [20].
Лактоацидоз и сепсис
Представление о том, что лактоацидоз, возникающий в контексте критического заболевания, относится к типу А и, следовательно, всегда указывает на гипоксию тканей, явно чрезмерно упрощено. Пациенты в критическом состоянии с такой же вероятностью, как и любые другие, страдают лактоацидозом типа B, и при обследовании любого пациента (включая тех, кто находится в критическом состоянии) с повышенным содержанием лактата в крови необходимо должным образом учитывать причины лактоацидоза типа B, описанные выше.
Сепсис — это дополнительная и гораздо более серьезная осложняющая проблема, которая требует особого внимания, не в последнюю очередь потому, что это очень частая черта критических заболеваний. Сепсис — это состояние, при котором различие между лактоацидозом типа A и типа B неуместно, поскольку у некоторых пациентов с сепсисом лактат накапливается, несмотря на адекватную оксигенацию тканей [21].
Был предложен ряд механизмов накопления лактата при отсутствии тканевой гипоксии у пациентов с сепсисом.К ним относятся снижение выведения лактата из кровообращения печенью и почками [22]; специфический дефект фермента пируватдегидрогеназы, вызванный сепсисом, который нарушает утилизацию пирувата в цикле лимонной кислоты [23]; и увеличение производства пирувата [24].
Сепсис и септический шок связаны со стрессовой реакцией, включающей повышенное высвобождение адреналина (адреналина). Этот гормон стимулирует связанный с мембраной фермент Na + / K + -АТФаза, который использует АТФ, образующийся в результате аэробного гликолиза, для обеспечения энергии, необходимой для «перекачки» ионов в клетки и из них.Стимуляция Na + / K + -АТФазы увеличивает аэробный гликолиз и, следовательно, производство лактата.
Было высказано предположение, что гиперлактатемия, связанная с сепсисом, может быть, по крайней мере частично, результатом этого стимулируемого адреналином аэробного гликолиза [21].
Каким бы ни был механизм, ясно, что у многих, чье критическое заболевание вызвано инфекцией или осложнилось ею, лактоацидоз не обязательно является полностью результатом гипоксии тканей.В этих обстоятельствах меры, принятые для улучшения перфузии тканей, будут менее эффективными для снижения лактата в крови и разрешения ацидоза.
D-лактоацидоз
Это редкая и очень специфическая форма лактоацидоза, характерная для людей с синдромом короткой кишки и тех, кто перенес операцию тощего шунтирования [25], лечение тяжелого ожирения. Молочная кислота существует в природе в двух изомерных формах: L-молочная кислота и D-молочная кислота.
У человека лактат получают из L-формы, но некоторые виды бактерий могут продуцировать D-форму.В вышеупомянутой группе пациентов мальабсорбция углеводов может привести к аномальному увеличению в кишечнике видов бактерий, продуцирующих D-лактат. D-молочная кислота попадает в кишечник, всасывается и накапливается в крови.
Восприимчивые пациенты страдают эпизодами D-лактоацидоза обычно после приема пищи с высоким содержанием углеводов. Поскольку обычные методы измерения лактата обнаруживают только L-изомер, лактат в крови является ложно нормальным, и единственный биохимический ключ к этому состоянию — необъяснимый ацидоз с высоким анионным промежутком.
Клиническое значение гиперлактатемии
Клинические признаки
Гиперлактатемия от легкой до умеренной (лактат в крови
Прогностическая ценность измерения лактата в отделениях интенсивной терапии
Традиционное использование измерения лактата в качестве маркера недостаточной перфузии тканей и гипоксии тканей в отделениях интенсивной терапии в некоторой степени ограничивается растущим осознанием за последнее десятилетие того, что жертвы травм и другие потенциально могут пострадать. при критическом заболевании возможно повышение уровня лактата, несмотря на адекватную перфузию тканей.
Несмотря на это ограничение, измерение лактата имеет значение в отделении неотложной помощи и отделении интенсивной терапии, потому что, независимо от механизма гиперлактатемии, концентрация лактата в крови позволяет прогнозировать заболеваемость и смертность.
Прогностическая ценность измерения лактата подтверждена во многих группах пациентов.
Например, в проспективном исследовании 76 жертв серьезных травм серийные измерения лактата проводились в течение первых 48 часов после госпитализации [26].Все 27 пациентов, у которых уровень лактата нормализовался в течение 24 часов, выжили, но выжили только трое из 22 пациентов, у которых уровень лактата оставался повышенным через 48 часов.
В исследовании 1278 пациентов с инфекцией смертность составила 4,9% среди тех, чей лактат был ниже 2,5 ммоль / л при поступлении, по сравнению с 36% среди тех, у кого лактат был> 4 ммоль / л [27]. Наконец, раннее исследование 233 пациентов в критическом состоянии, страдающих различными формами шока, показало, что уровень смертности среди тех, у кого лактат был> 3, составил 67%.82 ммоль / л по сравнению с только 25% для тех, у кого был уровень лактата.
Эти и многие другие исследования продемонстрировали, что повышенный уровень лактата в контексте травм, сепсиса и критических заболеваний, как правило, является плохим прогностическим признаком, указывающим на необходимость немедленных и интенсивных реанимационных мероприятий. Если они эффективны в снижении уровня лактата в крови в течение 24-48 часов, шансы на выживание могут быть значительно увеличены [29].
Недавний комитет экспертов пришел к выводу, что есть убедительные доказательства того, что тестирование лактата в месте оказания медицинской помощи приводит к улучшению результатов для пациентов в различных учреждениях интенсивной терапии [30].
Требования к отбору проб для измерения лактата
Хотя некоторые органы рекомендуют артериальную кровь для измерения лактата, венозная кровь является подходящей альтернативой; результаты клинически значимо не различаются [31]. Следует избегать использования жгута во время сбора крови, поскольку это может вызвать ложное повышение лактата. Гепарин — подходящий антикоагулянт.
In vitro гликолиз и, следовательно, производство лактата продолжается после отбора пробы, так что концентрация лактата увеличивается на 30% всего за 30 минут при хранении при комнатной температуре.По этой причине кровь необходимо анализировать сразу же после взятия пробы. Если возникнет какая-либо задержка, образец необходимо хранить на льду, чтобы предотвратить продолжающийся гликолиз. Преаналитические ошибки, связанные с измерением лактата, являются предметом недавнего обзора [32].
Сводка
Лактат — нормальный продукт анаэробного гликолиза. Основное клиническое значение лактата заключается в том, что при тяжелом остром заболевании часто повышается анаэробный гликолиз — результат гипоксии тканей.Как следствие, увеличивается концентрация лактата в крови.
Клиническая ценность лактата как индикатора тканевой гипоксии снижается из-за того, что гиперлактатемия может возникать, несмотря на нормальную перфузию тканей и адекватную доставку кислорода, если, например, нарушены механизмы метаболизма / удаления лактата. Независимо от причины гиперлактатемия часто связана со снижением pH крови и, как следствие, с лактоацидозом.
Несмотря на отсутствие специфичности для тканевой гипоксии, лактат является ценным прогностическим маркером всех форм критических заболеваний и полезным диагностическим инструментом при обследовании пациентов с необъяснимым метаболическим ацидозом.
Физиология лактата в здоровье и болезнях | BJA Education
Ключевые точки
Концентрация лактата в крови отражает баланс между производством лактата и его клиренсом.
Гликолиз, глюконеогенез и превращение пирувата в лактат и из него связаны с NAD + и NADH.
Отказ окислительных механизмов может повлиять как на производство, так и на клиренс лактата.
Концентрация лактата> 5 ммоль литр -1 с тяжелым метаболическим ацидозом прогнозирует высокую смертность.
Нарушение клиренса лактата, а не гипоксическая тканевая продукция лактата, является причиной гиперлактемии у стабильных пациентов с сепсисом.
Нормальная концентрация лактата в плазме составляет 0,3–1,3 ммоль литр –1 . Когда-то считавшееся специальным исследованием, он все чаще измеряется автоматически с помощью анализа газов крови. Концентрации в плазме представляют собой баланс между производством лактата и метаболизмом лактата. У людей лактат присутствует в левовращающей изоформе.
Нормальное производство лактата
При гликолизе в цитоплазме образуется промежуточный метаболит пируват (рис. 1). В аэробных условиях пируват превращается в ацетил-КоА и входит в цикл Креба. В анаэробных условиях пируват превращается лактатдегидрогеназой (ЛДГ) в молочную кислоту. В водных растворах молочная кислота почти полностью диссоциирует до лактата и H + (pKa при 7,4 = 3,9) (рис. 2). Следовательно, термины «молочная кислота» и «лактат» в некоторой степени взаимозаменяемы.Лактат забуферивается в плазме с помощью NaHCO 3 .
Рис. 1
Гликолиз, цикл Креба и окислительное фосфорилирование.
Рис. 1
Гликолиз, цикл Креба и окислительное фосфорилирование.
Рис. 2
Диссоциация молочной кислоты.
Рис. 2
Диссоциация молочной кислоты.
Тканевые источники продукции лактата включают эритроциты, перивенозные гепатоциты, скелетные миоциты и кожу.Продукция базального лактата составляет 0,8 ммоль кг −1 час −1 (1300 ммоль день −1 ).
Измерение лактата
Спектрофотометрические анализаторы измеряют лактат в депротеинизированной крови, используя ЛДГ для окисления лактата в присутствии никотинамидадениндинуклеотида (NAD + ) до пирувата. Свет при 340 нм используется для измерения образовавшегося дигидроникотинамидадениндинуклеотида (НАДН). Это связано с концентрацией лактата.В измерениях лактата, полученных с помощью газоанализаторов крови, используется модифицированная амперометрическая ячейка. В клетке содержится фермент лактатоксидаза, который производит перекись водорода из лактата. Пероксид водорода окисляется на платиновом аноде, образуя ток, пропорциональный концентрации лактата. Ток от второго электрода, который функционирует без фермента, вычитается из измерительного электрода, чтобы устранить помехи.
Показания амперометрической ячейки на 13% выше, чем у спектрофотометрического анализатора; корректировка гематокрита уменьшает эту разницу.1 In vitro гликолиз эритроцитов приводит к ложному повышению лактата цельной крови. Образцы, которые не подлежат немедленному анализу, следует стабилизировать. Этого можно достичь охлаждением, осаждением белка или добавлением гликолитических ингибиторов.
Лактат и лактоацидоз
Ионы водорода, высвобождающиеся при диссоциации молочной кислоты, могут использоваться в производстве АТФ путем окислительного фосфорилирования. Нарушение окислительных путей во время производства лактата приводит к чистому увеличению H + и возникновению ацидоза.(Окислительное фосфорилирование во время тяжелых физических упражнений предотвращает ацидоз, несмотря на массивное производство лактата.)
НАДН и НАД
+Гликолиз требует NAD + (рис. 1), частично полученного путем превращения пирувата в лактат. Поставка НАДН контролирует скорость превращения пирувата в лактат. Ткани, такие как сердце, которые необходимы для выработки большого количества АТФ, требуют преобразования пирувата в ацетил-КоА. Чтобы поддерживать низкий уровень НАДН, используются челноки, которые помогают транспортировать электроны через митохондриальную мембрану и окислять НАДН обратно до НАД + .Шаттл малат-аспартат является основным механизмом. Глицерин-фосфатный челнок играет второстепенную роль. Все вместе они известны как окс-фос-шаттл (рис. 3). Если скорость гликолиза повышается до точки, при которой окс-фос-шаттл перегружен, концентрация НАДН повышается и выработка лактата восстанавливает НАД + , повышая концентрацию лактата.
Рис. 3
Рис. 3
Нормальный метаболизм лактата
Печень удаляет 70% лактата.Поглощение включает как переносчик монокарбоксилата, так и менее эффективный процесс диффузии (важен при концентрации> 2 ммоль литр -1 ). В перипортальных гепатоцитах метаболизм включает процессы глюконеогенеза и, в меньшей степени, окисление до CO 2 и вода (рис. 4). Богатые митохондриями ткани, такие как скелетные и сердечные миоциты и клетки проксимальных канальцев, удаляют остаток лактата, превращая его в пируват. Для этого требуется NAD + , поставляемый шаттлом из окс-фосфора (рис.4). Менее 5% лактата выводится почками.
Рис. 4
Основные режимы удаления лактата из плазмы.
Рис. 4
Принципиальные режимы удаления лактата из плазмы.
Причины гиперлактемии
Повышение выработки лактата
Гиперлактемия (> 5 ммоль. -1 ) условно делится на тип А, при котором гипоксия ткани приводит к более быстрому образованию, чем удаление, и тип В, при котором явная гипоксия тканей не играет роли.2 Тип B был далее подразделен в зависимости от того, вызван ли он основным заболеванием (B1), лекарствами и токсинами (B2) или врожденными ошибками метаболизма (B3) .3 Эта классификация имеет тенденцию чрезмерно упрощать часто многофакторную ситуация во время тяжелой болезни. Кроме того, это бесполезно функционально (Таблица 1).
Таблица 1Причины гиперлактемии рассматриваются с точки зрения увеличения продукции и уменьшения клиренса. * Нет никаких доказательств того, что гипоксия является стимулом производства лактата во время энергичных упражнений
| . | Примеры . | Тип . |
|---|---|---|
| Повышенная продукция | ||
| Повышенная скорость гликолиза | ||
| Повышенный AMP — дисбаланс между спросом и предложением АТФ | Гипоксемия, анемия, гипоперфузия, шок, отравление CO | 9036 Тяжелые физические нагрузкиA |
| Катехоламины | Феохромоцитома | B1 |
| Сальбутамол, инфузия эпинефрина | B2 | 903 Инфузия 9036 В2 903 Гликолиз 9011 9036 Нерегулируемый 9036 Субстрат пирувата|
| Отсутствие активности пируватдегидрогеназы | Дефицит тиамина | B3 |
| Врожденная аномалия пируватдегидрогеназы | B3 | Ингибирование эндотоксином | B2 |
| Образование аланина | Критическое заболевание | B2 |
| Злокачественные новообразования | B2 | |
| Цианидная токсичность | B2 | |
| Сниженный клиренс | ||
| Печеночный метаболизм | ||
| Нарушение окислительного метаболизма | Нарушение цианового кровотока в печени 123, ферментные дефекты B30 | |
| Нарушение глюконеогенеза | Бигуаниды, алкогольная интоксикация, диабет | B1, B1, B2 |
| Митохондриальный тканевый метаболизм | Гипоксемия, анемия, региональная гипоперфузия A, шок | |
| Дефекты ферментов, цианидная токсичность | B3, B1 | |
| Почечная экскреция | Почечная экскреция обычно составляет <5% клиренса лактата.Эта фракция может увеличиваться при гиперлактаемии | |
| . | Примеры . | Тип . |
|---|---|---|
| Повышенная продукция | ||
| Повышенная скорость гликолиза | ||
| Повышенный AMP — дисбаланс между спросом и предложением АТФ | Гипоксемия, анемия, гипоперфузия, шок, отравление CO | 9036 Тяжелые физические нагрузкиA |
| Катехоламины | Феохромоцитома | B1 |
| Сальбутамол, инфузия эпинефрина | B2 | 903 Инфузия 9036 В2 903 Гликолиз 9011 9036 Нерегулируемый 9036 Субстрат пирувата|
| Отсутствие активности пируватдегидрогеназы | Дефицит тиамина | B3 |
| Врожденная аномалия пируватдегидрогеназы | B3 | Ингибирование эндотоксином | B2 |
| Образование аланина | Критическое заболевание | B2 |
| Злокачественные новообразования | B2 | |
| Цианидная токсичность | B2 | |
| Сниженный клиренс | ||
| Печеночный метаболизм | ||
| Нарушение окислительного метаболизма | Нарушение цианового кровотока в печени 123, ферментные дефекты B30 | |
| Нарушение глюконеогенеза | Бигуаниды, алкогольная интоксикация, диабет | B1, B1, B2 |
| Митохондриальный тканевый метаболизм | Гипоксемия, анемия, региональная гипоперфузия A, шок | |
| Дефекты ферментов, цианидная токсичность | B3, B1 | |
| Почечная экскреция | Почечная экскреция обычно составляет <5% клиренса лактата.Эта фракция может повышаться во время гиперлактемии. | |
Причины гиперлактемии рассматриваются с точки зрения увеличения продукции и снижения клиренса. * Нет никаких доказательств того, что гипоксия является стимулом производства лактата во время энергичных упражнений
| . | Примеры . | Тип . |
|---|---|---|
| Повышенная продукция | ||
| Повышенная скорость гликолиза | ||
| Повышенный AMP — дисбаланс между спросом и предложением АТФ | Гипоксемия, анемия, гипоперфузия, шок, отравление CO | 9036 Тяжелые физические нагрузкиA |
| Катехоламины | Феохромоцитома | B1 |
| Сальбутамол, инфузия эпинефрина | B2 | 903 Инфузия 9036 В2 903 Гликолиз 9011 9036 Нерегулируемый 9036 Субстрат пирувата|
| Отсутствие активности пируватдегидрогеназы | Дефицит тиамина | B3 |
| Врожденная аномалия пируватдегидрогеназы | B3 | Ингибирование эндотоксином | B2 |
| Образование аланина | Критическое заболевание | B2 |
| Злокачественные новообразования | B2 | |
| Цианидная токсичность | B2 | |
| Сниженный клиренс | ||
| Печеночный метаболизм | ||
| Нарушение окислительного метаболизма | Нарушение цианового кровотока в печени 123, ферментные дефекты B30 | |
| Нарушение глюконеогенеза | Бигуаниды, алкогольная интоксикация, диабет | B1, B1, B2 |
| Митохондриальный тканевый метаболизм | Гипоксемия, анемия, региональная гипоперфузия A, шок | |
| Дефекты ферментов, цианидная токсичность | B3, B1 | |
| Почечная экскреция | Почечная экскреция обычно составляет <5% клиренса лактата.Эта фракция может увеличиваться при гиперлактаемии | |
| . | Примеры . | Тип . |
|---|---|---|
| Повышенная продукция | ||
| Повышенная скорость гликолиза | ||
| Повышенный AMP — дисбаланс между спросом и предложением АТФ | Гипоксемия, анемия, гипоперфузия, шок, отравление CO | 9036 Тяжелые физические нагрузкиA |
| Катехоламины | Феохромоцитома | B1 |
| Сальбутамол, инфузия эпинефрина | B2 | 903 Инфузия 9036 В2 903 Гликолиз 9011 9036 Нерегулируемый 9036 Субстрат пирувата|
| Отсутствие активности пируватдегидрогеназы | Дефицит тиамина | B3 |
| Врожденная аномалия пируватдегидрогеназы | B3 | Ингибирование эндотоксином | B2 |
| Образование аланина | Критическое заболевание | B2 |
| Злокачественные новообразования | B2 | |
| Цианидная токсичность | B2 | |
| Сниженный клиренс | ||
| Печеночный метаболизм | ||
| Нарушение окислительного метаболизма | Нарушение цианового кровотока в печени 123, ферментные дефекты B30 | |
| Нарушение глюконеогенеза | Бигуаниды, алкогольная интоксикация, диабет | B1, B1, B2 |
| Митохондриальный тканевый метаболизм | Гипоксемия, анемия, региональная гипоперфузия A, шок | |
| Дефекты ферментов, цианидная токсичность | B3, B1 | |
| Почечная экскреция | Почечная экскреция обычно составляет <5% клиренса лактата.Эта фракция может повышаться при гиперлактаемии | |
Повышенный гликолиз
Для поддержки увеличения гликолиза требуется NAD + от превращения пирувата в лактат. Активность фосфофруктокиназы (PFK) ограничивает скорость. Падение АТФ после, например, гипоксемии, анемии, гипоперфузии, тяжелых физических нагрузок и отравления угарным газом — все служит для стимуляции ПФК по мере повышения АМФ. Кроме того, как эндогенная секреция, так и экзогенно вводимые катехоламины также стимулируют гликолиз.
При тяжелых физических нагрузках миоциты типа II производят большое количество лактата (концентрация может возрасти до 25 ммоль / л –1 без каких-либо долгосрочных последствий; см. Выше). Это обеспечивает некоторые повышенные потребности сердца в энергии (рис. 4). После тяжелых упражнений и во время легкой «разминки» мышечные волокна типа I обеспечивают повышенную долю метаболизма лактата.
Нерегулируемый гликолиз, вызванный режимами парентерального кормления, содержащими фруктозу, в настоящее время представляет исторический интерес.
Ошибки обмена веществ
Активность пируватдегидрогеназы (рис. 1) нарушается из-за врожденных нарушений метаболизма, дефицита тиамина и эндотоксина. Катаболизм белков, возникающий в результате тяжелого заболевания или злокачественного новообразования, приводит к образованию аланина, который превращается в пируват. Любые дефекты цикла Креба или цепи переноса электронов вызывают накопление пирувата.
Пониженный клиренс лактата в печени
Печень получает 25% сердечного выброса.Печеночная воротная вена обеспечивает 75% кровотока печени и 50–60% ее кислорода. Изменения печеночного кровотока и снабжения печенью кислородом, а также собственное заболевание печени влияют на способность печени метаболизировать лактат.
Только когда кровоток в печени снижается до 25% от нормы, происходит снижение клиренса лактата. При тяжелом шоке поглощение лактата переносчиком монокарбоксилата становится насыщенным, развитие внутриклеточного ацидоза подавляет глюконеогенез, а снижение кровотока печени доставляет меньше лактата для метаболизма.В анаэробных условиях гликолиз становится преобладающим способом производства энергии печенью. Таким образом, печень становится органом, вырабатывающим лактат, а не использующим лактат для глюконеогенеза (рис. 4).
Пероральные гипогликемические препараты
Глюконеогенез поставляет NAD + , необходимый для преобразования лактата в пируват (рис. 4). Пероральные гипогликемические препараты на основе бигуанидов подавляют глюконеогенез в печени и почек (хотя метформин, по-видимому, влияет на метаболизм лактата только при нарушении функции почек).Метформин противопоказан при почечной и печеночной недостаточности. Поставка NAD + уязвима для требований других ферментных систем, таких как алкогольдегидрогеназа. Это становится значительным при активации отравлением этанолом. Глюконеогенез нарушается при диабете I типа.
Решение Хартмана
Сильная разница ионов в растворе Хартмана составляет 28 мэкв. -1 , что ближе к нормальному значению 40-42 мэкв. -1 , чем физиологический раствор 0.9%, где SID равен нулю. Таким образом, раствор Хартмана вызывает меньший гиперхлоремический ацидоз, чем солевой раствор 0,9%. Лактат (29 ммоль литр -1 ) будет действовать как сильный ион и может временно вызвать ацидоз, пока он не метаболизируется в печени.5
Сепсис
Хотя избыточное производство лактата фагоцитарными клетками в ответ на эндотоксин или травму тканей является причиной некоторого повышения лактата при септических состояниях, также происходит снижение экстракции и утилизации лактата в печени.
Хроническая болезнь
Снижение способности хронически больной печени обрабатывать лактат становится очевидным, когда увеличивается периферическая продукция или происходит дальнейшее повреждение печени.
Снижение внепеченочного метаболизма
Ткани, богатые митохондриями, не могут метаболизировать лактат, если их снабжение кислородом прекращается или если есть внутренние аномалии окислительных путей. В таких условиях, как и печень, они будут вырабатывать лактат, а не потреблять ткани.
Пониженная почечная экскреция
Почки обрабатывают лактат путем выделения, глюконеогенеза и окисления. Поскольку почечный порог составляет 6–10 ммоль / л –1 , почечная экскреция значима только при гиперлактаемии.
Лактат и критическое заболевание
Концентрация лактата в крови> 5 ммоль / л -1 у пациентов с тяжелым ацидозом при pH <7,35 или дефиците оснований более 6 летальность составляет 80% .6
Остановка сердца и реанимация
Гипоксия всего тела, возникающая при остановке сердца или тяжелой гиповолемии, запускает анаэробный метаболизм.Концентрация лактата напрямую отражает клеточную гипоксию. Следовательно, во время остановки сердца в стационаре и через 1 час после восстановления спонтанного кровообращения концентрация лактата позволяет прогнозировать выживаемость7
Сепсис
При синдроме системной воспалительной реакции (SIRS) или раннем сепсисе гиперлактемия может отражать гипоксию тканей. Раннее усиление доставки кислорода улучшает исход.8 Интерпретация концентрации лактата у пациентов с установленным сепсисом затруднена.У стабильных пациентов с сепсисом повышенная доставка кислорода, а уровни кислорода в тканях обычно превышают те, которые вызывают анаэробный метаболизм. Нарушение клиренса лактата обычно более значимо, чем увеличение продуктивности. Производство аэробного лактата у таких пациентов может быть вовлечено в модуляцию углеводного обмена при стрессе.9 Дихлорацетат усиливает активность пируватдегидрогеназы и снижает концентрацию лактата в крови у пациентов с сепсисом, но не влияет на гемодинамику или выживаемость.10
Инфаркт кишечника
Гипоксия кишечника вызывает анаэробный метаболизм. Печень получает больше лактата из воротной вены. Первоначально он окисляется или превращается в глюкозу перипортальными гепатоцитами. Бактериальная транслокация и глубокий сдвиг жидкости способствуют коллапсу кровообращения. Падение глобальной доставки кислорода. Высвобождение эндогенного катехоламина пытается поддержать кровообращение, но также увеличивает гликолиз и образование лактата. По мере развития шока кровоток в печени падает, и внутриклеточный ацидоз подавляет глюконеогенез из лактата.Печень скорее производит, чем очищает лактат. Кишечные бактерии метаболизируют глюкозу и углеводы до d-лактата. Он медленно метаболизируется человеческим ЛДГ и способствует нарастанию лактоацидоза.
Список литературы
1,,.Оценка биосенсора для измерения лактата в цельной крови
,Clin Biochem
,1999
, vol.32
(стр.109
—12
) 2,. ,.Клиническая картина и классификация лактоацидоза
,Клинические и биохимические аспекты молочного ацидоза
,1976
Oxford
Blackwell Scientific
(стр.1
—200
) 3.Уровни лактата в крови
,Curr Opin Crit Care
,1999
, vol.5
(стр.234
—9
) 4,.Лактоацидоз при сепсисе: комментарий
,Intensive Care Med
,1996
, vol.22
(стр.6
—16
) 5.Физиология кислотных оснований в эпоху после Коперника
,Curr Opin Crit Care
,1999
, vol.5
(стр.429
—35
) 6« и др.для группы изучения DCA-лактоацидоза: естественная история и течение приобретенного лактоацидоза у взрослых
,Am J Med
,1994
, vol.97
(стр.47
—54
) 7,,,.Кислотно-основные факторы выживаемости после сердечно-легочной реанимации
,Crit Care Med
,1985
, vol.13
(стр.888
—92
) 8« и др.Ранняя целенаправленная терапия в лечении тяжелого сепсиса, септического шока
,N Engl J Med
,2001
, vol.345
(стр.1368
—77
) 9,.Патогенез лактоацидоза при сепсисе
,Curr Opin Crit Care
,1999
, vol.5
(стр.452
—7
) 10,,, et al.Контролируемое клиническое испытание дихлорацетата для лечения лактоацидоза у взрослых
,N Engl J Med
,1992
, vol.327
(стр.1564
—9
)Повышение квалификации в области анестезии, интенсивной терапии и боли | Том 6, номер 3, 2006 г. © Правление и попечители Британского журнала анестезии [2006]. Все права защищены. Для получения разрешений обращайтесь по электронной почте: [email protected]
.Набор проблем метаболизма
Набор проблем метаболизмаНабор проблем с метаболизмомЗадача 7: Соотношение пируват / лактатПравильно!Объясните, почему в анаэробных клетках соотношение пируват / лактат намного меньше 1, в то время как в аэробных условиях соотношение пируват / лактат намного больше 1. A. Лактат производится из пирувата только в анаэробных условиях.Гликолитический путь продуцирует пируват, который в присутствии кислорода далее метаболизируется в цикле лимонной кислоты с образованием НАДН и ФАДН 2 для окислительного фосфорилирования в митохондриях. Обычно в этих условиях уровень молочной кислоты будет низким. В отсутствие кислорода (анаэробный) пируват должен быть преобразован в молочную кислоту, единственная реакция, которая может регенерировать NAD + , обеспечивая дальнейший гликолиз.Производство молочной кислоты только в анаэробных условиях объясняет, почему пируват / лактат намного меньше единицы в анаэробных клетках и намного больше единицы в аэробных клетках. |
Биологический проект
Университет Аризоны
Вторник, 20 августа 1996 г.
Связаться с командой разработчиков
http: // www.biology.arizona.edu
Все права защищены © 1996. Все права защищены.
Лактат как точка опоры метаболизма
Abstract
Ошибочно считается следствием нехватки кислорода в сокращающихся скелетных мышцах, теперь мы знаем, что L-энантиомер лактат-аниона образуется в полностью аэробных условиях и постоянно используется в различных клетках. , ткани, органы и на уровне всего тела. Перемещаясь между клетками-продуцентами (драйверами) и потребителями (реципиентами), лактат выполняет по крайней мере три цели: 1] является основным источником энергии для дыхания митохондрий; 2] основной глюконеогенный предшественник; и 3] сигнальная молекула.Работая за счет массового воздействия, окислительно-восстановительной регуляции клеток, аллостерического связывания и перепрограммирования хроматина путем лактилирования остатков лизина на гистонах, лактат оказывает большое влияние на распределение энергетического субстрата. Физиологический диапазон тканевого [лактата] составляет 0,5–20 мМ, а клеточное соотношение лактат / пируват (L / P) может колебаться от 10 до> 500; эти изменения во время упражнений и другие реакции стресс-напряжение затмевают другие метаболические сигналы по величине и продолжительности. Следовательно, динамика лактата оказывает быстрое и значительное краткосрочное и долгосрочное воздействие на окислительно-восстановительный потенциал клеток и другие системы контроля.Ингибируя липолиз жировой ткани через HCAR-1 и поглощение жирных кислот мышечными митохондриями через малонил-КоА и CPT1, лактат контролирует распределение энергетического субстрата. Повторяющееся воздействие лактата при регулярных физических упражнениях приводит к значительному влиянию на экспрессию регуляторных ферментов гликолиза и митохондриального дыхания. Лактат является центром регуляции метаболизма in vivo .
Ключевые слова
Гликолиз
Окислительный метаболизм
Аэробный
Анаэробный
Митохондриальный биогенез
Упражнение
Глюконеогенез
Активация клеточного субстрата
Энергетический субстрат
Энергетический субстрат
1αHCAR1
Лактилирование гистонов
TGFβ
Рекомендуемые статьи Цитирующие статьи (0)
Просмотреть аннотацию© 2020 Опубликовано Elsevier B.V.
Рекомендуемые статьи
Цитирующие статьи
Производство лактата и метаболический ацидоз, вызванный физической нагрузкой: виновен или невиновен?
В редакцию:
В прекрасной и очень интересной главе, посвященной тестированию с физической нагрузкой, опубликованной в Европейской респираторной монографии по тестированию функции легких , Рока и Рабинович 1 написали следующее. «Повышенная выработка лактата ответственна за падение мышечного pH, что, в свою очередь, может играть роль в определении непереносимости физических упражнений у этих пациентов (пациенты с ХОБЛ).Преждевременный лактоацидоз во время физических упражнений у пациентов с ХОБЛ был связан со снижением концентрации окислительных ферментов в мышцах нижних конечностей ».
Мы хотели бы подчеркнуть, что широко распространенное мнение о том, что молочная кислота вырабатывается в работающих мышцах в результате кислородной недостаточности, и что она непосредственно вызывает метаболический ацидоз, вызванный физической нагрузкой, подвергается критике. Кроме того, многочисленные данные о различных видах не согласуются с преобладающей теорией 2.
Мы все согласны с тем, что, глядя на конечный результат метаболизма во время интенсивных упражнений, наблюдаемый метаболический ацидоз совпадает с накоплением лактата, но означает ли это, что производство лактата виновно?
Недавно, объединив большую серию статей, Robergs et al .3 представили убедительные эмпирические наблюдения, что лактат является следствием, а не причиной клеточных событий, вызывающих ацидоз.
В результате превращения молекулы глюкозы в две молекулы пирувата три реакции высвобождают четыре протона, один из которых управляется пируваткиназой и потребляет два протона. Преобразование двух молекул пирувата в две молекулы лактата лактатдегидрогеназой (ЛДГ) потребляет два протона. Другой источник протонов — гидролиз аденозинтрифосфата (АТФ).
Во время упражнений высокой интенсивности, как подчеркнули Robergs et al. 3, наблюдается возрастающая зависимость от АТФ, поставляемого гликолизом. В этих условиях происходит более высокая скорость высвобождения цитозольных протонов в результате гликолиза и гидролиза АТФ. Буферная способность клеток может быть превышена, и может развиться ацидоз. Вследствие благоприятной биоэнергетики для реакции ЛДГ увеличивается выработка лактата. Производство лактата, по-видимому, не вызывает ацидоз и, кроме того, играет роль «приемника» протонов, образующихся во время катаболизма и гидролиза АТФ, тем самым уменьшая ацидоз.
В заключение, из-за появления «изо-времени» лактата и метаболического ацидоза остается, что для клинического применения накопление лактата, очевидно, является хорошим косвенным маркером клеточного метаболического ацидоза.
Что такое лактатный и лактатный порог
Лактатный порог — это термин, используемый в течение многих лет во всех видах спорта, и это один из наиболее часто используемых показателей в мире тренировок спортсменами и тренерами во всем мире.
Однако действительно ли мы знаем, что такое лактатный порог? Знаем ли мы, что такое лактат или его роль в работе и метаболизме? Дело в том, что до сих пор существует много путаницы в отношении лактата и того, что представляет собой лактатный порог.
Ранние исследования лактата
Лактат практически неизвестен в метаболизме человека, несмотря на его ключевую роль в его регуляции. В течение многих лет считалось, что лактат — это просто отходы в результате анаэробных упражнений. В какой-то момент даже считалось, что он кристаллизовался после упражнений, что привело к болезненным ощущениям в мышцах (что, как мы теперь знаем, не соответствует действительности).
Но загадка, окружающая лактат, возникла не из-за отсутствия научных исследований. Исследования лактата датируются 19 веком, когда лауреат Нобелевской премии Луи Пастер предположил, что лактат вырабатывается из-за недостатка кислорода во время сокращения мышц.Другой лауреат Нобелевской премии Отто Мейерхоф предположил, что гликоген является предшественником лактата. Он также заметил, что сокращение мышц вызывает лактат и потерю возбудимости. В 1923 году другой лауреат Нобелевской премии, А.В. Хилл и его коллега Луптон описали термин «долг O2» и связали его с анаэробным производством лактата.
Однако только в конце 20-го века мы начали по-настоящему понимать роль лактата в физических упражнениях и метаболизме. Доктор Джордж Брукс, специалист по метаболизму из Калифорнийского университета в Беркли, тщательно изучал лактат более 40 лет.Большая часть того, что мы знаем о лактате, — благодаря его работе.
Что мы знаем о лактате сейчас
Теперь мы знаем, что образование лактата может происходить в аэробных условиях, и что производство лактата является результатом использования глюкозы мышечными клетками в аэробных условиях.
Из работы Брукса мы также знаем, что лактат не является побочным продуктом. Фактически, это самый важный глюконеогенный предшественник (новый генератор глюкозы) в организме. Около 30 процентов всей глюкозы, которую мы используем во время упражнений, получается за счет «рециркуляции» лактата в глюкозу.
Метаболизм
Лактат также является ключевым регулятором промежуточного метаболизма, регулирующим использование субстрата. Он снижает и подавляет расщепление жира для получения энергии (липолиз), а также скорость использования глюкозы клетками (глюколиз).
Когнитивные функции
Вы не поверите, но лактат имеет решающее значение даже для мозга, поскольку он является основным топливом, которое используют нейроны. Лактат на самом деле необходим для долговременной памяти и даже может быть задействован в понимании болезни Альцгеймера.(Некоторые исследования показывают, что когда поглощение лактата нейронами подавляется, долговременная память подавляется).
Болезнь
Лактат также может быть вовлечен в некоторые хронические метаболические заболевания, такие как диабет 2 типа. Уровень лактата в крови у этой популяции в 2-3 раза выше, чем у здорового физически активного населения. Раковые клетки имеют нарушенный метаболизм, используя слишком много глюкозы аэробно (эффект Варбурга) и вырабатывая большое количество лактата, который может способствовать росту и прогрессированию опухоли.
Очевидно, что лактат — это не просто отходы анаэробных упражнений. Это основное топливо и ключевой регулятор метаболизма. Это также возможный эпицентр различных хронических заболеваний.
Лактат и производительность
Лактат является побочным продуктом утилизации глюкозы мышечными клетками. Чем выше поток глюкозы в клетку, тем выше производство лактата независимо от наличия кислорода. Во время упражнений высокой интенсивности мышечные волокна типа II-Fast Twitch полностью задействуются из-за высокой сократительной потребности скелетных мышц для производства энергии (АТФ).Мышечные волокна типа II очень гликолитичны (они используют много глюкозы), что приводит к выработке большого количества лактата. Это производство является естественным побочным продуктом использования глюкозы клетками скелетных мышц.
Во время интенсивных упражнений выработка лактата во много раз выше, чем в состоянии покоя. Высвобождение ионов водорода (H +), связанных с лактатом, может вызвать значительное снижение pH сократительной мышцы, что приводит к ацидозу. Это чрезмерное накопление H +, не только из-за лактата, но также из-за распада АТФ для сокращения мышц (гидролиз АТФ), может мешать сокращению мышц в разных местах.
Например, он может конкурировать с кальцием (Ca ++) за сайт связывания тропонина С (белок, участвующий в регуляции сокращения мышц). H + может также ингибировать высвобождение и повторное поглощение кальция из саркоплазматического ретикулума. Оба процесса участвуют в сокращении мышц. Все это может привести к снижению способности сокращения мышц, что может привести к значительному снижению пиковой силы сокращений, снижению максимальной скорости сокращения мышц и производительности.
Мы очень хорошо знаем, что чем выше соревновательный и тренировочный уровень спортсмена, тем меньше наблюдается накопление лактата в крови.В таблице 1 мы можем наблюдать уровни лактата в крови различных категорий езды на велосипеде при разной интенсивности упражнений (ватт / кг), которые я собирал за годы во время физиологических тестов. Мы ясно видим, что чем выше соревновательный уровень велосипедиста, тем ниже уровень лактата в крови и тем выше выходная мощность и производительность.
| Рабочая нагрузка | Юный велосипедист | Лучшие любители | Ср. Pro-Tour | Мировой класс |
| Вт / кг | Кровь La (ммоль / л) | Кровь La (ммоль / л) | Кровь La (ммоль / л) | Кровь La (ммоль / л) |
| 3 | 1.3 | 1,1 | 1,1 | 0,8 |
| 3,5 | 1,8 | 1,3 | 1,2 | 0,8 |
| 4 | 3 | 2,3 | 2 | 0,96 |
| 4,5 | 6,6 | 3,5 | 3,2 | 1,8 |
| 5 | 10 | 7,6 | 5,8 | 3,1 |
| 5,5 | 9.2 | 8,2 | 5,2 | |
| 6 | 8,9 |
Таблица 1. Различия в уровнях лактата в крови (ммоль / л) у соревнующихся велосипедистов разного уровня подготовки. Таблица изменена из San Millán et al, 2009
Этот более низкий уровень лактата в крови, наблюдаемый у ведущих спортсменов, связан с повышенной способностью выведения лактата. Лактат может быть экспортирован в кровь для очистки и получения энергии практически в каждом органе тела.Однако этот процесс занимает время (минуты), в то время как лактат вырабатывается непрерывно во время тренировки.
Хорошо тренированные спортсмены очень эффективны и выводят меньше лактата в кровь, поскольку они выводят его в больших количествах прямо в мышцу, вырабатывающую лактат, что занимает секунды или миллисекунды. Это очень выгодно, так как позволяет сократительным мышцам быстрее удалять H +, а также быстрее «рециркулировать» лактат для получения дополнительной энергии (АТФ).
Во время упражнений лактат в основном вырабатывается в быстро сокращающихся мышечных волокнах, которые используют много глюкозы для получения энергии.Он очищается в основном за счет медленно сокращающихся мышечных волокон. Это сложный процесс, в котором задействованы различные транспортеры и ферменты, специфичные для лактата. Быстро сокращающиеся волокна содержат большое количество одного переносчика, называемого МСТ-4 (монокарбоксилат-4), который переносит лактат от этих волокон. Медленно сокращающиеся волокна обладают транспортером под названием MCT-1, который забирает лактат внутрь этих волокон. Затем этот лактат превращается в пируват в митохондриях с помощью фермента, называемого mLDH (митохондриальная лактатдегидрогеназа), чтобы затем окончательно синтезировать АТФ (энергию).
Тренировка на выносливость (зона 2) направлена на улучшение способности клиренса лактата за счет увеличения количества митохондрий, очищающих лактат, в основном в медленно сокращающихся мышечных волокнах, а также за счет увеличения количества MCT-1 и mLDH. Как высокоинтенсивные тренировки, так и тренировки на выносливость увеличивают количество MCT-4, чтобы увеличить транспорт лактата от быстро сокращающихся волокон.
Как показано в таблице 1, лактат, вероятно, является параметром, который больше всего различает разные уровни спортивных результатов.Анализ лактата может дать нам много информации о метаболизме мышц во время упражнений, где мы можем косвенно оценить плотность митохондрий, окислительный статус и статус использования субстрата или характер набора мышечных волокон.
Тест на лактат, вероятно, лучший способ оценить метаболический стресс и работоспособность мышц, особенно у спортсменов на выносливость. Это также, вероятно, лучший метод для прогнозирования результатов в соревнованиях на выносливость, а также отличный параметр для определения индивидуальных тренировочных зон для спортсменов.Среди этих тренировочных зон «лактатный порог» — это специальная тренировочная зона, которую мы все хотим тренировать и улучшать. Однако единственный способ напрямую измерить лактатный порог — это провести тестирование на лактат.
Что такое порог лактата?
Лактатный порог — вероятно, наиболее часто используемый тренировочный термин тренерами и спортсменами во всем мире. Тем не менее, существуют большие разногласия относительно того, что на самом деле означает лактатный порог, а также относительно того, какая интенсивность упражнений вызывает его. Лактатный порог обычно известен как интенсивность упражнений или концентрация лактата в крови, при которой мы можем выдерживать нагрузку высокой интенсивности только в течение определенного периода времени.Однако именно здесь ведутся споры: что это за период времени? Какова эта концентрация лактата в крови? Как долго мы сможем выдерживать заданную интенсивность упражнений, прежде чем начнем действовать?
Многие авторы и тренеры уже очень давно пытаются ответить на эти вопросы. Первое описание порога лактата в крови датируется 1930 годом и было названо У. Хардингом Оулзом «Оулс-Пойнт». В 1964 году Васерман и Макилрой предложили термин «анаэробный порог», основываясь на убеждении, что накопление лактата происходит из-за недостатка мышечного кислорода и, следовательно, анаэробный метаболизм мышц необходим для продолжения сокращения мышц.Мадер и его сотрудники в 1976 году определили, что «анаэробный порог» достигается при концентрации лактата в крови 4 ммоль / л (миллимоль на литр), что в 1981 году было названо Шёдином и Якобсом «начало накопления лактата в крови» (OBLA). также при концентрации лактата в крови 4 ммоль / л. Фаррел и соавторы предложили в 1979 году термин «начало накопления лактата в плазме» (OPLA), который обозначал интенсивность упражнений, при которой концентрация лактата в крови на 1 ммоль / л превышала исходную.Другим термином, предложенным в 1981 году Лафонтеном и сотрудниками, было «максимальное устойчивое состояние», которое теоретически происходит при концентрации лактата в крови 2,2 ммоль / л. В 1983 году Койл и его сотрудники предложили термин «порог лактата», который представлял собой нелинейное увеличение лактата в крови по крайней мере на 1 ммоль / л. Другой термин, «максимальная стационарная рабочая нагрузка» (MSSW), был предложен Borch и соавторами в 1993 году и был установлен на фиксированном уровне [La-] 3 ммоль / л. Вероник Биллат в 2003 году предложила термин «максимальное установившееся состояние лактата» (MLSS), поскольку интенсивность упражнений на уровне одного лактата в крови может быть устойчивой.
Непонятно, не правда ли? В научном сообществе существует множество теорий и гипотез, но нет единого мнения о том, что такое «лактатный порог». Суть в том, чтобы понять, что означает порог лактата, заключается в том, что по мере того, как мышцы подвергаются более метаболическому стрессу, происходит более высокое накопление лактата и H +. Митохондрии в сократительных мышцах становятся более напряженными, чтобы своевременно очищать лактат, и в какой-то момент, если интенсивность упражнений продолжается, митохондрии сократительных мышц становятся насыщенными и, следовательно, не могут справиться с клиренсом лактата, а затем экспортируют его в кровь, и именно тогда мы наблюдайте повышение уровня лактата в крови, которое соответствует метаболическому событию, когда невозможно поддерживать заданную интенсивность упражнений.
На мой взгляд, важно взглянуть на концепцию лактатного порога под другим углом. Во-первых, к сожалению, многие спортсмены и тренеры не проводят тестирование на лактат, поэтому они никогда не могут узнать о своем метаболизме лактата, несмотря на то, что все еще говорят о тренировках с лактатным порогом.
«Многие спортсмены и тренеры не проводят тестирование на лактат, поэтому они никогда не могут узнать о своем метаболизме лактата, несмотря на то, что они все еще говорят о тренировках с лактатным порогом.”
Кроме того, мы склонны описывать усилия по достижению порога лактата как те высокие нагрузки, которые мы можем выдерживать в течение относительно коротких периодов времени без «взрыва», и здесь возникает большая путаница. Где мы определяем интенсивность упражнений и период времени, когда мы можем выдержать большие усилия? Это 5, 10, 30 или 300 минут? Концентрация лактата в крови составляет 3, 4 или 6 ммоль / л? Восхождение на 5-километровый подъем по кат-1 в течение 25 минут без падения требует определенного «лактатного порога» / максимального устойчивого состояния, которое может представлять концентрацию лактата в крови 4-6 ммоль / л и конкретную индивидуальную выходную мощность (или дробную пороговую мощность / FTP. ).Однако эта интенсивность отличается от 10-километрового подъема по кат-2 без падения, что может занять 40 минут и, следовательно, другой порог / максимальное устойчивое состояние, которое может представлять концентрацию лактата в крови 3-5 ммоль / л и другой FTP, который в то же время отличается от порогового значения или максимального устойчивого состояния 40 км TT. Бежать марафон с заданным темпом требует очень важных усилий по поддержанию максимального устойчивого состояния, которое на самом деле является истинным порогом лактата для всего марафона, при котором концентрация лактата в крови составляет ~ 2–2.5 ммоль / л. Этот порог отличается и вызывает более высокую концентрацию лактата в крови при беге на ½ марафона, 10 км или 5 км. Кажется, что каждый вид спорта на выносливость имеет разные «пороги лактата», которые являются ключевыми для успешных тренировок.
Развитие порога лактата
Все это кажется слишком запутанным, и по этой причине я считаю, что пора развить концепцию лактатного порога более прагматично. Возможно, нам придется рассмотреть различные термины, такие как, например, концепция максимального метаболического стресса, который может поддерживаться в течение определенного времени («максимальное метаболическое устойчивое состояние» / MMSS).В зависимости от вида спорта и события будут разные MMSS, которые будут отражать максимальный метаболический стресс, который мы можем выдержать на определенных дистанциях и дисциплинах, таких как марафон, 1500 м, бег на 10 км, 40 км TT или 5-километровое восхождение по кат-1. Затем мы можем преобразовать этот MMSS в концентрацию лактата в крови, чтобы получить наш лактатный порог, или в другие различные параметры, такие как частота сердечных сокращений, выходная мощность (FTP) или темп бега. Это не только полезный способ прогнозировать производительность, но и отслеживать прогресс.В некотором смысле это уже делается многими тренерами и спортсменами, которые постоянно используют FTP или целевой темп.
Заблуждение при обучении в отношении порога лактата
Типичная тренировочная ошибка, которую совершают многие спортсмены и тренеры, — это тренировка на «пороге лактата», чтобы улучшить способность выведения лактата. Это неверно, поскольку мы знаем, что во время упражнений лактат в основном вырабатывается гликолитическими волокнами (быстро сокращающиеся), которые задействуются на «пороге лактата». Однако лактат в основном очищается соседними медленными волокнами, которые обладают очень высокой митохондриальной емкостью и гораздо большим количеством ферментов mlDH и переносчиков MCT-1.Следовательно, для улучшения способности очищать лактат, хотя это совершенно противоречит здравому смыслу, это ключ к тренировке этих медленных мышечных волокон для стимуляции роста и функции митохондрий, а также для увеличения MCT-1 и mLDH. Тренировка на пороге лактата важна для улучшения гликолитических волокон и их механизмов (наш «Турбо») и для увеличения количества и функции гликолитических ферментов, а также для увеличения количества транспортеров MCT-4, необходимых для транспортировки лактата от быстро сокращающихся волокон. чтобы затем очиститься медленными сокращающимися волокнами.Тратить слишком много времени на порог лактата также очень сложно, так как это требует больших усилий и может привести к перетренированности, что мы постоянно наблюдаем в нашей лаборатории.
Мы постоянно видим в нашей лаборатории спортсменов и тренеров, которые имеют это заблуждение и совершают эту ошибку, приводящую к перетренированности и не улучшающей способность выведения лактата. С помощью специальных протоколов мы измеряем метаболизм лактата, жиров и углеводов во время всех интенсивностей упражнений, чтобы изучить весь метаболический и физиологический ответ на упражнения, что позволяет нам прогнозировать производительность, а также достаточно четко определять отдельные тренировочные зоны, в частности Зону 2 (Z2), которая опыт последних 18 лет показал, что это зона тренировок, дающая наилучшие результаты для улучшения способности выведения лактата.
«Зона 2 (Z2) зарекомендовала себя как тренировочная зона, дающая наилучшие результаты для улучшения способности выведения лактата».
Так много спортсменов приходят в нашу лабораторию, не зная этих концепций, и тренируются слишком много на «пороге лактата», и, определяя их конкретные тренировочные зоны, мы полностью меняем их тренировочные программы, и мы постоянно видим очень важные улучшения в их способности очищать лактат и производительность, пока в то же время мы значительно сокращаем случаи перетренированности.
В заключение, лактатный порог остается наиболее часто используемым во всем мире тренировочным термином, и все же нет единого мнения о том, что именно он представляет. Существует слишком много путаницы не только в отношении того, что такое порог лактата, но и в отношении того, что такое лактат как таковой, и какова его роль и значение в упражнениях и метаболизме. Я просто верю, что после нескольких десятилетий дискуссий и споров пришло время для концепции «лактатного порога» развиваться и называться и определяться по-другому, чтобы спортсмены и тренеры могли использовать ее в более значимой и понятной манере, чтобы описать это « магия »интенсивности упражнений, которую можно поддерживать только в течение определенного времени, что имеет решающее значение для производительности и успеха.
Произошла ошибка при настройке пользовательского файла cookie
Этот сайт использует файлы cookie для повышения производительности. Если ваш браузер не принимает файлы cookie, вы не можете просматривать этот сайт.
Настройка вашего браузера для приема файлов cookie
Существует множество причин, по которым cookie не может быть установлен правильно. Ниже приведены наиболее частые причины:
- В вашем браузере отключены файлы cookie. Вам необходимо сбросить настройки своего браузера, чтобы он принимал файлы cookie, или чтобы спросить вас, хотите ли вы принимать файлы cookie.
- Ваш браузер спрашивает вас, хотите ли вы принимать файлы cookie, и вы отказались. Чтобы принять файлы cookie с этого сайта, используйте кнопку «Назад» и примите файлы cookie.
- Ваш браузер не поддерживает файлы cookie. Если вы подозреваете это, попробуйте другой браузер.
- Дата на вашем компьютере в прошлом. Если часы вашего компьютера показывают дату до 1 января 1970 г., браузер автоматически забудет файл cookie. Чтобы исправить это, установите правильное время и дату на своем компьютере.
- Вы установили приложение, которое отслеживает или блокирует установку файлов cookie. Вы должны отключить приложение при входе в систему или проконсультироваться с системным администратором.
Почему этому сайту требуются файлы cookie?
Этот сайт использует файлы cookie для повышения производительности, запоминая, что вы вошли в систему, когда переходите со страницы на страницу. Чтобы предоставить доступ без файлов cookie потребует, чтобы сайт создавал новый сеанс для каждой посещаемой страницы, что замедляет работу системы до неприемлемого уровня.
Что сохраняется в файле cookie?
Этот сайт не хранит ничего, кроме автоматически сгенерированного идентификатора сеанса в cookie; никакая другая информация не фиксируется.


