Венозная система — анатомия и функции
Анатомия венозной системы
Венозная система — это та часть системы кровообращения, по которой кровь движется от периферии к сердцу. Мы различаем поверхностную и глубокую венозные системы.
Поверхностная подкожная венозная система нижних конечностей включает в себя большую и малую подкожные вены. Она транспортирует кровь от кожи и подкожных тканей.
Глубокая венозная система включает подвздошные, бедренные, подколенные и глубокие бедренные вены. Глубокие вены обычно проходят параллельно соответствующим артериям.
Эти две венозные системы отделены друг от друга мышцами и фасциями и связаны вместе третьей венозной системой — перфорантными венами (сообщающиеся вены).
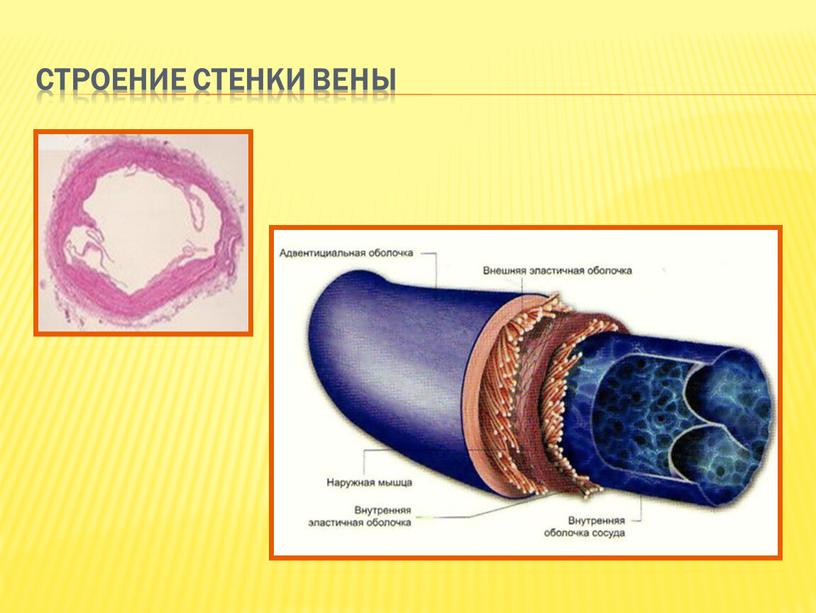
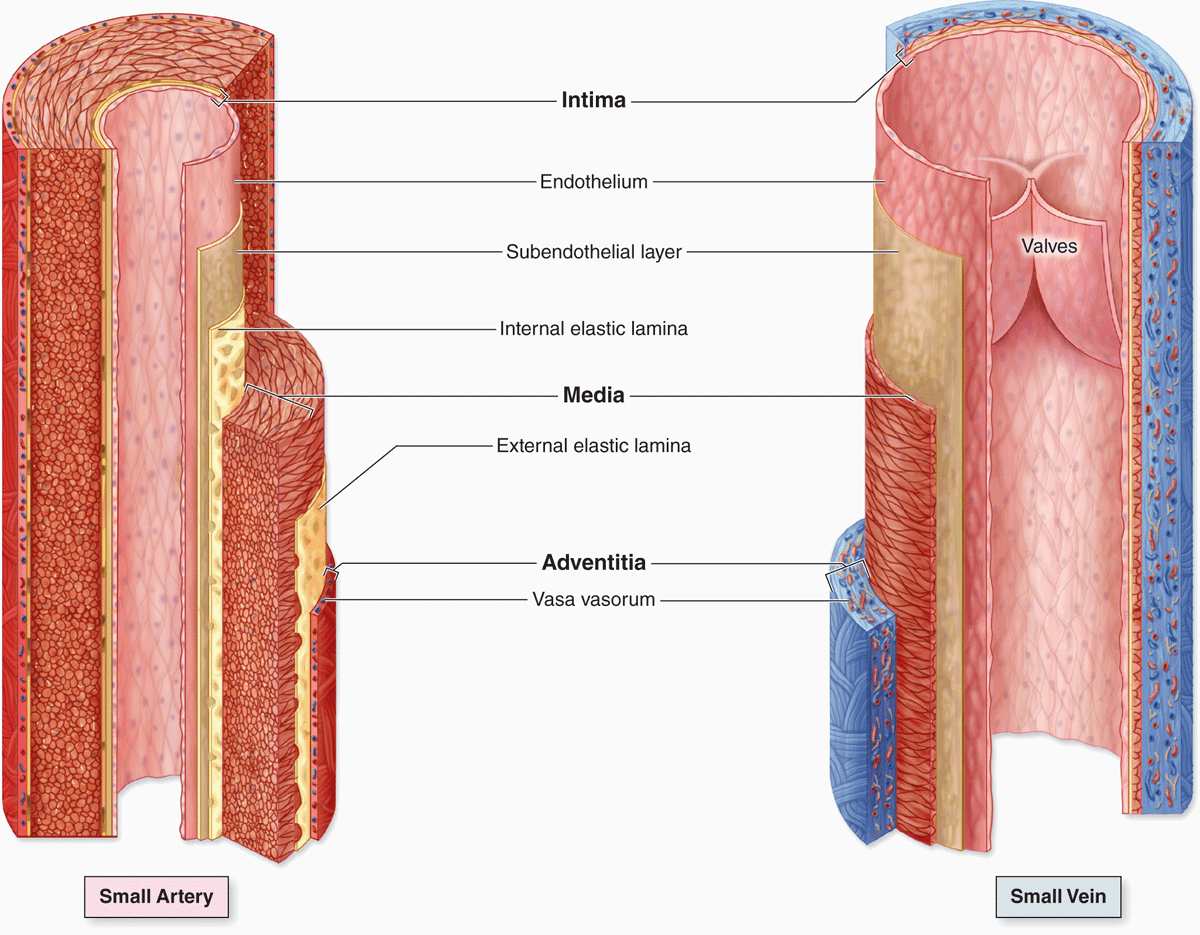
Венозная стенка состоит из трех слоев:
- интима (= внутренний слой)
- медиа (= средний слой) и
- адвентиция (= внешний слой)
Стенки вен тоньше, чем у артерий.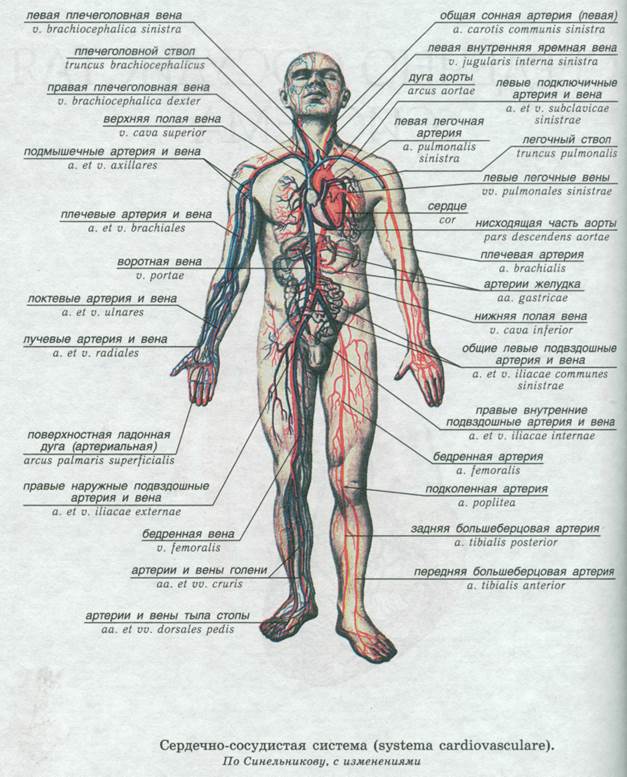
На длинных участках вен имеются клапаны, которые разделяют их на отдельные сегменты. Эти клапаны открываются при движении крови к сердцу против силы тяжести, и закрываются в тот момент, когда кровь останавливается и начинает двигаться в обратном направлении.
Циркуляция крови
Компрессионный трикотаж medi
Компрессионный трикотаж mediЧем артерии отличаются от вен
Артерии — это кровеносные сосуды, которые доставляют кровь, обогащенную кислородом, от сердца к организму.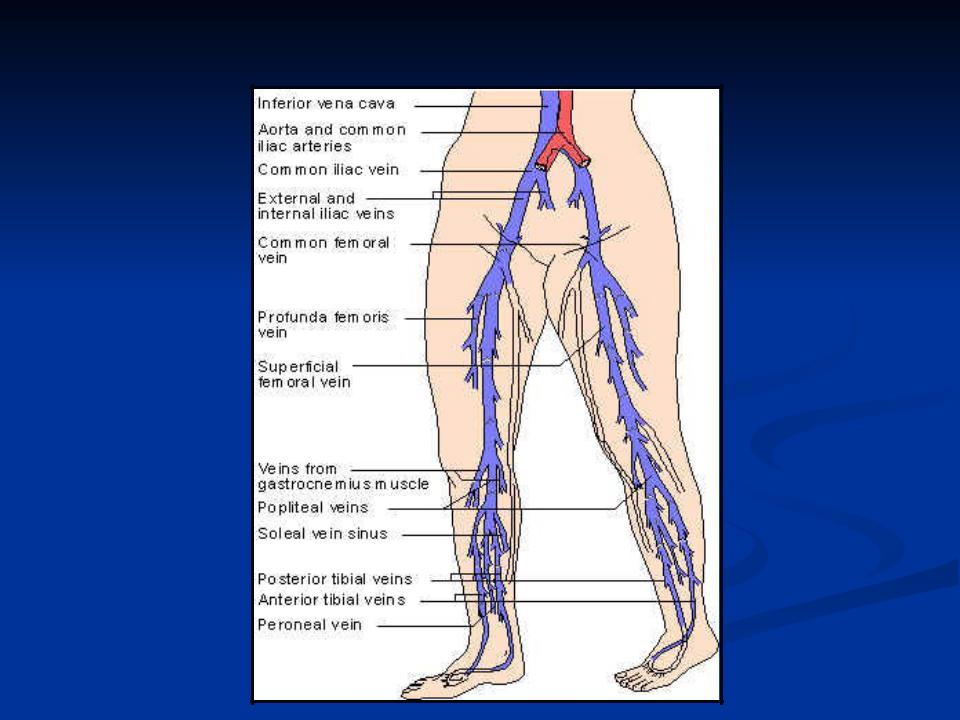 Вены — это кровеносные сосуды, которые доставляют кровь с низким содержанием кислорода из организма обратно в сердце для повторного насыщения кислородом.
Вены — это кровеносные сосуды, которые доставляют кровь с низким содержанием кислорода из организма обратно в сердце для повторного насыщения кислородом.
Артерии и вены являются двумя основными типами кровеносных сосудов человека. Эти сосуды являются каналами, которые распределяют кровь по организму. Чтобы понять, чем артерии отличаются от вен, необходимо разобраться в видах этих кровеносных сосудов и их строении.
Какие существуют типы артерий?
Эластичные артерии имеют в середине стенок толстые эластические волокна. Именно поэтому они могут растягиваться в ответ на каждый толчок крови из сердца. Переходные артерии характеризуются наличием как мышечных, так и эластических волокон в своих стенках. Мышечные артерии берут кровь из эластичных артерий.Они разветвляются в мелкие артерии и артериолы. Артериолы — это наименьший тип артерий, которые транспортируют кровь от сердца. Они служат для транспортировки крови в капиллярные сети.
Какие существуют типы вен?
Глубокие вены расположены в мышечной ткани.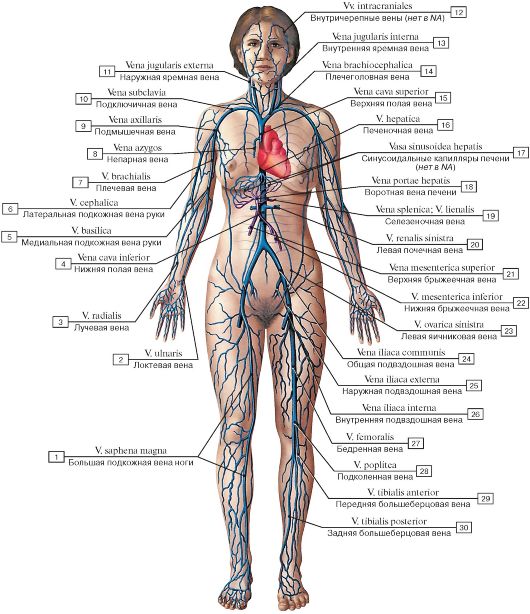 Они характеризуются близким расположением соответствующей артерии рядом. Поверхностные вены расположены ближе к поверхности кожи. У них нет соответствующих артерий рядом. Легочные вены переносят кровь, богатую кислородом, от легких к сердцу. Каждое легкое имеет два набора легочных вен: правые и левые. Системные вены расположены по всему телу от ног до шеи, включая верхние конечности и туловище. Они транспортируют дезоксигенированную кровь обратно в сердце.
Они характеризуются близким расположением соответствующей артерии рядом. Поверхностные вены расположены ближе к поверхности кожи. У них нет соответствующих артерий рядом. Легочные вены переносят кровь, богатую кислородом, от легких к сердцу. Каждое легкое имеет два набора легочных вен: правые и левые. Системные вены расположены по всему телу от ног до шеи, включая верхние конечности и туловище. Они транспортируют дезоксигенированную кровь обратно в сердце.
Чем артерии отличаются от вен и почему это важно знать?
Далее рассмотрим строение вен и артерий. Стенки вен и артерий состоят из трех слоев:
- Наружный слой кровеносного сосуда — в основном он состоит из коллагена и эластичных волокон. Эти волокна позволяют венам и артериям ограниченно растягиваться. Они растягиваются достаточно, чтобы проявлять необходимую гибкость, но при этом сохраняя стабильность под давлением кровотока.
- Средний слой стенок артерий и вен состоит из гладких мышц и эластичных волокон.
 Этот слой значительно толще в артериях и тоньше в венах.
Этот слой значительно толще в артериях и тоньше в венах. - Внутренний слой стенки кровеносного сосуда сделан состоит из эластичного волокна и коллагена. Его консистенция варьируется в зависимости от типа кровеносного сосуда.
В отличие от артерий, вены содержат клапаны. Вены нуждаются в клапанах для того, чтобы кровь имела возможность течь по направлению к сердцу. Эти клапаны особенно важны в нижних и верхних конечностях. Они борются с гравитацией и предотвращают отток крови. Артерии не нуждаются в клапанах, так как создаваемое сокращением сердца давление заставляет кровь интенсивно течь по ним в одном направлении.
Аорта и полая вена — самые большие сосуды в кровообращении
В организме человека есть множество кровеносных сосудов. Все они необходимы для транспортировки крови, несущей органам питательные вещества. Самой большой артерией является аорта.
Значимость артерий для организма человека
Кровеносная система тела состоит:
- сердца;
- артерий;
- вен.
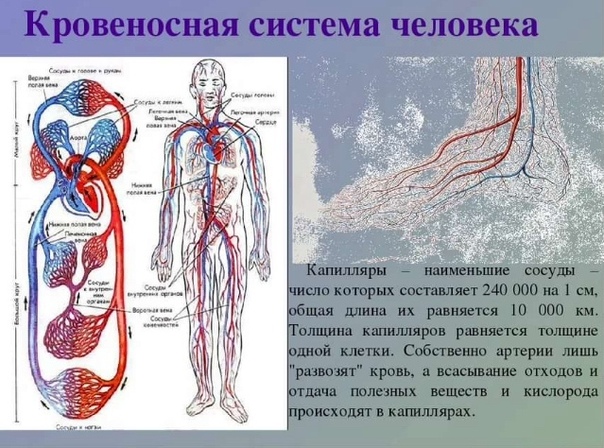
Также сюда входят кроветворные и кровеносные сосуды. По артериям течет артериальная кровь, являющаяся соединительной тканью и имеющая важное значение для кровообращения. Она проходит через сердце, будучи обогащенной кислородом. Аорта, являясь самой большой артерией тела человека, питается кровью, которая перекачивается сердцем. Диаметр аорты составляет 2,5 см. Характерной особенностью этого сосуда являются прочные стенки, способные выдержать давление, обеспечиваемое сокращением сердца.
Исключительными артериями, не несущими артериальную кровь, являются артерии легочного ствола. В данном случае кровообращение позволяет обогатить жидкость кислородом.
В системе кровообращения выделяют два круга: малый и большой. Первый необходим для снабжения кровью легких. Поступая из правого желудочка, жидкость проходит к легочным капиллярам, после чего насыщается кислородом и отправляется в левое предсердие. Артериальная кровь следует по большому кругу и отправляется в левый желудочек, после чего следует к аорте. В теле человека также есть артериолы — маленькие сосуды, позволяющие транспортировать жидкость по всему организму. Через вены эта кровь поступает в правое предсердие.
В теле человека также есть артериолы — маленькие сосуды, позволяющие транспортировать жидкость по всему организму. Через вены эта кровь поступает в правое предсердие.
Значимость вен в системе кровообращения человека
Особенностью вен является перенос красной жидкости, еще не насыщенной кислородом. Они отличаются менее прочными стенками, чем у самой большой артерии в теле. Соответственно, в отличие от артериальных стенок, венозные испытывают меньшее давление. Однако среди вен тоже есть одна довольно крупная. Самая большая вена достигает в диаметре 2,5 сантиметров. Маленькие же вены принято называть венулами.
По легочной вене течет кровь, которая уже насыщена кислородом. У каждой вены есть внутренние клапаны, препятствующие обратному оттоку. Человек, столкнувшийся с нарушениями работы клапанов, может заболеть варикозом.
Где расположена самая большая артерия тела
Самый большой сосуд в теле человека, играющий важную роль в системе кровоснабжения, имеет сложное расположение. Его восходящая часть начинается от левого желудочка, далее ствол идет дугой, спускаясь вниз. Именно внизу находится нисходящая часть, которую разделяют на брюшную и грудную. Особенностью восходящей линии является снабжение артерий, которые переносят кровь к сердцу. Такие артерии называют венечными.
Его восходящая часть начинается от левого желудочка, далее ствол идет дугой, спускаясь вниз. Именно внизу находится нисходящая часть, которую разделяют на брюшную и грудную. Особенностью восходящей линии является снабжение артерий, которые переносят кровь к сердцу. Такие артерии называют венечными.
Дуга аорты переносит кровь к подключичной артерии, а также к общей сонной (левые и плечеголовные стволы). Эти сосуды переносят питательную жидкость, насыщенную кислородом, в мозг, шейный отдел и руки.
Что представляет собой артериальное давление
Именно об артериальном давлении часто приходится слышать обывателям, поэтому ему уделяют самое большое внимание. Действительно, артерии являются важными сосудами, нормальное функционирование которых жизненно необходимо для человека. Нормальное артериальное давление показывает, что кровь может снабжать кислородом и питательными элементами весь организм.
Все кровеносные сосуды делятся на вены и артерии. Когда по ним проходит кровь, создается давление.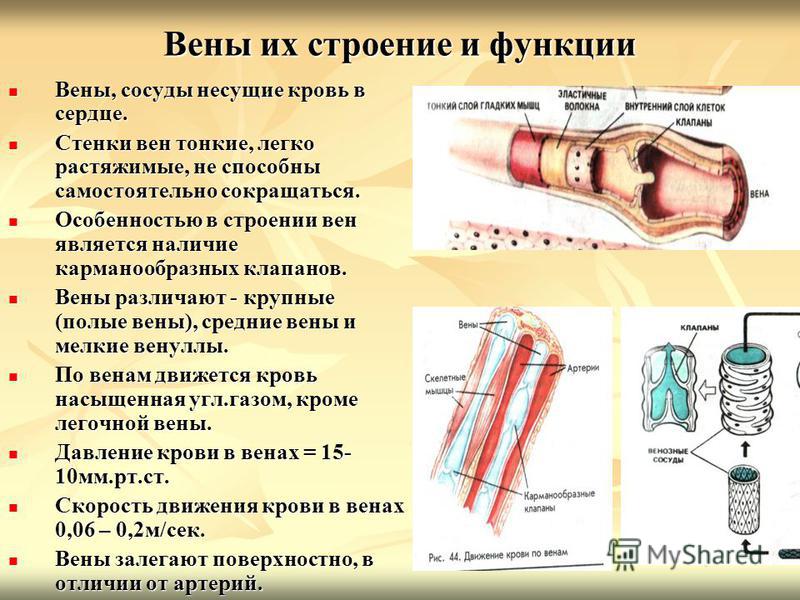 Артериальное давление появляется в результате работы красной жидкости, проходящей по артериальным сосудам, причем его показатели зависят от степени эластичности этих сосудов. Известно, что мышцы нашего сердца выполняют сокращение не менее 60 раз в минуту при нормальной жизнедеятельности. Такой показатель необходим для того, чтобы все тело успешно снабжалось питательной жидкостью.
Артериальное давление появляется в результате работы красной жидкости, проходящей по артериальным сосудам, причем его показатели зависят от степени эластичности этих сосудов. Известно, что мышцы нашего сердца выполняют сокращение не менее 60 раз в минуту при нормальной жизнедеятельности. Такой показатель необходим для того, чтобы все тело успешно снабжалось питательной жидкостью.
При измерении артериального давления регистрируют систолический и диастолический показатели. Первый показатель — это систолическое артериальное давление. Его нормой считается 120 мм рт. ст. Для диастолического давления норма составляет 80 мм рт. ст. Когда происходит увеличение давления, регистрируют систолу. При снижении давления и расслаблении сердечной мышцы регистрируется диастолическое артериальное давление.
Почему возникает высокое артериальное давление
Большое (высокое) артериальное давление принято называть гипертензией. Когда насосная мощность становится чрезмерной, человеческое тело оказывается под нагрузкой собственной крови. Организм оказывается не в состоянии нормально функционировать, что может грозить пагубными последствиями. Гипертензия часто встречается среди жителей развитых стран, где наблюдается стрессовый уровень жизни.
Организм оказывается не в состоянии нормально функционировать, что может грозить пагубными последствиями. Гипертензия часто встречается среди жителей развитых стран, где наблюдается стрессовый уровень жизни.
Чем старше становится человек, тем выше риск развития гипертензии. Даже молодые люди иногда сталкиваются с высоким артериальным давлением. Сосуды могут испытывать нагрузку из-за большого выброса гормонов (адреналин и норадреналин). Проблемы с высоким давлением встречаются у тех, кто любит употреблять пиво, нанося вред почкам. Проблема гипертензии заключается в том, что практически всегда она проходит скрыто. Люди, ведущее малоподвижный образ жизни, накапливающие лишний вес или употребляющие много алкоголя, а также соленой пищи, часто даже не подозревают о развитии гипертензии. Между тем чем выше давление, тем выше становится риск повреждения сосудов. Самые страшные последствия гипертензии представляют собой инсульт, развитие недостаточности сердца или почек, инфаркта миокарда.
Почему возникает гипотензия
Низкое артериальное давление (гипотензия) не является опасным для человека. Однако люди, испытывающие гипотензию, ощущают слабость в теле. Часто возникает головокружение, снижается концентрация и растет утомляемость. Поэтому гипотензия способна причинять большой дискомфорт. Самыми неприятными последствиями этого явления считается снижение интеллектуальной активности. С гипотензией сталкиваются девушки, при этом Всемирная организация здравоохранения утверждает, что низкий уровень давления составляет 100/60 мм рт. ст. для женщин и 110/70 мм рт.ст. для мужчин. Стоит отметить, что некоторые чувствуют себя вполне комфортно даже при постоянной гипотензии.
Самая большая вена тела человека
В системе кровообращения принято выделять две полые вены: нижнюю и верхнюю. Нижняя полая вена собирает венозную кровь, циркулирующую в нижней части организма. Верхняя полая вена идет от головы и впадает в правое предсердие.
Роль сердца в кровообращении
Система кровообращения человека представляет собой сложную структуру. Движение крови происходит благодаря разнице давления между артериальной и венозной системами. Именно сердце порождает разницу давления, перекачивая кровь из вен в артерии. У артерий практически нет гладких мышц, но есть эластичная оболочка, за счет которой амортизируются перепады давления. Благодаря упругости и растяжимости, артерии способны принимать дополнительные объемы красной жидкости, приводящие к подъему давления на 50-60 мм.
Движение крови происходит благодаря разнице давления между артериальной и венозной системами. Именно сердце порождает разницу давления, перекачивая кровь из вен в артерии. У артерий практически нет гладких мышц, но есть эластичная оболочка, за счет которой амортизируются перепады давления. Благодаря упругости и растяжимости, артерии способны принимать дополнительные объемы красной жидкости, приводящие к подъему давления на 50-60 мм.
Благодаря упругим стенкам артерий, нужное давление поддерживается, причем даже если сердце в данный момент не перекачивает кровь. Это позволяет ему не упасть до нуля. Кровоток в системе кровоснабжения циркулирует непрерывно. Когда стенка растягивается, происходит пульсация, которую можно прощупать, приложив палец. Благодаря гладкой мускулатуре артериолы быстро изменяют просвет, что позволяет создавать сопротивление для кровотока. Вот почему на артериолы приходится максимум падения давления. В венозной системе кровь оказывается благодарят посткапиллярам и венам.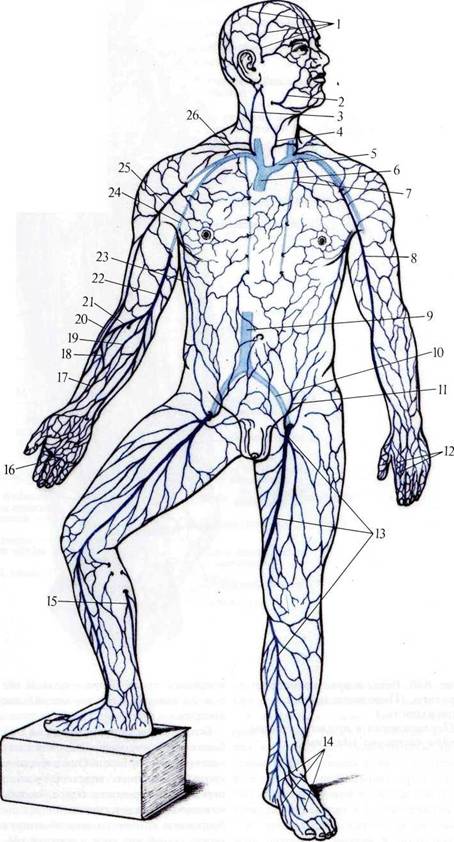
В человеке за счет развитой системы кровообращения есть несколько механизмов, способствующих венозному возврату. Первый представляет собой базовый механизм, сводящийся к использованию перепадов давления. Вены есть и в скелетных мышцах, причем во время их сокращения кровь как бы выжимается из мышцы. Подобный механизм важен для ног, ведь из-за прямохождения красной жидкости приходится преодолевать гравитацию. Третий механизм представляет собой использование атмосферного давления в грудной клетке. Когда человек совершает вдох, кровь в его теле начинает цикл возврата. Именно поэтому принято считать, что вены играют роль емкостных сосудов.
Наконец, следует отметить и капиллярную систему, играющую большую роль в кровообращении. Капилляры характеризуются самой высокой проницаемостью, поэтому в капиллярной крови хорошо растворяются низкомолекулярные вещества. С помощью капилляров в теле осуществляется обмен веществ между жидкостью ткани и плазмой. Капиллярная кровь характеризуется феноменальными показателями. Например, один из самых удивительных фактов говорит, что даже при диффузии обменная поверхность капилляров человеческого тела обеспечивает перекачку 60 литров крови за минуту.
Например, один из самых удивительных фактов говорит, что даже при диффузии обменная поверхность капилляров человеческого тела обеспечивает перекачку 60 литров крови за минуту.
Особенности строения артерий
Мы обозначили, что артерии представляют собой сосуды гораздо более крепкие, чем вены. Строение любой артерии трехслойное. Первый слой представляет собой эндотелиальные клетки. Его называют внутренним. Средний слой состоит из волокон гладкой мускулатуры и эластичной ткани. В этом и состоит самое главное отличие артерий друг от друга. В зависимости от преобладания конкретных волокон различаются и сами артерии. Крупные отличаются большим объемом коллагена и эластина. Мелкие же (артериолы) почти на 90% состоят из мышечных элементов. Наружный слой представляет собой соединительную ткань.
Особенности артериальной системы у мужчин
Самым главным отличием мужской артериальной системы от женской является наличие яичковых сосудов. При этом отмечается, что сердечно-сосудистые заболевания встречаются чаще именно у мужской половины населения планеты. Причем наибольший ущерб наносит системе кровообращения холестерин, способствующий развитию атеросклероза. Данное явление также становится причиной развития инфаркта миокарда.
Причем наибольший ущерб наносит системе кровообращения холестерин, способствующий развитию атеросклероза. Данное явление также становится причиной развития инфаркта миокарда.
Особенности артериальной системы у женщин
Благодаря наличию особых гормонов, кровообращение женщин защищено от воздействия холестерина. Но в какой-то момент эстрогены перестают вырабатываться, что создает риск развития гипертонии. Сложная ситуация складывается при беременности, так как это приводит к увеличению объема циркулирующей крови.
Что мы узнали о венах и артериях
Вены и артерии тела человека являются основой сосудистой системы. Они имеют разную структуру, так как должны выполнять различные функции. Артерия несет в организме обогащенную кислородом кровь к органам прямо из сердца. Чтобы обеспечить движение крови, используются сокращения миокарда, поэтому движение становится интенсивным и может достигнуть скорости 25 см/сек.
В венах кровь движется непосредственно от самих органов к сердцу. Она бедна кислородом, но в ней много углекислого газа и прочих продуктов распада. Движение венозной происходит за счет строения сосуда. Именно поэтому скорость здесь на порядок ниже. Одновременно процент венозной крови составляет 64%, тогда как на артериальную приходится всего 14%.
Она бедна кислородом, но в ней много углекислого газа и прочих продуктов распада. Движение венозной происходит за счет строения сосуда. Именно поэтому скорость здесь на порядок ниже. Одновременно процент венозной крови составляет 64%, тогда как на артериальную приходится всего 14%.
Вена, анатомия. Вена — кровеносный сосуд, по которому кровь движется к сердцу. Вены получают кровь из посткапиллярных венул. Вены объединяются в венозную систем
4. Движение крови по венам
Линейная скорость кровотока в венах, как и в других отделах сосудистого русла, зависит от суммарной площади поперечного сечения, поэтому она наименьшая в венулах 0.3 — 1.0 см/с, наибольшая — в полых венах 10 — 25 см/с. Течение крови в венах ламинарное, но в месте впадения двух вен в одну возникают вихревые потоки, перемешивающие кровь, её состав становится однородным.
Давление крови в венах является значительно более низким, чем в артериях, и может быть ниже атмосферного ; венозные сосуды имеют более тонкие стенки, и при физиологических изменениях внутрисосудистого давления меняется их ёмкость особенно в начальном отделе венозной системы, во многих венах имеются клапаны, препятствующие обратному току крови.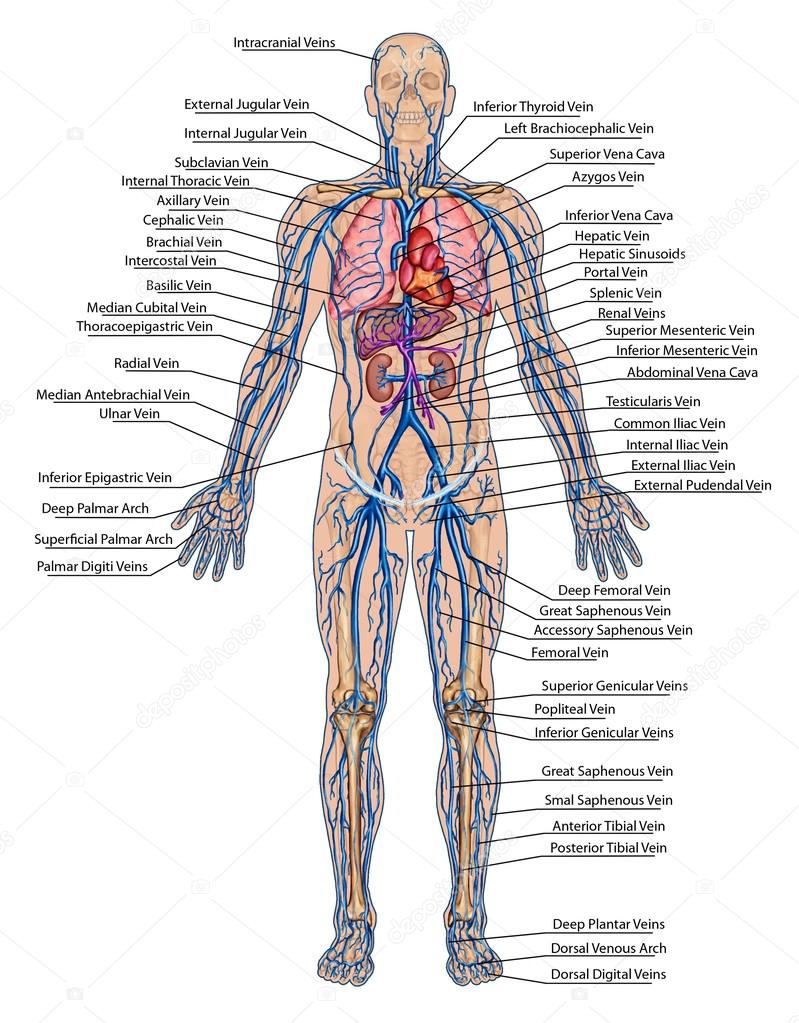
 Флебография используется в диагностике, например, при недостаточности трехстворчатого клапана, а также при расчётах величины давления крови в малом круге кровообращения.
Флебография используется в диагностике, например, при недостаточности трехстворчатого клапана, а также при расчётах величины давления крови в малом круге кровообращения.Основная движущая сила — разница давлений в начальном и конечном отделах вен, создаваемой работой сердца. Имеется ряд вспомогательных факторов, влияющих на возврат венозной крови к сердцу.
 Ёмкость венозной системы при этом увеличивается из-за растягивающего действия гидростатического фактора, и в венах дополнительно накапливается 400 — 600 мл притекающей из микрососудов крови; соответственно на эту же величину снижается венозный возврат к сердцу. Одновременно в венах, расположенных выше уровня сердца, венозное давление уменьшается на величину гидростатического давления и может стать ниже атмосферного. Так, в венах черепа оно ниже атмосферного на 10 мм рт. ст., но вены не спадаются, так как фиксированы к костям черепа. В венах лица и шеи давление равно нулю, и вены находятся в спавшемся состоянии. Отток осуществляется через многочисленные анастомозы системы наружной яремной вены с другими венозными сплетениями головы. В верхней полой вене и устье яремных вен давление в положении стоя равно нулю, но вены не спадаются из-за отрицательного давления в грудной полости. Аналогичные изменения гидростатического давления, венозной ёмкости и скорости кровотока происходят также при изменениях положения поднимании и опускании руки относительно сердца.
Ёмкость венозной системы при этом увеличивается из-за растягивающего действия гидростатического фактора, и в венах дополнительно накапливается 400 — 600 мл притекающей из микрососудов крови; соответственно на эту же величину снижается венозный возврат к сердцу. Одновременно в венах, расположенных выше уровня сердца, венозное давление уменьшается на величину гидростатического давления и может стать ниже атмосферного. Так, в венах черепа оно ниже атмосферного на 10 мм рт. ст., но вены не спадаются, так как фиксированы к костям черепа. В венах лица и шеи давление равно нулю, и вены находятся в спавшемся состоянии. Отток осуществляется через многочисленные анастомозы системы наружной яремной вены с другими венозными сплетениями головы. В верхней полой вене и устье яремных вен давление в положении стоя равно нулю, но вены не спадаются из-за отрицательного давления в грудной полости. Аналогичные изменения гидростатического давления, венозной ёмкости и скорости кровотока происходят также при изменениях положения поднимании и опускании руки относительно сердца.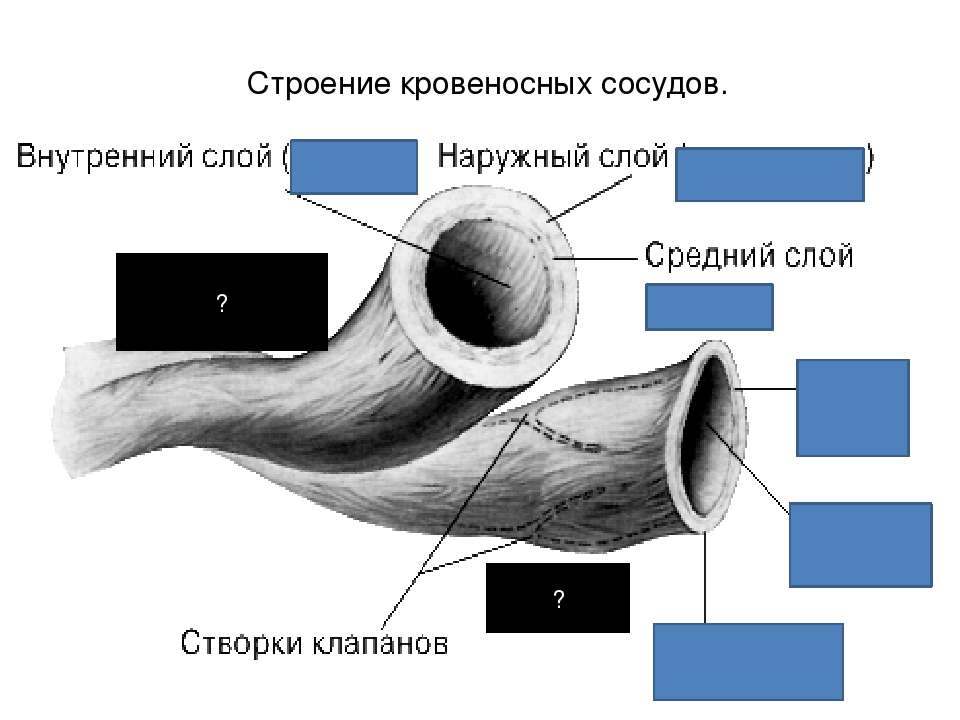
 Наличие клапанного аппарата в венах предотвращает обратный ток крови в венах при их сдавливании. 4. Дыхательный насос Во время вдоха давление в грудной клетке уменьшается, внутригрудные вены расширяются, давление в них снижается до — 5 мм рт. ст., происходит засасывание крови, что способствует возврату крови к сердцу, особенно по верхней полой вене. Улучшению возврата крови по нижней полой вене способствует одновременное небольшое увеличение внутрибрюшного давления, увеличивающее локальный градиент давления. Однако во время выдоха приток крови по венам к сердцу, напротив, уменьшается, что нивелирует возрастающий эффект. 5. Присасывающее действие сердца способствует кровотоку в полых венах в систоле фаза изгнания и в фазе быстрого наполнения. Во время периода изгнания атриовентрикулярная перегородка смещается вниз, увеличивая объём предсердий, вследствие чего давление в правом предсердии и прилегающих отделах полых вен снижается. Кровоток увеличивается из-за возросшей разницы давления присасывающий эффект атриовентрикулярной перегородки.
Наличие клапанного аппарата в венах предотвращает обратный ток крови в венах при их сдавливании. 4. Дыхательный насос Во время вдоха давление в грудной клетке уменьшается, внутригрудные вены расширяются, давление в них снижается до — 5 мм рт. ст., происходит засасывание крови, что способствует возврату крови к сердцу, особенно по верхней полой вене. Улучшению возврата крови по нижней полой вене способствует одновременное небольшое увеличение внутрибрюшного давления, увеличивающее локальный градиент давления. Однако во время выдоха приток крови по венам к сердцу, напротив, уменьшается, что нивелирует возрастающий эффект. 5. Присасывающее действие сердца способствует кровотоку в полых венах в систоле фаза изгнания и в фазе быстрого наполнения. Во время периода изгнания атриовентрикулярная перегородка смещается вниз, увеличивая объём предсердий, вследствие чего давление в правом предсердии и прилегающих отделах полых вен снижается. Кровоток увеличивается из-за возросшей разницы давления присасывающий эффект атриовентрикулярной перегородки.
Анатомия человека. Кровеносные сосуды — материалы для подготовки к ЕГЭ по Биологии
Автор статьи — профессиональный репетитор М. А. ФилатовВ организме человека различают три основных типа сосудов:
- Артерии
- Вены
- Капилляры
Артерии – это сосуды, по которым кровь течёт от сердца. Самая крупная артерия – это аорта, она отходит от левого желудочка. В артериях кровь движется под большим давлением, поэтому они имеют толстые и упругие стенки, образованные мышечной тканью.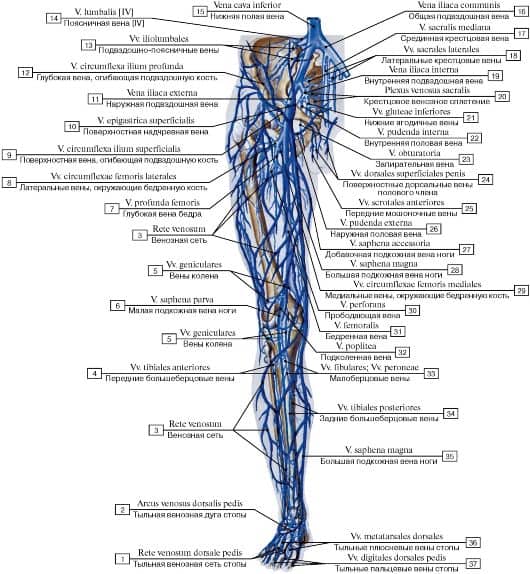
Стенки некоторых крупных артерий настолько толстые, что питательные вещества и кислород не могут проникнуть в глубокие слои мышечной стенки сосуда, поэтому в стенки прорастают дополнительные маленькие сосуды, которые снабжают питанием мышечные клетки, такие сосуды называют сосудами сосудов. Крупные артерии многократно ветвятся на более мелкие, в результате образуя сеть капилляров.
Капилляры – это мельчайшие кровеносные сосуды. Их диаметр примерно соответствует диаметру эритроцита, а в некоторых случаях даже меньше его. Таким образом, достигается наибольшая поверхность соприкосновения эритроцита со стенкой капилляра, обеспечивая наилучший газообмен. Капилляры пронизывают все органы человека, их общая протяженность составляет около 100 тысяч километров. После газообмена кровь из капилляров собирается в вены.
Рис. Кровеносные сосуды: 1 – вена с клапанами, 2 – артерия, 3 – капилляр.
Вены – это сосуды, по которым кровь поступает к сердцу. Многие из них располагаются неглубоко под кожей, поэтому они хорошо видны на теле. Давление крови в венах меньше чем в артериях, и даже чем в капиллярах. Это связано с тем, что пройдя через капилляры, кровоток теряет скорость из-за трения о стенки капилляров. Во многих венах имеются специальные приспособления – венозные клапаны, они не дают крови течь назад.
Многие из них располагаются неглубоко под кожей, поэтому они хорошо видны на теле. Давление крови в венах меньше чем в артериях, и даже чем в капиллярах. Это связано с тем, что пройдя через капилляры, кровоток теряет скорость из-за трения о стенки капилляров. Во многих венах имеются специальные приспособления – венозные клапаны, они не дают крови течь назад.
NB! Несколько веков назад считалось недостойным знатной персоны проводить много времени на свежем воздухе, тем самым люди стремились подчеркнуть, что они не относятся к рабочему классу. Как следствие богатые особы имели очень бледную кожу, через которую хорошо проступали вены. Поскольку вены похожи на синие жилки под кожей, то про таких людей говорили, что у них по жилам «течёт голубая кровь».
Поражение сосудов шеи
Поражение сосудов шеи (прецеребральных отделов артерий головного мозга).
Брахиоцефальные артерии (БЦА) – это магистральные сосуды организма. К БЦА относятся:
К БЦА относятся:
- брахиоцефальный ствол,
- общая сонная артерия (делится на внутреннюю и наружную артерии)
- подключичные артерии,
- позвоночные артерии.
Анатомия позвоночных артерий часто индивидуальна. Внутренние сонные и позвоночные артерии (они же прецеребральные отделы артерий головного мозга) после проникновения внутрь черепа образуют Виллизиев круг. Это анатомическое образование призвано обеспечивать равномерное распределение крови по всем отделам головного мозга.
Проблема в том, что анатомия Вилизиевого круга также вариабельна и более чем у 20% людей европейской популяции круг разомкнут. При такой особенности анатомии достаточно прекращения кровообращения даже в одной из артерий для развития инсульта (гибель ткани мозга).
Однако, подавляющее число ишемических инсультов эмбологенного характера. Это означает, что причиной недуга является засорение артерий мозга материальными объектами.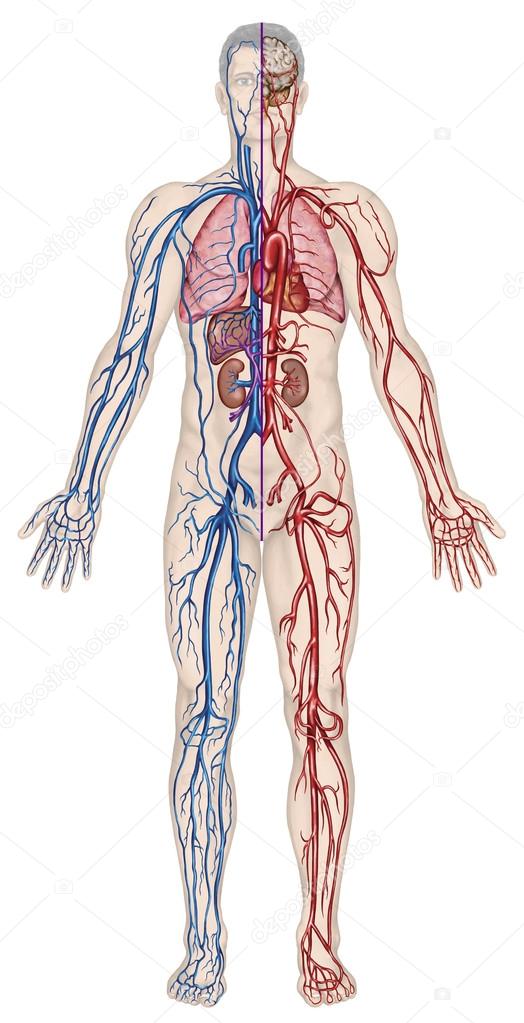
Эмболию могут вызывать тромбы из полостей сердца (при его патологии), но чаще всего – это фрагменты распадающихся атеросклеротических бляшек из сонных артерий и зоны деления общей сонной артерии на внутреннюю и наружную (зона бифуркации). Именно зона бифуркации — типичное место для возникновения и развития атеросклеротической бляшки.
Бляшки, в свою очередь подразделяются на различные типы и классифицируются по степени сужения сосуда. Наиболее опасными являются эмбологенный бляшки – то есть те, которые в любой момент могут разрушиться и все их содержимое мгновенно закупорит множество артерий головного мозга и вызовет инсульт.
Предвестниками инсульта могут быть:
- головная боль;
- головокружение;
- онемение половины тела;
- нарушения зрения;
- затруднения при формулировании мыслей.
- нарушение артикуляции
- нарушения в тонких функциях кистей рук (например, при письме)
- затруднения при ходьбе и т.
 д.
д.
Очень часто инсульт возникает без каких либо предвестников. Именно поэтому ультразвуковая диагностика артерий шеи (триплексное, дуплексное сканирование) совершенно необходимая процедура для мужчин и женщин после 40-50 лет.
Ангиохирурги СПБ больницы РАН используют различные методы лечения атеросклероза БЦС, в случае сонных артерий – это прежде всего каротидная эндартерэктомия — радикальное оперативное лечение, позволяющее извлечь бляшку и восстановить целостность стенки сосуда.
Операция проводится по методике обеспечивающей максимально возможную степень защиты головного мозга и микрохирургическое восстановление артерии.
На сегодняшний день каротидная эндартерэктомия дает наиболее стойкие положительные результаты на отдаленных периодах наблюдения – от 5 до 20~25 лет. Именно поэтому в странах с развитой медициной каротидная эндартерэктомия является основным методом лечения данной патологии.
Для других зон поражения в СПб больнице РАН проводятся трансплантации артерий и шунтирующие операции.
Получить консультацию специалистов и узнать подробности можно через контакт-центр 323 45 35
Вариантная анатомия глубоких вен головного мозга человека
На правах рукописи
ЕВСЕЕВ АЛЕКСЕЙ ВИТАЛЬЕВИЧ
ВАРИАНТНАЯ АНАТОМИЯ ГЛУБОКИХ ВЕН ГОЛОВНОГО МОЗГА ЧЕЛОВЕКА
14.03.01. — Анатомия человека
АВТОРЕФЕРАТ диссертации на соискание ученой степени кандидата медицинских наук
КРАСНОЯРСК-2013
Работа выполнена на кафедре оперативной хирургии и топографической анатомии ГБОУ ВПО «Красноярский государственный медицинский университет им. проф. В. Ф. Войно-Ясенецкого» Министерства здравоохранения Российской Федерации.
Научный руководитель: кандидат медицинских наук, доцент
Шнякин Павел Геннадьевич
Официальные оппоненты:
Деревцова Светлана Николаевна — доктор медицинских наук, доцент кафедры анатомии и гистологии человека ГБОУ ВПО «Красноярский государственный медицинский университет им.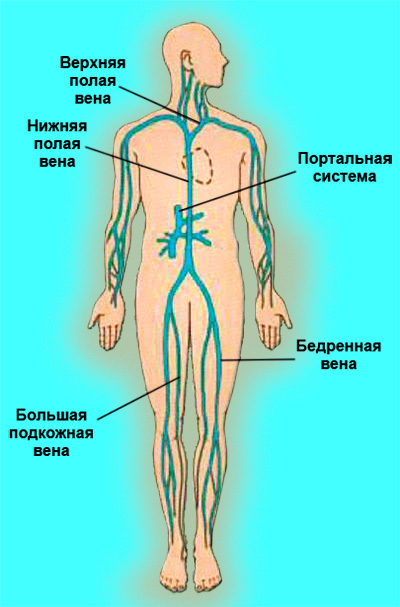 проф. В. Ф. Войно-Ясенецкого» Министерства здравоохранения Российской Федерации. Машак Александр Николаевич — доктор медицинских наук, профессор, заведующий кафедрой анатомии человека педиатрического факультета ГБОУ ВПО «Новосибирский государственный медицинский университет» Министерства здравоохранения Российской Федерации.
проф. В. Ф. Войно-Ясенецкого» Министерства здравоохранения Российской Федерации. Машак Александр Николаевич — доктор медицинских наук, профессор, заведующий кафедрой анатомии человека педиатрического факультета ГБОУ ВПО «Новосибирский государственный медицинский университет» Министерства здравоохранения Российской Федерации.
Ведущая организация:
ГБОУ ВПО «Алтайский государственный медицинский университет» Министерства здравоохранения Российской Федерации.
Защита диссертации состоится «Г » в часов на
заседании диссертационного совета Д 208.037.02. при ГБОУ ВПО «Красноярский государственный медицинский университет им. проф. В. Ф. Войно-Ясенецкого» Министерства здравоохранения Российской Федерации (660022, г. Красноярск, ул. Партизана Железняка, 1).
С диссертацией можно ознакомиться в научной библиотеке ГБОУ ВПО «Красноярский государственный медицинский университет им. проф. В. Ф. Войно-Ясенецкого» Министерства здравоохранения Российской Федерации по адресу: 660022, г. 2013г.
2013г.
Ученый секретарь диссертационного совета, кандидат медицинских наук, доцент
Кочетова Людмила Викторовна
«О С Vi LA !1 с : Hb: 11 ПАЯ ЬИВЛйаТЕКА 2013
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Актуальность проблемы. Сосудистые заболевания головного мозга остаются одной из главных проблем современной медицины, вносящих существенный вклад в общую структуру смертности и инвалидности населения всего земного шара (Суслина 3. А., 2006; Liney G., 2006; Скворцова В. И., 2007; Тул Д., 2007; Agid R., 2008; Малярова Е. Ю., 2010). Параллельно с совершенствованием методов диагностики и лечения больных с цереброваскулярной патологией растет заболеваемость нарушениями мозгового кровообращения. По мнению ряда исследователей, это связано с ростом числа больных с артериальной гипертонией (Суслина 3. А., 2006; Thubrikar M. J., 2007; Белова Л. А., 2009; Салихова Е. А., 2010; Lumenta С. В., 2010).
В настоящее время лечение больных с цереброваскулярной патологией в основном носит симптоматический, редко — патогенетический характер, и практически не воздействует на этиологию заболевания, которая в большинстве случаев остается не до конца изученной.
В этой связи остаётся актуальным более детальное и при этом комплексное исследование сосудов головного мозга, так как даже незначительные особенности анатомии сосудов головного мозга могут оказаться решающими в развитии цереброваскулярной патологии.
Результаты проводимых морфологических исследований сосудов головного мозга в большей степени касаются артериальной системы, в то время как мозговым венам, общее количество которых превышает количество артерий, уделено меньшее внимание (Гонгальский В. В., 2005; Tobinick Е., 2006; Uddin M. А., 2006; Лойт А. А., 2007; Манвелов Л. С., 2007; Pranevicius О., 2007; Runge V. M., 2007; Zhao M., 2007; Bateman G. A., 2008). При этом очевидно, что система «притока» крови не может являться всеобъемлющей и основной мишенью при развитии цереброваскулярной патологии, а система «оттока» оставаться интактной.
С совершенствованием современных визуализирующих методик исследования сосудов головного мозга, таких как церебральная ангиография, мультиспиральная компьютерная ангиография, магнитно-резонансная ангиография, транскраниапьная ультразвуковая допплерография, всё чаще неврологами, нейрохирургами и врачами функциональной диагностики выставляются такие диагнозы, как церебральная венозная недостаточность, венозная энцефалопатия, тромбозы вен и венозных синусов головного мозга (Lasjaunias Р. , 2003; Marques M. С., 2003; Wasay M., 2005; Ллойт А. А., 2007; Zadeh G., 2007; Ворожцова И. Н., 2008; Тулупов А. А., 2009; Lumenta С. В., 2010; Иванов А. Ю„ 2011; Тулупов А. А., 2012). В этой связи для диагностики патологии венозной системы головного мозга крайне важным остаётся знание вариантной анатомии этой системы, и в первую очередь
, 2003; Marques M. С., 2003; Wasay M., 2005; Ллойт А. А., 2007; Zadeh G., 2007; Ворожцова И. Н., 2008; Тулупов А. А., 2009; Lumenta С. В., 2010; Иванов А. Ю„ 2011; Тулупов А. А., 2012). В этой связи для диагностики патологии венозной системы головного мозга крайне важным остаётся знание вариантной анатомии этой системы, и в первую очередь
глубоких мозговых, вен, осуществляющих отток венозной крови от подкорково-стволовых структур.
В настоящее время наиболее часто встречаемые топографо-анатомические варианты глубоких вен головного мозга представлены во многих отечественных и зарубежных руководствах (Netter F. Н., 2003; Lombardi М„ 2005; Ллойт А. А., 2006; Liney G., 2006; Muhammad A. TJ., 2006; Rhoton А., 2007; Runge V. М., 2007), в то время как крайние варианты анатомии и конституциональные особенности изучены недостаточно. При этом знание вариантов анатомии венозной системы головного мозга, в том числе и глубоких мозговых вен, имеет не только важный фундаментальный, но и практический интерес, в первую очередь для нейрохирургов, как возможный источник массивных кровотечений при операциях на основании головного мозга и в полости боковых и третьего желудочков.
Учитывая актуальность проблемы и недостаток информации о конституциональных особенностях вариантной анатомии глубоких мозговых вен, поставлены цель и задачи исследования.
Цель исследования — выявление вариантной анатомии глубоких вен головного мозга у трупов мужчин с разной формой головы.
Задачи исследования:
1. Изучить вариантную анатомию базальной вены, внутренней мозговой вены, большой мозговой вены и их притоков у трупов мужчин с разной формой головы.
2. Провести сравнительный анализ вариантной анатомии глубоких вен головного мозга у трупов мужчин с разной формой головы.
3. Выявить особенности венозного оттока от подкорковых структур головного мозга у трупов мужчин с разной формой головы.
4. Установить варианты анатомии глубоких вен головного мозга у мужчин, умерших от внутримозгового кровоизлияния.
Личный вклад автора. Антропометрические, органометрические исследования, статистическая обработка, анализ и написание диссертации выполнялись автором самостоятельно.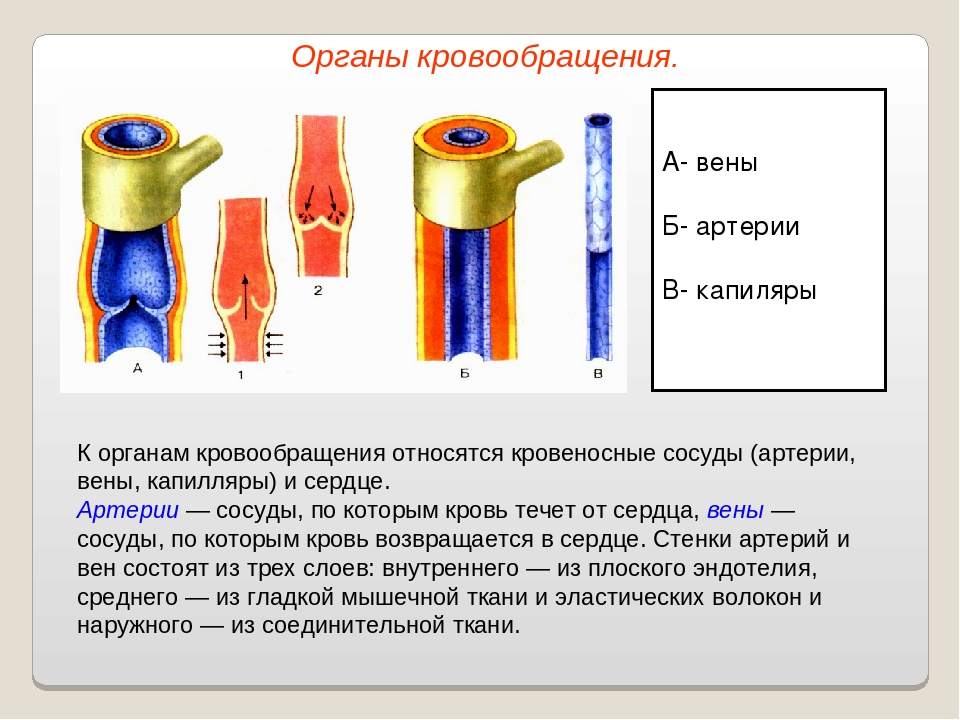
Новизна исследования. Впервые получены сведения о конституциональных особенностях глубоких вен головного мозга человека.
Выявлены крайние варианты анатомии глубоких вен головного мозга: отсутствие передней мозговой и передней соединительной вен, удвоение базальной вены, начало базальной вены от нижней вены бокового желудочка, удвоение верхней ворсинчатой вены.
Установлено, что длина глубоких вен головного мозга с продольным направлением (базапьная вена и внутренняя мозговая вена), имеет наибольшее значение у долихоцефалов, а брахицефалам свойственна наибольшая длина вен, идущих в поперечном направлении (глубокая средняя мозговая вена).
Выявлено, что в месте впадения в большую мозговую вену в трети случаев отмечается значительное преобладание (в 1,5-3 раза) диаметра внутренней мозговой вены над диаметром базальной веной, в остальных случаях диаметр базальной вены и внутренней мозговой вены приблизительно одинаков. Преобладание диаметра базальной вены над внутренней мозговой веной в месте впадения в большую мозговую вену не выявлено. Таким образом, в трети случаев имеются морфологические предпосылки для преимущественного оттока венозной крови из подкорковых структур в систему внутренней мозговой вены.
Таким образом, в трети случаев имеются морфологические предпосылки для преимущественного оттока венозной крови из подкорковых структур в систему внутренней мозговой вены.
Получены результаты по вариантной анатомии глубоких вен головного мозга у мужчин, умерших от внутримозгового кровоизлияния. Выявлено, что средние показатели длины, диаметра и расположения вен совпадают с показателями у лиц, умерших от причин, не связанных с поражением центральной нервной системы.
Теоретическая и практическая значимость. Полученные сведения имеют важное теоретическое и практическое значение. Данные о вариантной анатомии глубоких вен головного мозга человека с учетом конституциональных особенностей дополняют имеющиеся сведения в области анатомии человека. Эти сведения могут быть использованы в ходе обучения студентов медицинских вузов.
На основании исследования в дооперационном периоде по форме головы пациента нейрохирург сможет с определённой степенью вероятности предположить о конституциональных особенностях глубоких вен головного мозга, что крайне важно при операциях на основании черепа и желудочках головного мозга. Полученные данные по вариантой анатомии мозговых вен могут быть использованы рентгенологами для интерпретации данных МРТ-ангиографии, МСКТ-ангиографии головного мозга.
Полученные данные по вариантой анатомии мозговых вен могут быть использованы рентгенологами для интерпретации данных МРТ-ангиографии, МСКТ-ангиографии головного мозга.
Формы внедрения. Полученные результаты внедрены в процесс обучения на кафедре анатомии и гистологии человека и кафедре оперативной хирургии и топографической анатомии КрасГМУ им. проф. В. Ф. Войно-Ясенецкого.
Основные положения, выносимые на защиту:
1. Анатомия глубоких вен головного мозга соответствует форме головы.
2. Варианты архитектоники глубоких вен головного мозга предопределяют особенности венозного оттока от подкорковых структур головного мозга.
Апробация работы. Материалы диссертационного исследования докладывались на всероссийских научно-практических конференциях (Ежегодные научно-практические конференции Красноярского государственного медицинского университета им. проф. В. Ф. Войно-Ясенецкого в 2012-2013 гг.; Всероссийская конференция студентов и молодых учёных «Пироговские чтения», г. Челябинск, 2012г.; Русско-
Челябинск, 2012г.; Русско-
японский симпозиум по нейронаукам, г. Красноярск, 2012 г.; Всероссийская научно-практическая конференция молодых учёных «Поленовские чтения», г. Санкт-Петербург, 2013 г.).
Публикации. По теме диссертации опубликовано 7 научных работ, из них 4 статьи в журналах, рекомендованных ВАК РФ.
Структура и обьем диссертации. Диссертация изложена на 126 страницах машинописного текста (собственного текста — 89 страниц), состоит из введения, обзора литературы, материалов и методов исследования, главы собственных исследований, заключения, выводов и практических рекомендаций. При изложении материала использовано 43 таблицы и 40 рисунков.
Список литературы состоит из 100 отечественных и 102 зарубежных источников.
МАТЕРИАЛ И МЕТОДЫ ИССЛЕДОВАНИЯ
Антропометрический, органометрический методы исследования и метод наливки сосудов головного мозга красителем выполнены на базе кафедры топографической анатомии и оперативной хирургии КрасГМУ им. головы (рис. 1).
головы (рис. 1).
Рис. I. Точки для измерения продольною и поперечного размеров головы.
В дальнейшем вычислялся индекс головы (ИГ) по формуле: ИГ = Поперечный размер / Продольный размер х 100. В соответствии с полученными цифрами, определялась форма головы (табл. 1).
Таблица I.
Определение формы головы но индексу головы_
Долихоцефалическая ИГ < 74,9
Мезоцефал ичсская 75,0< ИГ<79,9
Брахицефалическая ИГ>80
В изъятом мозге катетеризировалась большая мозговая вена (БМВ) и дистиллированной водой промывались глубокие вены головного мозга и препарат 7 дней фиксировался в растворе нейтрального формалина. Для лучшей визуализации глубоких вен основания мозга препарировались и удалялись артерии Виллизиевого круга, выполнялась частичная резекция базапьных отделов височных долей. Повторно катетеризировалась, БМВ и в неё под небольшим давлением водился раствор подогретого желатина, окрашенного раствором метиленового синего.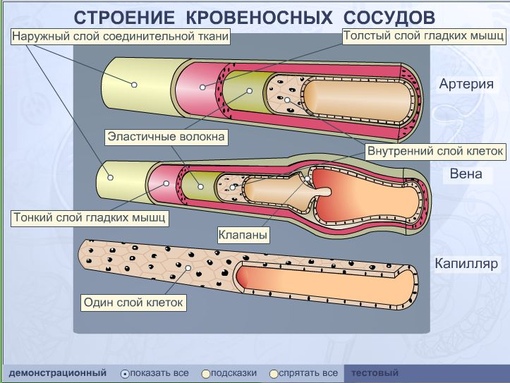 Раствор вводился до прокрашивания истоков базальной вены (БВ) с обеих сторон.
Раствор вводился до прокрашивания истоков базальной вены (БВ) с обеих сторон.
Последовательно изучались глубокие вены головного мозга. Длина вен исследовалась приложением к ним лигатуры, которая впоследствии накладывалась на миллиметровую линейку. Диаметр вен измерялся зубомерным микрометром МКЦ- 0-25-0,001.
На первом этапе изучалась базальная вена и её притоки. Изучалась длина вены, диаметр в области истока, средней трети и устья, варианты впадения основных притоков. В области таламического участка базальной вены изучалось её расположение относительно зрительного тракта.
Исследовались малый и большой венозные круги основания головного
мозга.
После этого выполнялось рассечение головного мозга в горизонтальной плоскости на уровне боковых желудочков, и изучались внутренние мозговые вены (ВМВ): их длина, диаметр в области истока, средней трети и устья, количество и варианты впадения основных притоков.
Далее исследовалась длина и диаметр БМВ и её основные притоки. са 7,0 81а15оА.
са 7,0 81а15оА.
Нормальность распределения определялась на основе критерия Шапиро-Уилка.
Характеристика вариационных рядов для количественных признаков с непараметрическим распределением и данных с параметрическим распределением, ввиду малой их доли, представлена медианой (Ме) с межквартельным интервалом [Р25; Р75]. Значения средних величин отображались как Ме [Р25; Р75].
Описательная статистика для качественных признаков представлена в виде процентных долей и стандартной ошибки (М ± т %).
При сравнительном анализе трех независимых рядов непараметрических данных использовался критерий множественных сравнений Краскелла-Уоллеса, непараметрический критерий Манна-Уитни.
Для оценки связи между признаками применялся коэффициент ранговой корреляции Спирмена.
Значимость различий относительных показателей в группах наблюдения оценивали при помощи непараметрического критерия %2 Пирсона, точного критерия Фишера.
За критический уровень значимости при проверке статистических гипотез в исследовании принимался уровень, равный 0,05.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ
В ходе краниометрического исследования 120 трупов мужчин было выявлено 47 трупов с брахицефалической (39,1%), 40 с мезоцефапической (33,3 %), 33 долихоцефал и ческой (27,5 %) формой головы.
Выявлено, что передняя мозговая вена (ПМВ) встречалась непостоянно. Частота встречаемости ПМВ у трупов с разной формой головы представлена в табл. 2.
Таблица 2
Частота встречаемости передней мозговой вены у трупов мужчин _с разной формой головы, % (п = 120)__
Сторона Частота встречаемости передней мозговой вены М± ш Достоверность различий
Форма головы
Долихоцефал ич. (ш=33) Мезоцефал ич. (т=40) Брахицефалич (пэ=47)
слева 87,50 ± 5,22 90,0 ± 4,74 87,23 ± 4,86 -
справа 87,50 ± 5,22 87,50 ± 5,22 87,23 ± 4,86 -
Передняя соединительная вена наиболее редко определялась у долихоцефалов — в 27,50 ± 7,06 % случаев, у мезоцефалов наиболее часто — в 51,51 ± 8,69 % случаев, у брахицефалов — в 44,68 ± 7,25 % случаев.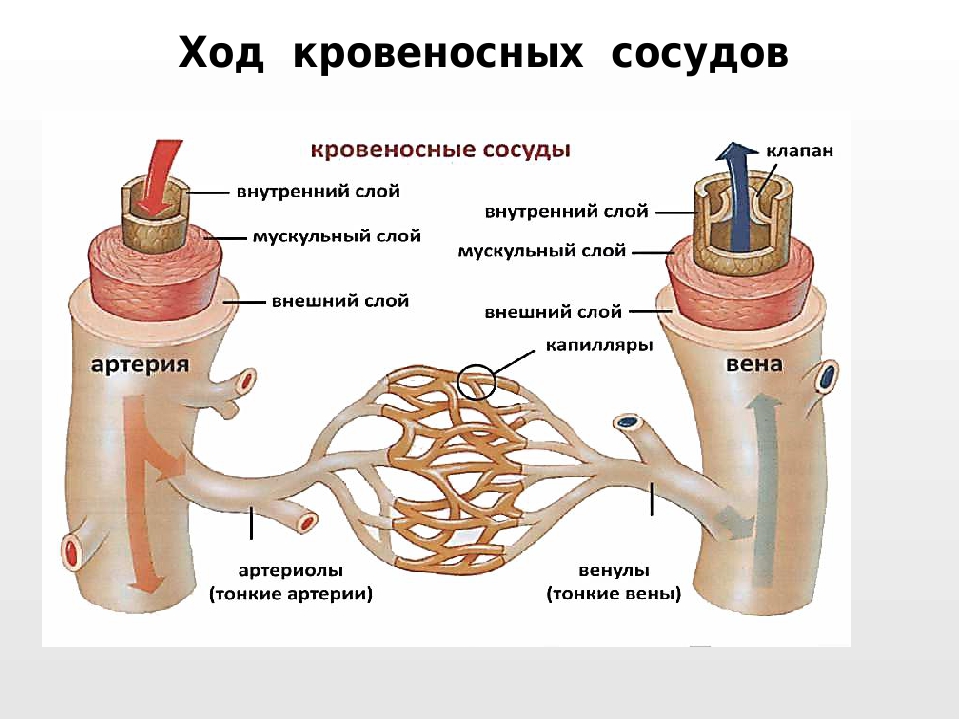
У брахицефалов длина ПМВ колебалась от 11 до 15 мм, у мезоцефалов от 12 до 16 мм, у долихоцефалов от 13 до 16 мм Средняя длина ПМВ трупов с разной формой головы представлена в табл. 3.
Таблица 3
Длина передней мозговой вены у трупов мужчин с разной _формой головы, мм (п = 120)___
Сторона Длина передней мозговой вены Me [Р 25 %; Р 75 %] Достоверность различий
Форма головы
Долихоцефалич. (П1=ЭЭ) Мезоцефалич. (П2=40) Брахицефалич. (пэ=47)
слева 14 [14; 14] 14 [13,5; 14] 13 [13; 13,5] pi-3<0,05 Р2-Э<0,05
справа 14 [14; 14] 14 [14; 14] 13 [12,5; 13] pi-3<0,05 Р2-З<0,05
Исходя из данных таблицы, длина передней мозговой вены у брахицефалов достоверно меньше в сравнении с долихоцефалами и мезоцефалами.
Диаметр передней мозговой вены колебался у брахицефалов от 0,63 до 1,35 мм, у мезоцефалов от 0,51 до 1,26 мм, у долихоцефалов от 0,51 до 1,02 мм. Средний диаметр передней мозговой вены у трупов с разной формой головы представлен в табл. 4.
4.
Таблиц» 4
Диямегр передней мозговой вены у трупов мужчин с разной _формой головы, мм (п = 120)__
Сторона Диаметр передней мозговой вены Me [Р 25 %; Р 75 %] Достоверность различий
Форма головы
Долихоцефал ич. (ni=33) Мезоцефалич. (П2=40) Брахицефалич. (пэ=47)
слепа 0,70 [0,66; 0,87] 0,81 [0,72; 0,90] 0,87 [0,78; 0,93] -
справа 0,78 [0.69; 0.93] 0,84 [0,78; 0.96] 0,87 [0,84; 1,02] -
Таким образом, достоверных отличий в диаметре передней мозговой вены у трупов с разной формой головы не выявлено.
Глубокая средняя мозговая вена (ГСМВ) встречалась с обеих сторон в 100% случаев. Длина глубокой средней мозговой вены колебалась у брахицефалов от 11 до 22 мм, у мезоцефалов — от 8 до 14 мм, у долихоцефалов — от 6 до 14 мм. Средние показатели длины глубокой средней мозговой вены у трупов с разной формой головы см. в табл. 5.
Таблица 5
Длина глубокой средней мозговой вены у трупов мужчин с разной
формой головы, мм (п = 120)
Сторона Длина глубокой средней мозговой вены Me [Р 25 %; Р 75 %] Достоверность различий
Форма головы
Долихоцефалия. (т=33) Мезоцефалич. (П2=40) Брахицефалич. (пз=47)
(т=33) Мезоцефалич. (П2=40) Брахицефалич. (пз=47)
слева 11 [10; 12] 11 [10; 12] 14 [13; 14] рьз<0,05 р2-з<0,05
справа 11 [11: 12] 12 [11; 13] 14 [13; 14] рьз<0,05 рг-з<0,05
Исходя из данных таблицы, у брахицефалов отмечалась наиболее длинная глубокая средняя мозговая вена (на 2-Змм длиннее) в сравнении с долихоцефалами и мезоцефалами.
Диаметр глубокой средней мозговой вены колебался от 0,6 до 1,4 мм. Средние значения диаметра глубокой средней мозговой вены у трупов с разной формой головы отражено в табл. 6.
Таблица 6
Диаметр глубокой средней мозговой вены у трупов мужчин _с разной формой головы, мм (п -120)__
Сторона Диаметр глубокой средней мозговой вены Ме [Р 25 %; Р 75 %] Достоверность различий
Форма головы
Долихоцефалия. (ni=33) Мезоцефал ич. (п2=40) Брахицефал ич. (пз=47)
слева 0,93 [0,811 1,08] 1,05 [0,93; 1,17] 1,05 [0,93; 1,17] -
справа 0,96 [0,81; 1.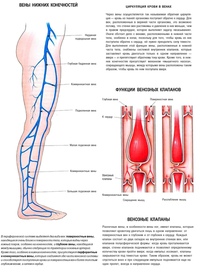 05] 0,96 [0.87; 1,02] 0,96 [0,84; 1,261 -
05] 0,96 [0.87; 1,02] 0,96 [0,84; 1,261 -
Достоверных различий в диаметре глубокой средней мозговой вены у трупов с разной формой головы не выявлено.
Выявлено, что вена обонятельного тракта (ВОТ) встречалась непостоянно (табл. 7).
Таблица 7
Частота встречаемости вены обонятельного тракта у трупов мужчин
с разной формой головы, % (п — 120)
Сторона Частота встречаемости вены обонятельного тракта М± m Достоверность различий
Форма головы
Долихоцефалич. (ni=33) Мезоцефалич. (т=40) Брахицефалич. (пэ=47)
слева 36,36 ± 8,37 32,50 ± 7,40 38,29 ± 7,09 -
справа 30,30 ± 7,99 25,00 ± 6,84 25,53 ± 6,36 -
Достоверных различий в частоте встречаемости ВОТ у трупов с разной формой головы не установлено.
Выявлено, что вена обонятельного тракта могла впадать в угол, образованный слиянием передней и глубокой средней мозговой веной, в переднюю мозговую вену и непосредственно в глубокую среднюю мозговую вену. Частота вариантов впадения вены обонятельного тракта в глубокие вены представлена в табл. 8.
Частота вариантов впадения вены обонятельного тракта в глубокие вены представлена в табл. 8.
Таблица 8
Частота вариантов впадения вены обонятельного траста у трупов мужчин с разной __ формой головы, % (п = 120)__
Место впадения Сторона Частота впадения вены обонятельного тракта М± m Достоверность различий
Форма головы
Долихоцефал. (ш=33) Мезоцефал. (п2=40) Брахицефал. (пз=47)
Угол перед, и глуб. средн. мозговой вены слева 41,67 ±8,58 46,15 ± 13,82 44,44 ± 4,78 -
справа 20,00 ±6,96 30,00 ± 14,49 16,67 ± 10,75 -
Передняя мозговая вена слева 8,33 ±4,81 15,39 ± 10,00 16,67 ±8,78 -
справа 40,00 ± 8,52 10,00 ± 9,48 16,67 ± 10,75 -
Глубок, средн. мозговая вена слева 50,00 ± 8,70 38,46 ± 13,49 38,89 ± 11,49 -
справа 40,00 ± 8,52 60,00 ± 15,49 66,66 ± 13,60 -
Таким образом, как видно из данных таблицы, отмечается большая вариабельность мест впадения вены обонятельного тракта в глубокие вены головного мозга вне зависимости от формы головы.
Установлено, что предталамический отдел базальной вены формировался на уровне переднего продырявленного вещества путём слияния передней мозговой вены и глубокой средней мозговой вены. В тех случаях, когда передняя мозговая вена отсутствовала, базальная вена была продолжением глубокой средней мозговой вены. Частота встречаемости вариантов формирования базальной вены представлена в табл. 9
Таблица 9
Частота встречаемости вариантов формирования базальной вены у трупов мужчин с
_ )азной формой головы, % (п= 120)
Вариант формирования базальных вен Сторона Частота встречаемости вариантов формирования базальных вен № т Достоверность различий
Форма головы
Долихоцефал. (т=33) Мезоцефал. (п2=40) Брахицефал. (пз=47)
Слияние перед, и глуб. средн. мозговой вены слева 90,91 ± 5,06 90,00 ± 4,74 87,23 ± 4,86 -
справа 90,91 ± 5.06 87,50 ± 5,22 87,23 ± 4,86 -
Продолжение средней мозговой вены слева 9,09 ± 5,06 10, 00 ± 4,74 12,77± 4,86 -
справа 9,09 ± 5,06 12,50± 5,22 12,77± 4,86 -
Установлено, что межножковые вены определялись с обеих сторон в 80-100% случаев, в оставшихся случаях межножковые вены определялись только с одной стороны.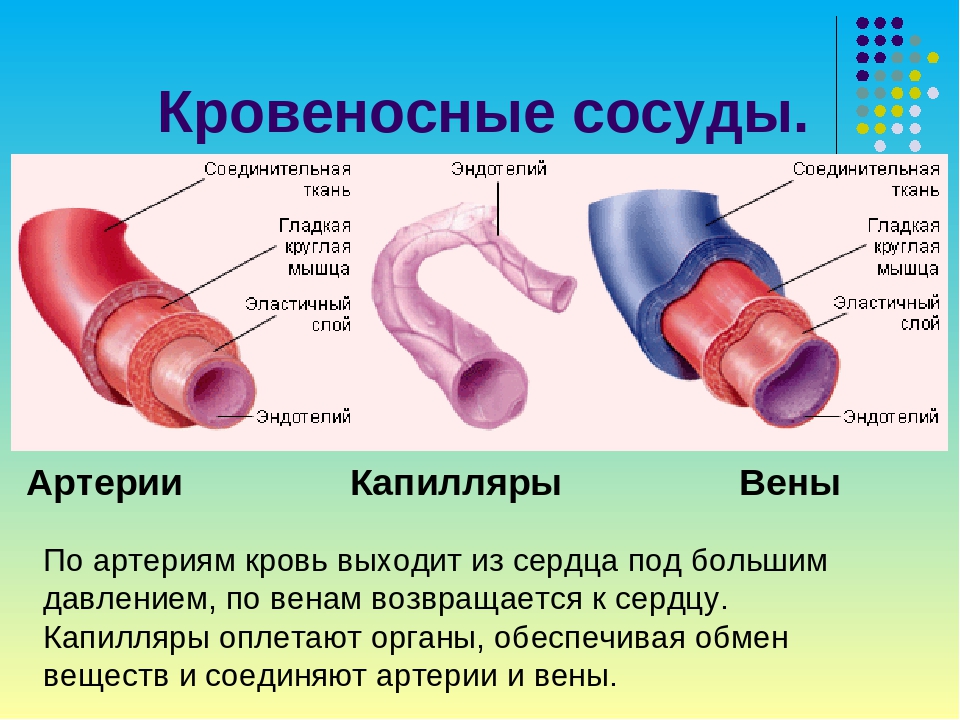 Частота встречаемости межножковых вен у трупов с разной формой головы отражена в табл. 10.
Частота встречаемости межножковых вен у трупов с разной формой головы отражена в табл. 10.
Таблица 10
Частота встречаемости межножковых вен у трупов мужчин с разной
формой головы, % (п= 120)
Сторона Частота встречаемости межножковых вен М± ш Достоверность различий
Форма головы
Долихоцефал ич. (т=33) Мезоцефал ич. (П2=40) Брахицефал ич. (пз=47)
слепа 90,91 ±5,06 100 87,23 ± 4,86 -
справа 84,85 ± 6,24 97,5 ± 2,46 82,98 ± 5,48 -
Достоверных различий в частоте встречаемости межножковых вен у трупов с разной формой головы не установлено.
Выявлено неодинаковое расположение таламического отдела базальной вены относительно зрительного тракта. Установлено два положения базальной вены:
1) базальная вена находится на зрительном тракте;
2) базальная вена находится медиальнее зрительного тракта. Частота разных вариантов расположения базальной вены относительно зрительного тракта у трупов с разной формой головы зафиксирована в табл. 11.
11.
Таблица 11
Частота встречаемости вариантов расположения базальной вены относительно зрительного тракта у трупов мужчин с разной формой головы, % (п = 120)
Расположение базальной вены Сторона Частота встречаемости вариантов расположения базальной вены относительно зрительного тракта М ± ш % Достоверн. различий
Форма головы
Долихоцеф. (т=ЭЗ) Мезоцеф. (ш=40) Брахицеф. (пэ=47)
Мсдиальнсе зрит, тракта Слева 72,73 ± 7,75 80,00 ± 6,00 68,09 ± 6,79 -
Справа 90,91 ±5,06 85,00 ± 5,64 70,22 ± 6,67 -
На зрительном тракте Слева 24,24 ± 7,46 17,50 ±6,00 27,66 ± 6,52 -
Справа 6,06 ±4.15 12,50 ±5,22 23,40 ±6,17 -
Отсутствие телам ич. отдела базальной вены Слева 3,03 ± 2,98 2,50 ±2,46 4,25 ± 2,94 -
Справа 3,03 ± 2,98 2,50 ± 2,46 6,38 ± 3,56 -
Таким образом, для базальной вены при всех формах головы наиболее характерно медиальное расположение по отношению к зрительному тракту.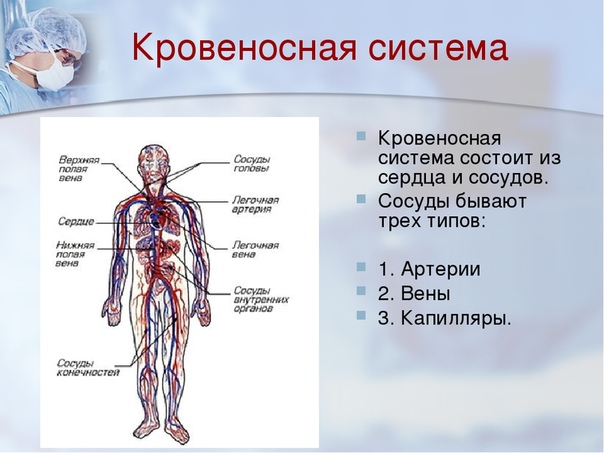
Установлено, что медиальная затылочная вена наблюдалась непостоянно: у брахицефалов слева в 48,93 ± 7,29 % случаев, справа — в 48,93 ± 7,29 % случаев, у мезоцефалов слева — в 60,00 ± 7,27 % случаев, справа — в 50,00 ± 7,9 % случаев, у долихоцефалов слева — в 54,54 ± 8,66 % случаев, справа — в 51,51 ± 8,69 % случаев. Таким образом, у трупов со всеми формами головы, медиальная затылочная вена отсутствовала примерно в половине случаев.
Установлено, что длина базальной вены колебалась от 40 до 46 мм. Длина базальной вены у трупов с разной формой головы представлена в табл. 12.
Таблица 12
Длина базальной вены у трупов мужчин с разной формой головы, мм (п = 120)
Сторона Длина базальной вены Ме [Р 25 %; Р 75 %] Достоверность различий
Форма головы
Долихоцефал. (ш=33) Мезоцефал. (п2=40) Брахицефал. (ш=47)
слева 42 [41; 43] 40 [38; 41] 39 [39; 41] р|-з<0,05 Р2-Э<0,05
справа 42 [40; 44] 39 [38; 41] 40 [39; 41] р1-э<0,05 Р2-з<0,05
Из данных, представленных в таблице, видно, что долихоцефалы имели наибольшую длину вены, в сравнении с брахицефалами и мезоцефалами (на 2-3 мм длиннее). Таким образом, долихоцефалы, имеющие наибольшие (в сравнении с другими формами головы) продольные размеры головы, имеют наиболее длинную базальную вену, имеющую направление близкое к продольному.
Таким образом, долихоцефалы, имеющие наибольшие (в сравнении с другими формами головы) продольные размеры головы, имеют наиболее длинную базальную вену, имеющую направление близкое к продольному.
Диаметр базальной вены был неодинаковым в начальном, среднем и нижнем отделах (в месте впадения в большую мозговую вену). Вне зависимости от формы головы диаметр начального БВ отдела колебался от 0,24 до 2,4 мм, среднего отдела от 0,7 до 3,04 мм, нижнего отдела от 1,3 до 4,64 мм. Средний диаметр разных отделов базальной вены у трупов с разной формой головы представлен в табл. 13.
Таблица 13
Диаметр базальной вены у трупов мужчин с разной _формой головы, мм (п — 120)_
Отдел базальной вены Диаметр базальной вены Ме [Р 25 %; Р 75 %]
Сторона Форма головы Достоверность различий
Долихоцефал. (т=33) Мезоцефал. (п2=40) Брахицефал. (т=47)
Исток Слева 0,84 [0,78; 0,91] 0,80 [0,74; 1] 1,02 [0,8; 1,38] -
Справа 0,80 [0,74; 0,88] 0,84 [0,68; 1,22] 0,98 [0,79; 1,24] -
Середина Слева 1,30 [1,16; 1,48] 1,56 [1,42; 1,64] 1,94 [1,74; 2,2] -
Справа 1,36 [1,16; 1,46] 1,57 [1,34; 1,83] 1,84 [1,52; 2,24] -
Усгьс Слева 2,70 [3,32; 3,06] 3,04 [2,28; 3,39] 3,02 [2,8; 3,44] -
Справа 2,84 [1,96; 3,04] 3,13 [2,1; 3,33] 2,92 [2,76; 3,08] -
Исходя из данных таблицы, диаметр базальной вены увеличивается от начального отдела до нижнего в среднем на 2 мм. При этом значимых различий в диаметре разных отделов базальной вены у трупов с разной формой головы не выявлено.
При этом значимых различий в диаметре разных отделов базальной вены у трупов с разной формой головы не выявлено.
Исследование показало, что базальная вена могла впадать непосредственно в большую мозговую вену, либо во внутреннюю мозговую вену в её нижней трети (табл. 14).
Таблица 14
Частота встречаемости вариантов впадения баэальных вен у трупов мужчин с разной формой головы, % (п = 120)
Место впадения базальной вены Частота встречаемости вариантов впадения баэальных вен М± ш Достоверность различий
Сторона Форма головы
Долихоцеф. (т=33) Мезоцеф (п2=40) Брахицеф (пэ=47)
Внутренняя мозгов, вена Слева 33.33 ± 8,20 30,00 ±7,24 25,53 ± 6,36 -
Справа 33,33 ± 8,20 27,50 ± 7,06 25,53 ± 6,36 -
Большая мозгов, вена Слева 66,67 ± 8,20 70,00 ± 7,24 74,47 ± 6,36 -
Справа 66.67 ± 8,20 72,5 ± 7,06 74,47 ± 6,36 -
Из данных, представленных в таблице, следует, что для базальной вены наиболее характерно впадение непосредственно в большую мозговую вену, при этом примерно в трети случаев при всех формах головы отмечалось впадение базальной вены во внутреннюю мозговую вену.
Выявлено, что внутренняя мозговая вена встречается в 100% случаев и при всех формах головы образуется путём слияния таламостриарной вены и вены прозрачной перегородки.
Установлено, что вена прозрачной перегородки представлена рассыпным и магистральным типами (табл. 15).
Таблица 15
Частота встречаемости типов вены прозрачной перегородки у трупов мужчин с разной формой головы, % (п = 120)
Тип вены прозрачной перегород. Частота встречаемости типов вены прозрачной перегородки М±т Достоверность различий
Сторона Форма головы
Долихоцефал. (ш=33) Мезоцефал. (п2=40) Брахицефал. (пз=47)
Магистральный Слева 75,75 ± 7,46 72,50 ± 7,06 68,08 ± 6,79 -
Справа 78,78 ±7,11 77,50 ± 6,60 74,47 ± 6,36 -
Рассыпной Слева 24,25 ± 7,46 27,50 ± 7,06 31,98 ±6,79 -
Справа 21,22 ± 7,11 22,50 ± 6,60 25,53 ± 6,36 -
Таким образом, для ВПП наиболее характерен магистральный тип, встречающийся при всех формах головы в 70-80% случаев.
Постоянным притоком внутренней мозговой вены являлась верхняя ворсинчатая вена, которая определялась с обеих сторон в 100% случаев. Вариантная анатомия верхней ворсинчатой вены представлена разными уровнями её впадения во внутреннюю мозговую вену, либо в таламостриарную вену (табл. 16).
Таблица 16
Частота встречаемости вариантов впадения верхней ворсинчатой вены у трупов мужчин с разной формой головы, % (п = 120)
Место впадения Частот встречаемости вариантов впадения верхней ворсинчатой вены М± т Достоверность различий
Сторона Форма головы
Долихоцеф. (п=33) Мезоцеф. (п=40) Брахицеф. (п=47)
Вну-трен. мозг, вена в/3, с/3 Слева 24,24 .-ь 7,45 27,50 ± 7,06 27,65 ± 6,52 -
Справа 39,39 ± 8,50 35,00 ± 7,54 38,30 ± 7,09 -
Внутренняя мозг, вено на уровне межжелуд. отв. Слева 63,63 ± 8,37 62,50 ± 7,65 61,70 ±7,09 -
Справа 57,57 ± 8,60 60,00 ± 7,74 57,45 ±7,21 -
Тапамостриарная вена Слева 12,13 ±5,68 10,00 ±4,74 10,65 ±4,49 -
Справа 3,04 ± 2,98 5,00 ±3,44 4,25 ± 2,94 -
Исходя из данных таблицы, при всех формах головы верхняя ворсинчатая вена чаще впадала во внутреннюю мозговую вену на уровне межжелудочкового отверстия.
Задняя вена бокового желудочка (ЗВБЖ) определялась с обеих сторон в 100 % случаев. При этом она могла впадать во внутреннюю мозговую вену и в большую мозговую вену (табл. 17).
Таблица 17
Частота встречаемости вариантов впадения задней вены бокового желудочка у трупов мужчин с разной формой головы, % (п = 120)
Место впадения задней вены бокового желудочка Частота встречаемости вариантов впадения задней вены бокового желудочка М± т
Сторона Форма головы Достоверность различий
Долихоцефал. (п.-ЗЗ) Мезоцефал. (п2=40) Брахицефал. (пз=47)
Внутренняя мозговая вена Слева 84,84 ± 6,24 85,00 ± 5,64 87,23 ± 4,86 -
Справа 87,87 ± 5,68 92,50 ±4,16 85,10 ±5,19 -
Большая мозговая вена Слева 15,16 ±6,24 15,00 ± 5,64 12,77 ± 4,86 -
Справа 12,13 ±5,68 7,50 ±4,16 14,90± 5,19 -
Таким образом, при всех формах головы задняя вена бокового желудочка впадала во внутреннюю мозговую вену в 85-90 % случаев.
Исследование показало, что задняя вена бокового желудочка была представлена двумя типами: магистральным и рассыпным (табл. 18).
Таблица 18
Частота встречаемости типов задней вены бокового желудочка у трупов мужчин с разной формой головы, %, (п = 120)
Тип задней вены бокового желудочка Частота встречаемости типов задней вены бокового желудочка М±ш
Сторона Форма головы Достоверность различий
Долихоцефал. (41=33) Мезоцефал. (ш=40) Брахицефал. (ю=47)
Магистральный Слева 87,87 ± 5,68 82,50 ± 6,00 89,36 ± 4,49 -
Справа 84,84 ± 6,24 80,00 ± 6,32 82,97 ± 5,48 -
Рассыпной Слева 12,13 ±5,68 17,50 ±6,00 10,64 ±4,49 -
Справа 15,16 ±6,24 20,00 ± 6,32 17,03 ±5,48 -
Исходя из данных таблицы, при всех формах головы наиболее характерен магистральный тип задней вены бокового желудочка (83-90% случаев).
Длина внутренней мозговой вены колебалась от 30 до 53 мм. Средние показатели длины внутренней мозговой вены у трупов с разной формой головы представлены в табл. 19.
19.
Таблиц» 19
Длина внутренней мозговой вены у трупов мужчин с разной _формой головы, мм (п = 120__
Сторона Длина внутренней мозговой вены Ме [Р 25 %; Р 75 %) Достоверность различий
Форма головы
Долихоцсфалич. (ш=33) Мезоцефал ич. (П2=40) Брахицефалич. (пэ=47)
слева 44 [43; 44] 4) [40; 42] 36 135; 37] р1-:<0,05 рг-з<0,05 р1-з<0,05
справа 44 [43; 46] 41 [40; 42] 35 [34; 37] р1-2<0.05 рг-з<0,05 р|-з<0,05
Из данных, представленных в таблице, видно, что долихоцефалы, имеющие наибольшие продольные размеры головы имеют и наибольшую длину внутренней мозговой вены (на 3-8 мм. длиннее по сравнению с мезоцефалами и брахицефалами), также имеющей продольное направление.
Диаметр внутренней мозговой вены был неодинаковым на всем ее протяжении. В начальном и среднем отделах диаметр колебался в пределах 1,7-2,5 мм, в области впадения в большую мозговую вену диаметр колебался в пределах 4—4,4 мм. Средние показатели среднего диаметра разных отделов внутренней мозговой вены у трупов с разной формой головы отражены в табл. 20.
Средние показатели среднего диаметра разных отделов внутренней мозговой вены у трупов с разной формой головы отражены в табл. 20.
Таблица 20
Диаметр внутренней мозговой вены у трупов мужчин с разной _формой головы, мм (п =120)___
Отдел внутренней мозговой вены Диаметр внутренней мозговой вены Ме [Р 25 %; Р 75 %] Достоверность различий
Сторона Форма головы
Долихоцефал. (п=33) Мезоцефал. (п=40) Брахицефал. (п=47)
Исток Слева 1,94 [1,72; 2,08] 2,21 [1,96; 2.34] 2,48 [2,34; 2,60] -
Справа 1,86 [1,74; 2,06] 1,96 [1,88; 2,14] 2,36 [2,20; 2,50] -
Середина Слева 2,54 [2,44; 2,64] 2,64 [2,47: 2,75] 2,96 [2,84; 3,20] -
Справа 2,50 [2,32; 2,64] 2,46 [2,24; 2,50] 2,84 [2,70; 3,06] -
Устье Слева 4,25 [3,96; 4,46] 4,24 [4,08; 4,43] 4,30 [4,14; 4,42] -
Справа 4,20 [3,96; 4,24] 4,36 [4,20; 4,47] 4,00[3,89; 4,21] -
Из данных таблицы видно, что диаметр внутренней мозговой вены от истока до устья увеличивается в среднем на 2-2,5 мм. При этом достоверных
При этом достоверных
отличий в диаметре разных отделов внутренней мозговой вены у трупов с разной формой головы не выявлено.
Большая мозговая вена определялась в 100 % случаев при всех формах головы. Количество притоков большой мозговой вены колебалось от 5 до 13, при этом у брахицефалов — 10 [8; 10], у мезоцефалов — 8,5 [7; 10], у долихоцефалов — 10 [8; 10].
Передневерхняя мозжечковая вена (ПВМВ) являлась постоянным притоком БМВ и встречалась в 100% случаев. ПВМВ была представлена двумя типами: магистральным и рассыпным (табл. 21)
Таблица 21
Частота встречаемости типов нередневерхней мозжечковой вены у трупов мужчин с
разной формой головы, % (п =120)
Тип передне- верхней мозжечковой вены Частота встречаемости типов передневерхней мозжечковой вены М± ш Достоверность различий
Форма головы
Долихоцефал ич. (т=33) Мезоцефалич. (п2=40) Брахицефалии .(пэ=47)
Магистральный 69,69 ± 8,00 70,00 ± 7,24 70,21 ±6,67 -
Рассыпной 30,31 ±8,00 30,00 ± 7,24 29,79 ± 6,67 -
Таким образом, магистральный тип передневерхней мозжечковой вены встречался в два раза чаще рассыпного при всех формах головы.
Задняя верхняя вена мозолистого тела (ЗВВМТ) определялась у брахицефалов в 65,95 ±6,91% случаев, у мезоцефалов — в 62,5 ± 7,75% случаев, у долихоцефалов — в 51,51 ±8,69% случаев. Установлено, что ЗВВМТ могла впадать в разные глубокие вены головного мозга (табл. 22).
Таблица 22
Частота встречаемости вариантов впадения задней верхней вены мозолистого тела у трупов мужчин с разной формой головы, % (п =120)
Место впадения задней верхней вены мозолистого тела Частота встречаемости вариантов впадения задней верхней вены мозолистого тела М± т Достоверность различий
Форма головы
Долихоцефал.( ш=33) Мезоцефал. (п2=40) Брахицефал. (пэ=47)
Большая мозговая вена 47,06 ± 12,10 64,00 ± 9,60 74,20 ± 7,86 р|-з<0,05
Медиальн. затылочная вена 23,53 ± 10,29 16,00 ±7,33 12,90 ± 6,02
Базальная вена 29,41 ±11,05 20,00 ± 8,00 12,90 ±6,02
Из данных таблицы видно, что задняя верхняя вена мозолистого тела наиболее часто впадала непосредственно в большую мозговую вену.
Вена эпифиза являлась постоянным притоком большой мозговой вены, она встречалась в 100% случаев и была представлена двумя типами: магистральным — с одной веной и рассыпным — с двумя-тремя венами (табл. 23).
Таблица 23
Частота встречаемости типа вен эпифиза у трупов мужчин с разной __формой головы, % (п =120)__
Тип вен эпифиза Частота встречаемости типа вен эпифиза М± ш Достоверность различий
Форма головы
Долихоцефалич. (т=33) Мезоцефалич. (п2=40) Брахицефал ич. (пэ=47)
Магистральный 84,85 ± 6,24 85 ± 5.64 74,46 ± 6,36 -
Рассыпной 15,15 ± 6,24 15 ±5,64 25,53 ± 6,36 -
Таким образом, при всех формах головы наиболее часто (75-85% случаев) встречается 1 вена эпифиза.
Длина большой мозговой вены колебалась от 4 мм до 22 мм. Показатели длины большой мозговой вены у трупов с разной формой головы представлены в табл. 24.
Таблица 24
Длина большой мозговой вены у трупов мужчин с разной _формой головы, мм (л =120)_
Длина большой мозговой вены Ме [Р 25 %; Р 75 %] Достоверность различий
Форма головы
Долихоцефалич. (ш=33) Мезоцефалич. ((12=40) Брахицефалия (пз=47)
14 113; 15] 13 [12; 14] 11 [9; 12] р|-2<0,05 р2-л<0,05 рм<0,05
Из данных таблицы видно, что, брахицефалы имели достоверно наименьшую длину БМВ (на 2-3 мм короче) в сравнении с долихоцефалами и мезоцефалами.
Диаметр большой мозговой вены колебался от 5 до 12 мм. Средние показатели диаметра большой мозговой вены у трупов с разной формой головы даны в табл. 25.
Таблица 25
Диаметр вены большой мозговой вены у трупов мужчин с разной
формой головы, мм (п=|20)
Диаметр большой мозговой вены Ме [Р 25 %; Р 75 %] Достоверность различий
Форма головы
Долихоцефалич. (11=33) Мезоцефалич. (т=40) Брахицефал ич. (пз=47)
6,7 [6,4; 7,2] 7,5 [6,95; 8,05] 8,4 [8; 8,8] р1-2<0,05 р|-з<0,05 P2.K0.05
Исходя из данных таблицы, диаметр большой мозговой вены оказался наибольшим у брахицефалов (на 1-2 мм больше), в сравнении с долихоцефалами и мезоцефалами.
Таким образом, брахицефалы имели наиболее короткую, но широкую большую мозговую вену, а долихоцефалы — наиболее длинную и узкую.
Установлено, что замкнутый большой венозный круг основания мозга встречается у брахицефалов в 44,68 ± 7,25 % случаев, у долихоцефалов — в 51,51 ± 8,69 % случаев, у мезоцефалов — в 27,50 ± 7,06 % случаев, т. е. у мезоцефалов почти в два раза реже (в сравнении с брахицефалами и долихоцефалами) наблюдался замкнутый большой венозный круг.
В отличие от большого венозного круга, замкнутый малый венозный круг отличается относительным постоянством при всех формах головы: у брахицефалов в 70,21 ± 6,32 % случаев, у долихоцефалов — в 75,75 ± 7,46 % случаев, у мезоцефалов — в 97,50 ± 2,46 % случаев.
Проведён корреляционный анализ между длиной, диаметром глубоких вен мозга и индексом головы (табл. 26).
Таблица 26
Показатели корреляционного анализа между длиной и диаметром глубоких вен головного мозга и индексом головы
Параметры Коэффициент корреляции
слева справа
Длина передней мозговой вены -0,5866 -0,5682
Диаметр передней мозговой вены 0,2982 0,3251
Длина глубокой средней мозговой вены 0,6970 0,6807
Диаметр глубокой средней мозговой вены 0,2211 0.1285
Длина базальной вены -0,4216 -0,3449
Диаметр базальной вены в верхней трети 0,2693 0.2638
Диаметр базальной вены в средней трети 0.5869 0.4783
Диаметр базальной вены в нижней трети 0.2003 0.1210
Длина внутренней мозговой вены -0,8465 -0,8265
Диаметр внутренней мозговой вены в верхней трети 0.5593 0,4844
Диаметр внутренней мозговой вены в средней трети 0,5140 0,3921
Диамегр внутренней мозговой вены в нижней трети 0,2389 0,2210
Длина большой мозговой вены -0,6759
Диаметр большой мозговой вены 0,6675
Как видно из данных, представленных в табл. 26, имеются корреляционные зависимости только между показателями длины некоторых глубоких мозговых вен и индексом головы, в то время как корреляционной связи между диаметром глубоких мозговых вен и индексом головы не установлено. Выявлена связь средней силы между индексом головы и длиной ГСМВ (0,68-0,69). Таким образом, при максимальных значениях ИГ (у брахицефалов), увеличивается длина ГСМВ, которая имеет поперечное направление. Выявлены обратные сильные связи и обратные связи средней силы между показателями ИГ и длиной продольно идущих вен (БВ, ВМВ,
БМВ). То есть при минимальных значениях ИГ (у долихоцефалов) отмечаются наибольшие показатели данных вен, имеющих продольное направление.
При сравнительном анализе диаметров внутренней мозговой вены и базальной вены в месте впадения в большую мозговую вену выявлено, что преобладание диаметра ВМВ над диаметром БВ в 1,5-3 раза встречалось (1)с обеих сторон, (2) только справа или (3) только слева. В табл. 27 представлена частота преобладания диаметра внутренней мозговой вены над базальной веной у трупов с разной формой головы.
Таблиц« 27
Частота преобладания диаметра внутренней мозговой вены над диаметром базальной вены у трупов мужчин с разной формой головы, % (п =120)
Сторона Частота встречаемости преобладания диаметра внутренней мозговой вены над диаметром базальной вены М± ш Достоверность различий
Форма головы
Долихоцефалии. (ш=ЗЭ) Мезоцефалич. (п2=40) Брахицефалии. (ш=47)
слева 30,31 ±7,99 30,00 ± 7,24 21,27 ±5,96 -
справа 33,33 ± 8,20 30,00 ± 7,24 12,77 ±4,86 рю<0,05
С обеих сторон преобладание диаметра внутренней мозговой вены в полтора и более раза над диаметром базальной вены определялось у брахицефалов в 8,51 ± 4,07 % случаев, у мезоцефалов — в 17,50 ± 6,00 % случаев, у долихоцефалов — в 15,15 ±6,24% случаев. Таким образом, реже диаметр ВМВ преобладал над диаметром БВ у брахицефалов по сравнению с долихоцефалами и мезоцефалами.
В остальных случаях наблюдались относительно равный диаметр внутренней мозговой вены и базальной вены. Случаев преобладания диаметра вены БВ над диаметром ВМВ не установлено.
Таким образом, вне зависимости от формы головы в 12-40% случаев имеются анатомические предпосылки для преобладания дорсального пути венозного оттока от подкорковых структур головного мозга над базальным. В оставшихся случаях — 60-88 % случаев имеются анатомические предпосылки для равноценного — базапьного и дорсального венозного оттока.
Исследование 6 препаратов головного мозга, изъятого у лиц с брахицефальной формой головы, умерших от внутримозгового кровоизлияния, показало, что данные по длине и диаметру глубоких мозговых вен находятся в пределах значений этих же показателей, полученных при исследовании препаратов головного мозга, изъятого у мужчин, умерших от причин, не связанных с поражением центральной нервной системы с брахицефальной формой головы.
ВЫВОДЫ
1. Вариантная анатомия глубоких вен головного мозга мужчин соответствует формам головы.
2. Долихоцефалы характеризуются наибольшей длиной глубоких мозговых вен, имеющих продольное направление (длина базальной вены -42 мм, длина внутренней мозговой вены — 44 мм) в сравнении с брахицефалами (длина базальной вены — 39 мм, длина внутренней мозговой вены — 35-36 мм) и мезоцефалами (длина базальной вены слева — 40 мм, длина внутренней мозговой вены — 41 мм). Брахицефалы имеют наибольшую длину вен, располагающихся поперечно (длина глубокой средней мозговой вены — 14 мм) в сравнении с долихоцефалами (длина глубокой средней мозговой вены — 11 мм) и мезоцефалами (длина глубокой средней мозговой вены — 11 мм).
3. Диаметр внутренней мозговой вены и базальной вены при всех формах головы увеличивается от начальных отделов до места впадения в большую мозговую вену на 2-3 мм.
4. Количество притоков глубоких мозговых вен, их формирование и впадение вариабельно и не зависит от формы головы.
5. Замкнутый большой венозный круг головного мозга встречается с разной частотой у трупов с различной формой головы: у брахицефалов -44,68 ± 7,25 % случаев, у долихоцефалов — 51,51 ± 8,69 % случаев, у мезоцефалов 27,50 ± 7,06 % случаев. Замкнутый малый венозный круг встречается относительно постоянно при всех формах головы: у брахицефалов — 70,21 ±6,32% случаев, у долихоцефалов — 75,75 ± 7,46 % случаев, у мезоцефалов — 97,50 ± 2,46 % случаев.
6. Преобладание дорсального пути венозного оттока от подкорковых структур головного мозга (диаметр внутренней мозговой вены в 1,5-3 раза превышает диаметр базальной вены) имеют брахицефалы слева — в 21,27 ± 5,96 %, справа — в 12,77 ± 4,86 % случаев, мезоцефалы слева и справа — в 30,00 ± 7,24 % случаев, долихоцефалы слева — в 30,31 ± 7,99 %, справа — в 33,33 ± 8,20 % случаев. В остальных случаях имеются равноценные базапьный и дорсальный пути венозного оттока от подкорковых структур головного мозга.
7. При брахицефальной форме головы длина и диаметр глубоких вен головного мозга у мужчин, умерших от внутримозговых кровоизлияний, не отличается от длины и диаметра глубоких мозговых вен у мужчин с брахицефальной формой головы, умерших от причин, не связанных с поражением центральной нервной системы.
ПРАКТИЧЕСКИЕ РЕКОМЕНДАЦИИ
1. Выявленные особенности анатомии глубоких вен головного мозга с учётом формы головы должны учитываться нейрохирургами при оперативных вмешательствах на основании головного мозга и в полости
боковых и третьего желудочков. Исходя из формы головы пациента, нейрохирург в предоперационный период с определенной долей вероятности может предположить особенности венозной архитектоники у каждого конкретного пациента.
2. Полученные данные по вариантам анатомии глубоких вен головного мозга у трупов с разной формой головы могут быть использованы при интерпретации данных МСКТ-ангиографии и МРТ-ангиографии (дифференцировки вен от артерий, отличие патологических сосудов от вариантов ангиоархитектоники).
СПИСОК РАБОТ, ОПУБЛИКОВАННЫХ ПО ТЕМЕ ДИССЕРТАЦИИ
1. Евсеев, A.B. Вариантная анатомия вены Розенталя у трупов с разной формой черепа / П. А. Самотесов, П. Г. Шнякин, А. В. Евсеев [и др.] // Врач-аспирант. — Воронеж, 2013. — Т. 56, № 1.2.-С. 285-289.
2. Евсеев, А. В. Особенности венозного оттока от подкорковых структур головного мозга в норме и у лиц, умерших от геморрагического инсульта / П. Г. Шнякин, П. А. Самотесов, А. В. Евсеев [и др.] // В мире научных открытий (проблемы науки и образования). — Красноярск, 2013. — Т. 39, №3.3.-С. 123-137.
3. Евсеев, А. В. Варианты строения артериального и венозного кругов основания головного мозга у лиц с разной формой черепа // П. Г. Шнякин, П. А. Самотесов, А. В. Евсеев [и др.] // Медицина и образование в Сибири : сетевое научное издание. — 2013. — № 2. — Режим доступа http://ngmu.ru/cozo/mos/article/text full.php?id= 1083
4. Евсеев, A.B. Особенности строения глубоких вен головного мозга в норме и у лиц, умерших от геморрагического инсульта / А. В. Евсеев, П. А. Самотесов, П. Г. Шнякин [и др.] // Сборник тезисов XII всероссийской конференции «Поленовские чтения». — Санкт-Петербург, 2013. — Т. V. -С. 131-132.
5. Евсеев, A.B. Вариантная анатомия внутренней мозговой вены у трупов с разной формой черепа / П. А. Самотёсов. П. Г. Шнякин, А. В. Евсеев [и др.] // Медицинская наука и образование Урала. — 2013. -№ 2. — С. 81-83.
6. Евсеев A.B. Вариантная анатомия вены Галена у трупов с разной формой головы / А.В.Евсеев, П. Г. Шнякин, П. А. Самотесов [и др.] // Международный научно-исследовательский журнал: Сборник статей XVII заочной научной конференции «Research Journal of International Studies». -Екатеринбург , 2013. — Т. 14, № 7. Часть 5. — С. 35-36.
7. Евсеев A.B. Корреляционный анализ между формой головы и длиной и диаметром глубоких вен головного мозга человека / A.B. Евсеев, П.Г. Шнякин., И.Е. Ермакова [и др.] // Сборник трудов IX международной научно-практической конференции «Динамика современной науки». -София, 2013. — Т. 9. — С. 84-87.
Подписано в печать 10.09.13. Формат 60×84 ‘/16. Усл. печ. л. 1,5. Бумага офсетная. Тираж 100 экз. Заказ 9-127
Отпечатано в типографии ИП Азарова H.H., т. 295-03-40
1 J — 1 2 О 9 i
2013115237
2013115237
Структура и функции кровеносных сосудов
Структура кровеносного сосуда
Кровеносные сосуды — это гибкие трубки, по которым кровь, кислород, питательные вещества, вода и гормоны переносятся по всему телу.
Цели обучения
Различать строение артерий, вен и капилляров
Основные выводы
Ключевые моменты
- Кровеносные сосуды состоят из артерий, артериол, капилляров, венул и вен.Сети сосудов направленно и регулируемо доставляют кровь ко всем тканям.
- Артерии и вены состоят из трех слоев ткани.
- Самый толстый внешний слой сосуда (адвентициальная оболочка или внешняя оболочка) состоит из соединительной ткани.
- Средний слой (tunica media) толще и содержит больше сократительной ткани в артериях, чем в венах. Он состоит из расположенных по кругу эластичных волокон, соединительной ткани и гладкомышечных клеток.
- Внутренний слой (tunica intima) — самый тонкий слой, состоящий из одного слоя эндотелия, поддерживаемого субэндотелиальным слоем.
- Капилляры состоят из единого слоя эндотелия и связанной соединительной ткани.
Ключевые термины
- tunica intima : Самый внутренний слой кровеносного сосуда.
- tunica externa : Самый внешний слой кровеносного сосуда.
- капилляр : любой из мелких кровеносных сосудов, соединяющих артерии с венами.
- tunica media : Средний слой кровеносного сосуда.
- анастомоз : соединение между кровеносными сосудами.
Кровеносные сосуды — ключевые компоненты системного и легочного кровообращения, которые распределяют кровь по всему телу. Есть три основных типа кровеносных сосудов: артерии, которые несут кровь от сердца, разветвляются на более мелкие артериолы по всему телу и в конечном итоге образуют капиллярную сеть. Последний способствует эффективному химическому обмену между тканью и кровью.Капилляры, в свою очередь, сливаются в венулы, а затем в более крупные вены, ответственные за возврат крови к сердцу. Стыки между сосудами называются анастомозами.
Артерии и вены состоят из трех отдельных слоев, в то время как капилляры гораздо меньшего размера состоят из одного слоя.
Туника Intima
Внутренний слой (tunica intima) — самый тонкий слой, образованный из единого непрерывного слоя эндотелиальных клеток и поддерживаемый субэндотелиальным слоем соединительной ткани и поддерживающих клеток.В более мелких артериолах или венулах этот субэндотелиальный слой состоит из одного слоя клеток, но может быть намного толще в более крупных сосудах, таких как аорта. Внутренняя оболочка окружена тонкой мембраной, состоящей из эластичных волокон, идущих параллельно сосуду. Капилляры состоят только из тонкого эндотелиального слоя клеток с связанным тонким слоем соединительной ткани.
Туника Медиа
Внутреннюю оболочку окружает средняя оболочка, состоящая из гладкомышечных клеток, эластичных и соединительных тканей, расположенных по кругу вокруг сосуда.В артериях этот слой намного толще, чем в венах. Состав волокон также различается; вены содержат меньше эластичных волокон и контролируют калибр артерий, что является ключевым моментом в поддержании артериального давления.
Туника Экстерна
Самый внешний слой — это внешняя оболочка или адвентициальная оболочка, полностью состоящая из соединительных волокон и окруженная внешней эластичной пластинкой, которая служит якорем для сосудов с окружающими тканями. Наружная оболочка часто бывает толще в венах, чтобы предотвратить коллапс кровеносного сосуда и обеспечить защиту от повреждений, поскольку вены могут располагаться поверхностно.
Структура стенки артерии : На этой схеме стенки артерии показаны гладкие мышцы, внешняя эластическая мембрана, эндотелий, внутренняя эластическая мембрана, внешняя оболочка, средняя оболочка и внутренняя оболочка.
Функция клапана
Основное структурное различие между артериями и венами — наличие клапанов. В артериях кровь перекачивается под давлением сердца, поэтому обратный ток не может возникнуть. Однако прохождение через капиллярную сеть приводит к снижению артериального давления, а это означает, что обратный ток крови возможен в венах.Чтобы противодействовать этому, в венах имеется множество однонаправленных клапанов, предотвращающих обратный ток.
Функция кровеносных сосудов
Кровеносные сосуды переносят питательные вещества и кислород по всему телу и способствуют газообмену.
Цели обучения
Перечень функций кровеносных сосудов
Основные выводы
Ключевые моменты
- Системная и легочная системы кровообращения эффективно доставляют кислород к тканям тела и удаляют продукты жизнедеятельности, такие как углекислый газ.Артериальная кровь (за исключением легочной артерии) очень насыщена кислородом и снабжает кислородом ткани организма.
- Венозная кровь (за исключением легочной вены) дезоксигенируется и возвращается в сердце, где ее перекачивают в легкие для реоксигенации.
- Питательные вещества, переносимые кровью, попадают в ткани через проницаемый эндотелий кровеносных сосудов.
- Иммунные клетки перемещаются по кровеносной системе и способны быстро проникать через стенки кровеносных сосудов, посещая места травм или инфекции.
- Кровеносные сосуды могут увеличивать или уменьшать кровоток у поверхности тела, увеличивая или уменьшая количество теряемого тепла в качестве средства регулирования температуры тела.
Ключевые термины
- терморегуляция : Поддержание постоянной внутренней температуры организма независимо от температуры окружающей среды
Кровь играет важную роль в организме: доставляет питательные вещества и химические вещества к тканям, удаляет продукты жизнедеятельности и поддерживает гомеостаз и здоровье.Кровеносная система транспортирует кровь по телу для выполнения этих действий, чему способствует обширная сеть кровеносных сосудов.
Газотранспорт
Кровеносную систему можно разделить на две части: системную и легочную. В системе кровообращения сильно насыщенная кислородом кровь (95-100%) перекачивается из левого желудочка сердца в артерии тела. При достижении капиллярных сетей может происходить газообмен между тканью и кровью, чему способствуют узкие стенки капилляров.Кислород выделяется из крови в ткани, а углекислый газ, продукт жизнедеятельности дыхания, абсорбируется. Капилляры сливаются с венулами, а затем с венами, неся дезоксигенированную кровь (~ 75%) обратно в правое предсердие сердца в конце системы кровообращения.
Легочная система гораздо меньшего размера повторно насыщает кровь кислородом и способствует удалению углекислого газа. Покинув сердце через правый желудочек, кровь проходит через легочную артерию, единственную артерию в организме, которая содержит дезоксигенированную кровь, и попадает в капиллярную сеть в легких.Тесная ассоциация тонкостенных альвеол с такими же тонкостенными капиллярами позволяет быстро выделять углекислый газ и поглощать кислород. Покидая легкие через легочную вену, единственную вену, по которой проходит насыщенная кислородом кровь, кровь попадает в левое предсердие. Это завершает систему легочного кровообращения.
Система кровообращения : На этой упрощенной схеме кровеносной системы человека (вид спереди) артерии показаны красным цветом, а вены — синим.
Дополнительные функции
Кровеносные сосуды также способствуют быстрому распределению и эффективному переносу таких факторов, как глюкоза, аминокислоты или липиды, в ткани и удалению продуктов жизнедеятельности для дальнейшей обработки, таких как молочная кислота в печень или мочевина в почки. Кроме того, кровеносные сосуды представляют собой идеальную сеть для наблюдения и распространения иммунной системы. По телу циркулируют многочисленные лейкоциты, выявляя инфекцию или травму.Как только травма обнаружена, они быстро покидают систему кровообращения, проходя через щели в стенках сосудов, чтобы достичь пораженной области, сигнализируя о более широком адресном иммунном ответе.
С механической точки зрения кровеносные сосуды, особенно близкие к коже, играют ключевую роль в терморегуляции. Кровеносные сосуды могут набухать, чтобы обеспечить больший кровоток, что приведет к большей потере тепла. И наоборот, кровоток через эти сосуды может быть уменьшен, чтобы уменьшить потерю тепла в более холодном климате.
18.1A: Структура кровеносных сосудов — Медицина LibreTexts
Кровеносные сосуды — это гибкие трубки, по которым кровь, связанный с ней кислород, питательные вещества, вода и гормоны проходят по всему телу.
Задачи обучения
- Различать структуры артерий, вен и капилляров
Ключевые моменты
- Кровеносные сосуды состоят из артерий, артериол, капилляров, венул и вен. Сети сосудов направленно и регулируемо доставляют кровь ко всем тканям.
- Артерии и вены состоят из трех слоев ткани.
- Самый толстый внешний слой сосуда (адвентициальная оболочка или внешняя оболочка) состоит из соединительной ткани.
- Средний слой (tunica media) толще и содержит больше сократительной ткани в артериях, чем в венах. Он состоит из расположенных по кругу эластичных волокон, соединительной ткани и гладкомышечных клеток.
- Внутренний слой (tunica intima) — самый тонкий слой, состоящий из одного слоя эндотелия, поддерживаемого субэндотелиальным слоем.
- Капилляры состоят из единого слоя эндотелия и связанной соединительной ткани.
Ключевые термины
- tunica intima : Самый внутренний слой кровеносного сосуда.
- tunica externa : Самый внешний слой кровеносного сосуда.
- капилляр : любой из мелких кровеносных сосудов, соединяющих артерии с венами.
- tunica media : Средний слой кровеносного сосуда.
- анастомоз : соединение между кровеносными сосудами.
Кровеносные сосуды являются ключевыми компонентами системного и легочного кровообращения, которые распределяют кровь по всему телу. Есть три основных типа кровеносных сосудов: артерии, которые несут кровь от сердца, разветвляются на более мелкие артериолы по всему телу и в конечном итоге образуют капиллярную сеть. Последний способствует эффективному химическому обмену между тканью и кровью. Капилляры, в свою очередь, сливаются в венулы, а затем в более крупные вены, ответственные за возврат крови к сердцу.Стыки между сосудами называются анастомозами.
Артерии и вены состоят из трех отдельных слоев, в то время как капилляры гораздо меньшего размера состоят из одного слоя.
Туника Интима
Внутренний слой (tunica intima) — самый тонкий слой, образованный из единого непрерывного слоя эндотелиальных клеток и поддерживаемый субэндотелиальным слоем соединительной ткани и поддерживающих клеток. В более мелких артериолах или венулах этот субэндотелиальный слой состоит из одного слоя клеток, но может быть намного толще в более крупных сосудах, таких как аорта.Внутренняя оболочка окружена тонкой мембраной, состоящей из эластичных волокон, идущих параллельно сосуду. Капилляры состоят только из тонкого эндотелиального слоя клеток с связанным тонким слоем соединительной ткани.
Tunica Media
Внутреннюю оболочку окружает средняя оболочка, состоящая из гладкомышечных клеток, эластичных и соединительных тканей, расположенных по кругу вокруг сосуда. В артериях этот слой намного толще, чем в венах. Состав волокон также различается; вены содержат меньше эластичных волокон и контролируют калибр артерий, что является ключевым моментом в поддержании артериального давления.
Туника Экстерна
Самый внешний слой — это внешняя оболочка или адвентициальная оболочка, полностью состоящая из соединительных волокон и окруженная внешней эластичной пластинкой, которая служит якорем для сосудов с окружающими тканями. Наружная оболочка часто бывает толще в венах, чтобы предотвратить коллапс кровеносного сосуда и обеспечить защиту от повреждений, поскольку вены могут располагаться поверхностно.
Структура стенки артерии : На этой схеме стенки артерии показаны гладкие мышцы, внешняя эластическая мембрана, эндотелий, внутренняя эластическая мембрана, внешняя оболочка, средняя оболочка и внутренняя оболочка.
Функция клапана
Основное структурное различие между артериями и венами — наличие клапанов. В артериях кровь перекачивается под давлением сердца, поэтому обратный ток не может возникнуть. Однако прохождение через капиллярную сеть приводит к снижению артериального давления, а это означает, что обратный ток крови возможен в венах. Чтобы противодействовать этому, в венах имеется множество однонаправленных клапанов, предотвращающих обратный ток.
кровеносных сосудов | Определение, анатомия, функции и типы
Кровеносный сосуд , сосуд в организме человека или животного, по которому циркулирует кровь.Сосуды, по которым кровь от сердца идет от сердца, называются артериями, а их очень маленькие ветви — артериолами. Очень маленькие ветви, которые собирают кровь из различных органов и частей, называются венулами, и они объединяются, образуя вены, которые возвращают кровь к сердцу. Капилляры — это крошечные тонкостенные сосуды, соединяющие артериолы и венулы; именно через капилляры питательные вещества и отходы обмениваются между кровью и тканями тела.
кровеносная системаКровь течет из сердца через артерии в капилляры.Затем он возвращается к сердцу по венам.
Британская энциклопедия, Inc.Подробнее по этой теме
Сердечно-сосудистая система человека: кровеносные сосуды
Из-за необходимости раннего развития транспортной системы внутри эмбриона, органы сосудистой системы являются одними из первых …
Внутренняя поверхность каждого кровеносного сосуда выстлана тонким слоем клеток, известным как эндотелий.Эндотелий отделен от жестких внешних слоев сосуда базальной пластинкой, внеклеточным матриксом, продуцируемым окружающими эпителиальными клетками. Эндотелий играет решающую роль в контроле прохождения веществ, включая питательные вещества и продукты жизнедеятельности, в кровь и из нее. При определенных обстоятельствах в тканях могут расти новые кровеносные сосуды — процесс, известный как ангиогенез. Ангиогенез играет важную роль в замещении поврежденной ткани, но также происходит в аномальных условиях, таких как рост и прогрессирование опухоли.
кровеносный сосуд; Сосудистая сеть головного мозга рыб-зебрыИзображение сосудистой сети головного мозга живой личинки рыбы-зебры, полученное с помощью конфокального микроскопа. Сосудистая сеть головного мозга играет важную роль в поддержании здоровья и функций мозга.
© Майкл Р. Тейлор / Фармацевтическая школа Университета Висконсин-МэдисонУ человека функции и структура кровеносных сосудов могут быть затронуты рядом различных заболеваний и состояний. Некоторые примеры включают воспаление; атеросклероз, при котором происходит отложение жира в эндотелии артерий; и гипертония, при которой сужение артериол вызывает аномальное повышение артериального давления. См. Артерия ; капиллярный; вена; сердечно-сосудистые заболевания.
Ультраструктура кровеносных сосудов — артерий — вен
В теле среднего человека около шести литров крови. Эта кровь переносится несколькими различными типами кровеносных сосудов, каждый из которых выполняет свою роль в циркуляции крови по телу.
Есть три основных типа судов; артерии, вены и капилляры. Артерии (за исключением легочной артерии) доставляют оксигенированной крови к тканям.В тканях обмен кислорода и питательных веществ осуществляется капиллярами. Капилляры также возвращают деоксигенированную кровь в вены, которые возвращают ее обратно к сердцу (за исключением легочных вен).
Рис. 1.0 — Обзор сосудов, участвующих в кровообращении. [/ caption]В этой статье мы проследим путь крови по телу, исследуя структуру и функции основных типов кровеносных сосудов.
Стенки емкости можно разделить на три части; tunica intima (самая внутренняя), tunica media и tunica adventitia. Каждый должен быть рассмотрен.
Артериальная система
В целом артериальная система забирает насыщенную кислородом кровь от сердца и доставляет ее в капилляры, где может происходить обмен кислорода и питательных веществ.
В организме есть четыре основных типа артерий, каждая из которых имеет свое строение и функцию. Мы рассмотрим каждый из них более подробно (в порядке уменьшения размера).
Большие эластичные (проводящие) артерии
Рис. 1.1 — Компоненты стенки артерии. [/ caption]Это самые большие артерии в организме, расположенные ближе всего к сердцу. Они работают, чтобы «проводить» кровь от сердца к участкам тела, где она может быть распределена.
Эластичные артерии включают большинство названных сосудов, окружающих сердце, таких как аорта и легочные артерии .
Структура:
- Tunica Intima : Эндотелиальные клетки с тонким субэндотелием соединительной ткани и прерывистыми эластичными пластинками.
- Tunica Media : Среда оболочки состоит из 40-70 окончатых эластичных мембран с гладкомышечными клетками и коллагеном между этими пластинками. Это самая толстая часть эластичной артерии.
- Tunica Adventitia : Тонкий слой соединительной ткани, содержащий лимфатические, нервные и vasa vasorum (кровеносные сосуды, которые снабжают кровью артерию — артериям нужна кровь, чтобы выжить, как и любой другой ткани!)
Medium Muscular ( Разводящие) артерии
Из крупных эластических артерий кровь поступает в более мелкие, распределяющие артерии.Они распределяют кровь по подобластям тела.
Средние мышечные артерии похожи по строению на крупные эластические артерии.
Структура:
- Tunica Intima : состоит из эндотелия, субэндотелиального слоя и толстой эластичной пластинки.
- Tunica Media : Состоит из примерно 40 слоев гладких мышц, соединенных щелевыми соединениями для обеспечения скоординированного сокращения.
- Tunica Adventitia : Тонкий слой соединительной ткани, содержащий второстепенные сосуды, лимфатические и нервные волокна.
Артериолы
Артериолы входят в состав микроциркуляции . Они несут кровь от мышечных артерий к метартериолам.
Структура :
Артерии диаметром менее 0,1 мм классифицируются как артериолы. Обычно они имеют около 3 слоев гладкомышечных клеток, а внутренняя эластичная пластинка отсутствует. Наружная эластическая пластинка присутствует только в более крупных артериолах.
Метартериолы
Артерии, снабжающие капиллярное русло, известны как метартериолы .
Вместо того, чтобы иметь непрерывный слой из гладкомышечных клеток , в определенных точках расположены промежуточные кольца гладких мышц. Эти кольца известны как прекапиллярные сфинктеры , , которые сокращаются, чтобы контролировать кровоток в капиллярном ложе.
[старт-клинический]
Клиническая значимость: прекапиллярные сфинктеры
Прекапиллярные сфинктеры очень важны для контроля перфузии тканей . Когда организм выполняет определенные действия, эти структуры могут ограничивать приток крови к определенным областям и поощрять его к другим.
Например, при беге скелетным мышцам требуется намного больше крови, чем обычно. Чтобы приспособиться к этому, прекапиллярные сфинктеры в скелетных мышцах расслабляются, чтобы увеличить кровоток .
[окончание клинической]
Капилляры
Капилляры состоят из одного слоя эндотелия и его конкордантной базальной мембраны.
Они специально адаптированы для обеспечения короткого расстояния диффузии для обмена питательных веществ и газов с тканями, которые они поставляют.
Есть три типа капилляров; непрерывный , фенестрированный и синусоидальный , каждая из которых имеет промежутки различного размера между эндотелиальными клетками.
Эти промежутки действуют как сито, контролируя, какие молекулы и структуры могут покидать капилляр. Например, в непрерывных капиллярах (расположенных в скелетных мышцах ) может уходить только вода и определенные ионы. В синусоидальных капиллярах (расположенных в печени ) могут выходить более крупные структуры, такие как клетки и белки.
Рис. 1.2. Три различных типа капилляров. [/ caption]Венозная система
Венозная система забирает дезоксигенированную кровь из капилляров и доставляет ее к сердцу (за исключением легочных вен). Из сердца кровь может перекачиваться в легкие и повторно насыщаться кислородом.
Подобно артериальной системе, венозная система состоит из различных сосудистых структур. Мы рассмотрим каждый из них более подробно (в порядке возрастания размера по мере удаления от капилляров).
Посткапиллярные венулы
Посткапиллярная венула получает кровь из капилляров и впадает в венулы . Кроме того, окружающая тканевая жидкость имеет тенденцию стекать в них, поскольку их давление ниже, чем в капиллярах или ткани.
Структура:
Стенка представляет собой эндотелиальную выстилку с ассоциированными перицитами и диаметром 10-30 мкм. Это похоже на структуру капилляров, но посткапиллярные венулы более проницаемы, что делает их предпочтительным местом миграции белых кровяных телец (e.грамм. к участкам заражения).
[старт-клинический]
Клиническая значимость: воспаление и посткапиллярные венулы
Во время воспаления давление в венулах на самом деле становится на выше, чем на , чем в окружающем интерстиции . Это позволяет жидкости просачиваться в место воспаления вместе с воспалительными цитокинами и лейкоцитами.
[окончание клинической]
Венулы
Венулы непрерывные с посткапиллярными венулами.Они продолжают отводить кровь от ложа капилляров. Многие венулы объединяются , образуя вену.
Структура :
Эндотелий связан с перицитами или тонкими гладкомышечными клетками (начало средней оболочки), образуя очень тонкую стенку. Венулы могут иметь диаметр до 1 мм. Они также содержат клапана, , которые сжимаются, чтобы ограничить ретроградный транспорт крови.
Жил
Вены — это основные сосуды венозной системы .Это последний шаг на пути к возвращению крови к сердцу.
Структура :
Рис. 1.3 — Структура стенки жилы. [/ caption]Вены обычно имеют больший диаметр и более тонкую стенку, чем соответствующая артерия. В стенке сосуда больше соединительной ткани, меньше эластичных и мышечных волокон.
Вены незначительно различаются по структуре в зависимости от их размера:
- Малая и средняя вены имеют хорошо развитую адвентициальную оболочку и тонкую внутреннюю и среднюю оболочки.
- Крупные вены имеют диаметр более 10 мм и более толстую внутреннюю оболочку. У них хорошо развита продольная гладкая мускулатура адвентициальной оболочки. Среда имеет круглую гладкую мускулатуру, которая обычно не выделяется, за исключением поверхностных вен ног.
Вены содержат клапана , которые в первую очередь предотвращают обратный ток крови. Они также действуют вместе с сокращением мышц, сжимая вены, чтобы продвигать кровь к сердцу.
Venae Comitantes
Venae comitantes — глубокие парные вены, заключенные вместе с артерией в одно влагалище. Пульсация артерии способствует венозному возврату в парные вены.
Структура и функции кровеносных сосудов и сосудистых ниш в кости
Кость обеспечивает питательную микросреду для множества типов клеток, которые координируют важные физиологические функции скелета, такие как энергетический обмен, минеральный гомеостаз, остеогенез и кроветворение.Эндотелиальные клетки образуют сложную сеть кровеносных сосудов, которая организует и поддерживает различные микросреды в кости. Недавнее выявление гетерогенности костной сосудистой сети подтверждает существование множественных сосудистых ниш в компартменте костного мозга. Уникальная комбинация клеток и факторов, определяющих конкретную микросреду, поставляет регуляторные сигналы для выполнения определенной функции. В этом обзоре обсуждаются последние достижения в нашем понимании сосудистых ниш в кости, которые играют критическую роль в регуляции поведения мультипотентных гематопоэтических и мезенхимальных стволовых клеток во время развития и гомеостаза.
1. Введение
Последние достижения в биологии сосудов расширили наше понимание и знание кровеносных сосудов и их характеристик при различных физиологических и патологических состояниях. Кровеносные сосуды не только действуют как транспортная система, но также играют важную роль в развитии органов, морфогенезе тканей, воспалении, формировании барьеров и заживлении ран [1–4]. Кроме того, активное участие кровеносных сосудов в патогенезе ряда заболеваний предполагает фундаментальную необходимость понимания этих универсальных транспортных сетей в организме [5].Кровеносные сосуды являются неотъемлемой частью скелетной системы, играющей множество ролей в поддержании гомеостаза костей. Первоначально важность кровеносных сосудов в кости была признана хирургами при восстановлении и заживлении переломов костей [6, 7]. Существенная роль, которую играет костная сосудистая сеть во время развития скелета [8–10] и заживления переломов [6, 9, 11], является предметом интенсивных исследований. Более того, клеточно-специфический вклад в плейотропные функции костей, таких как регулирование метаболизма всего тела [12–14], функций мозга [15–17] и минерального гомеостаза [18–20], все еще требует понимания.
Сообщается, что кровеносные сосуды в кости обеспечивают питательную микросреду для гемопоэтических стволовых клеток (HSC) [21, 22] и мезенхимальных стволовых клеток (MSC) [23, 24]. Различные микросреды в костях все еще нуждаются в хороших характеристиках, чтобы понять их функции во время развития, роста и болезней. Последние технические достижения в области визуализации костей существенно улучшили наши фундаментальные знания о скелетных кровеносных сосудах. Этот обзор призван предоставить обзор последних разработок и современных представлений о костной сосудистой сети и ее микросреде.
2. Строение и характеристика кровеносных сосудов скелетной системы
2.1. Скелетное кровообращение
Кость имеет разветвленную сеть кровеносных сосудов (рис. 1), на которые потребляется почти 10–15% сердечного выброса в состоянии покоя [25, 26]. Пространственное расположение кровеносных сосудов обеспечивает эффективную и оптимальную доставку кислорода и питательных веществ в различные места в компартменте костного мозга. Независимо от типа кости, основное кровоснабжение костей происходит из артерий, входящих в кортикальную область, которые соединяются с медуллярными синусоидами, чтобы окончательно выйти из кости через вены [27, 28].Однако форма и тип скелета могут повлиять на расположение капиллярной сети, существующей между артериями и венами. Типичные длинные кости, такие как бедренная и большеберцовая кость, снабжаются несколькими артериями и артериолами, которые классифицируются в зависимости от области кровоснабжения. Центральная артерия, также называемая питательной артерией, входит в кость через отверстие и разветвляется на ряд более мелких артерий и артериол, чтобы снабжать максимальное количество областей взрослой кости. Он поддерживает высокое кровяное давление, достигая удаленных участков, обычно заканчиваясь капиллярами, присутствующими в метафизе и эндосте.Есть центральная большая вена, которая принимает кровь из капилляров, присутствующих в различных областях, и выводит дезоксигенированную кровь и отходы питательных веществ из костей [29]. Надкостничные артерии снабжают внешнюю поверхность кости и связаны с гаверсовскими артериями, находящимися в кортикальной области, через артерии Фолькмана. Гаверсовские артерии проходят параллельно продольной оси длинной кости в коре головного мозга, в то время как более короткие артерии Фолькмана проходят перпендикулярно оси длинной кости [30, 31]. Гаверсовы артерии в конечном итоге сходятся в метафизарные капилляры, чтобы доставлять кровь в костномозговую область.Напротив, кровоснабжение из эпифизарных артерий не имеет пути к медуллярной области длинных костей, таким образом поддерживая отдельное кровообращение в области эпифиза. Эпифизарные артерии входят в кость из густой сети периартикулярных сосудистых сплетений, присутствующих на концах длинных костей. Вены, отводящие эпифизарную кровь, относительно меньше по размеру по сравнению с веной, присутствующей в медуллярной области (рис. 1).
2.2. Неоднородность кровеносных сосудов
Расхождение в артериальном кровоснабжении предполагает наличие множества вен и подтипов капилляров в кости.Однако до недавнего времени разнообразие внутри этих кровеносных сосудов не получало должного внимания. Фенестрированные или синусоидальные капилляры образуют большинство кровеносных сосудов в сосудистой сети скелета. Это сильно разветвленные сети кровеносных сосудов, присутствующие в костном мозге костей. Синусоидальные эндотелиальные клетки экспрессируют рецептор-3 фактора роста эндотелия сосудов (VEGFR3), тогда как эндотелий костной артерии отрицателен для Vegfr3 [32]. Сосудистые структуры в кости можно разделить на ламинин + / низкий Sca-1 — / низкий синусоиды, Sca-1 + ламинин + эндостальные сосуды и Sca-1 + ламинин + центральные артерии [33].Исследование кровеносных сосудов во время постнатального развития привело к идентификации нового подтипа кровеносных сосудов, называемого типом H, присутствующего в активно растущих областях кости. Они названы типом H, так как они экспрессируют высокие уровни маркеров кровеносных сосудов, эндомуцина (Emcn) и CD31 (Pecam1) по сравнению с синусоидальными сосудами, которые экспрессируют низкие уровни этих маркеров, таким образом, названных типом L [8, 10].
В активно растущей кости сосуды типа H присутствуют в областях метафиза и эндоста, в то время как сосуды типа L преобладают во всей области мозгового вещества.Капилляры типа H — это кровеносные сосуды с линейной структурой, расположенные столбчато, по сравнению с разветвленной сетью капилляров типа L. Ведущие фронты сосудов типа H, которые опосредуют ангиогенез в кости, содержат выпуклые люменизированные структуры [10, 29]. Однако функциональное значение этих уникальных структур сосудистого фронта остается неизвестным. Артерии и артериолы экспрессируют эфрин B2 (Efnb2) и отрицательны для экспрессии Emcn. Предполагается, что субпопуляция эндотелиальных клеток в эндотелии типа H, экспрессирующих как Efnb2, так и Emcn, генерирует артериолярные кровеносные сосуды (Efnb2 +, Emcn-).Эта субфракция кровеносных сосудов типа H отображает экспрессию других артериальных маркеров, таких как Sox17 и нейропилин-1 [34]. Артерии плотно обернуты мезенхимальными клетками с актином гладких мышц α + ( α SMA +), в то время как более мелкие артериолы содержат α SMA− и рецептор тромбоцитарного фактора роста бета + (PDGFR β +) периваскулярных клеток. Множественные типы костных мезенхимальных клеток и их связь с подтипами кровеносных сосудов обсуждаются позже в этом обзоре.Таким образом, костная сосудистая сеть неоднородна, уникальна и требует глубоких исследований, чтобы понять тканеспецифические сосудистые модификации и специализированные функции.
3. Кровоток и оксигенация в костях
Пространственное расположение кровеносных сосудов сложное и уникальное в каждой ткани, чтобы обеспечить надлежащее снабжение кислородом и питательными веществами всей ткани или органа. Организация различных подтипов кровеносных сосудов в длинных костях указывает на своеобразную картину кровотока. Скорость кровотока выше в сосудах типа H по сравнению с сосудами типа L.Когда кровь течет из капилляров типа H, скорость кровотока падает с каждой сосудистой ветвью в метафизе, достигая характерной низкой скорости для капилляров типа L в диафизе. Частые разветвления и соединения сосудистых сетей в диафизе поддерживают низкую скорость кровотока в диафизарных капиллярах [29, 35].
3.1. Кислородный статус в костно-сосудистой микросреде
Своеобразная картина кровотока в кости совпадает с кислородным статусом костной микросреды.Измерение местного напряжения кислорода (pO 2 ) у живых мышей показало, что pO 2 выше в области эндостальной кости, чем в более глубоких синусоидальных областях. Эндостальные области васкуляризированы капиллярами и артериолами типа H по сравнению с сосудами типа L в синусоидальных областях [36]. Также было показано, что низкая проницаемость сосудов в артериальных сосудах и сосудах типа H поддерживает низкоактивные формы кислорода (ROS) в микросреде по сравнению с фенестрированными высокопроницаемыми синусоидами [35].Анализ HSCs у перфузированных Hoechst мышей показал, что локализация долгосрочных HSCs (LT-HSCs) ограничена наименее перфузируемыми областями в BM [37, 38]. Низкое содержание кислорода или гипоксическая микросреда поддерживает поддержание HSC и защищает их от повреждений, вызванных кислородным стрессом [39]. Гипоксия-зависимая стабилизация фактора, индуцируемого гипоксией (HIF), важна для канонического HIF-опосредованного сигнального пути, который играет разные роли в кровеносных сосудах [8, 34], мезенхимальных клетках [40] и гематопоэтических клетках [39, 41, 42] в микросреде БМ.
Гипоксия и HIF-1 α -опосредованная регуляция роста и выживания хондроцитов важна для хондрогенеза и развития пластинок роста [43, 44]. Важной нижестоящей мишенью HIF-1 α является VEGF, фундаментальный фактор, необходимый для образования кровеносных сосудов в физиологических и патологических условиях [45]. VEGF играет плейотропную роль в регулировании нескольких процессов во время развития, роста и восстановления костей [46]. Генетические исследования хондроцитов продемонстрировали важные функции их VEGF в ангиогенезе и формировании костей в дополнение к регуляции хондрогенеза [47, 48].Таким образом, опосредованная гипоксией регуляция HIF контролирует уровни VEGF, чтобы сочетать рост кровеносных сосудов и остеогенез в кости [49, 50]. Стабилизация HIF в остеопрогениторах приводит к расширению ниши HSC и стимулированию продукции эритропоэтина в кости [51]. HSCs также используют передачу сигналов HIF для точной регуляции своего клеточного цикла и состояния покоя в BM [42].
Генетические и фармакологические манипуляции с кровотоком у развивающихся рыбок данио влияют на передачу сигналов синтазы оксида азота в примитивных HSC, что приводит к дефектному развитию HSC [52].Кровоток также играет важную роль в мобилизации кроветворных клеток из костей в различные органы и ткани. У мышей синусоидальные сосуды с высокой проницаемостью способствуют миграции и дифференцировке HSPCs [35]. Уменьшение количества сосудов и артериол типа H в кости с возрастом приводит к снижению перфузии скелетной крови и функции HSC [29, 34]. Кроме того, манипулирование кровотоком в кости приводит к нарушению ангиогенеза и образования кости [29], что позволяет предположить, что кровоток является потенциальной причиной возрастной потери костной массы.Эти убедительные доказательства доказывают важность кровотока в поддержании гомеостаза скелета путем регулирования образования костей и гематопоэза.
3.2. Клиническая важность кровотока в скелете
Несмотря на различия в костных структурах, исследования на моделях грызунов оказались полезными для разработки терапевтических стратегий, направленных на борьбу с заболеваниями костей человека. Основное понимание кровеносных сосудов и кровотока в скелетной системе в основном получено из результатов, полученных на моделях грызунов.Грызуны демонстрируют возрастную потерю костной массы, как и люди. Примечательно, что выявление уменьшения капилляров костных артерий с возрастом у мышей [34] соответствует возрастному снижению кровотока в бедренной артерии у людей [53]. Недавняя демонстрация уменьшения сосудов типа H у пожилых людей и людей с остеопорозом [54] подчеркивает важность исследования скелетных кровеносных сосудов у грызунов.
Растущее количество клинических доказательств указывает на важность кровотока в поддержании гомеостаза скелетной системы.Пониженное кровоснабжение было измерено в костях пожилых женщин с остеопорозом [55]. Нарушение кровоснабжения кости вызывает гибель костных клеток, что приводит к развитию состояния остеонекроза [56]. Сравнительное исследование пациентов с односторонним окклюзионным заболеванием артерий показало пагубное влияние дефектного кровотока на минерализацию костей [57]. Дефекты кровотока в субхондральной области были идентифицированы как потенциальный механизм возникновения остеоартрита [58]. Системные заболевания, такие как диабет [59], хронические обструктивные заболевания легких [60] и гипертония [61], которые нарушают перфузию сосудов, связаны с дефектами костей.Более того, кровоснабжение имеет решающее значение для инициирования образования костной мозоли во время заживления и восстановления перелома [6]. В местах перелома наблюдается дефектное формирование кровеносных сосудов, что свидетельствует о замедлении процессов заживления и регенерации [50]. Вызванные неиспользованием состояния остеопении, такие как постельный режим и разгрузка задних конечностей, также были связаны с изменениями кровоснабжения костей [62, 63]. Несмотря на клинические данные, подтверждающие экспериментальные данные, необходимы дальнейшие исследования, чтобы понять молекулярные механизмы, участвующие в возникновении этих клинических состояний.
4. Сосудистое микросредство для мезенхимальных клеток
4.1. Типы мезенхимальных стволовых клеток и клеток-предшественников, образующих строму костного мозга
Клетки мезенхимального происхождения, составляющие большую часть популяции стромальных клеток костного мозга, образуют важный компонент микросреды костного мозга. Мультипотентные мезенхимальные стволовые клетки и клетки-предшественники (MSPC) могут генерировать различные типы мезенхимальных стромальных клеток костного мозга, включая остеобласты, хондроциты, адипоциты и ретикулярные клетки.Понимание иерархической взаимосвязи стромальных клеток костного мозга все еще является интенсивной областью исследований. Хотя предполагалось периваскулярное происхождение MSPCs в различных органах [23], отдельные волны стромальных клеток были идентифицированы в развивающемся костном мозге [64, 65]. Методы отслеживания генетических клонов предоставили значительные знания в понимании гетерогенности, связанной с мезенхимальными клетками костного мозга. Клетки нестин-GFP + окружают эндотелиальные клетки (ЭК), которые образуют артерии и капилляры типа Н.Периваскулярные клетки нестин-GFP + были идентифицированы как маркеры ранних MSPC, которые могут генерировать строму костного мозга и клетки костного происхождения [66]. Точно так же остерикс + неонатальные мезенхимальные клетки обладают потенциалом генерировать клетки линии костей, хондроциты, адипоциты и строму костного мозга. Напротив, остерикс + эмбриональные и взрослые мезенхимные клетки обнаруживают ограниченный потенциал [64]. Примечательно, что как osterix +, так и Nestin-GFP + клетки присутствуют около капилляров типа H и отсутствуют вокруг перисинусоидальных капилляров типа L [8, 35].Было высказано предположение, что перисинусоидные стромальные клетки, экспрессирующие рецептор лептина (LepR), вносят вклад в клетки костного происхождения, если они отмечены на ранних этапах развития [67]. Примечательно, что экспрессия LepR в мезенхимальных клетках взрослых способствует их адипогенному потенциалу, ингибируя судьбу остеогенных клеток [68]. LepR + клетки вносят вклад в экспрессию хемокинового лиганда 12 (Cxcl12) мотива C-X-C в костном мозге [69]. Cxcl12, экспрессирующие нестин-отрицательные мезенхимальные клетки, обеспечивают HSC поддерживающее микроокружение [70]. Следовательно, будет интересно использовать индуцибельную (- CreER ) систему, чтобы понять стадийно-специфический вклад LepR + клеток в строму BM.
В отличие от периваскулярных MSPC, клетки непериваскулярного происхождения также были идентифицированы как способствующие формированию клеток костей и стромы BM. Клетки слежения за клетками хондрогенного происхождения с использованием системы Col2-CreER продемонстрировали их потенциал к образованию клеток костного происхождения и ретикулярных стромальных клеток с множеством Cxcl12 [65]. Точно так же отслеживание клонов с использованием других хондрогенных систем, таких как Sox9- и Aggrecan- CreER , также подтвердило способность клеток генерировать множественные мезенхимальные клональные клетки.Идентификация Gremlin1 как маркера клеток с остеохондроретикулярным потенциалом указывает на возможное существование различных подтипов предшественников в пуле MSPCs. Клонально расширяющиеся клетки Gremlin1 + были идентифицированы в пластинке роста и области метафиза, и у них отсутствует потенциал дифференцировки адипоцитов [71]. Эти исследования демонстрируют наличие неоднородности в MSPC и необходимость понимания подтипов в популяции, чтобы определить их иерархические отношения.
4.2. Локализация мезенхимальных стромальных клеток в сосудистой нише
Локализация MSPCs предполагает, что множественные регионы в микросреде костного мозга могут поддерживать и обеспечивать ниши для MSPC. Клетки Col2 +, Sox9 + и Aggrecan + расположены на ростовой пластинке, которая является бессосудистой областью [65]. Клетки Gremlin1 + присутствуют как в области ростовой пластинки, так и в области метафиза [71]. Клетки нестин-GFP + располагаются вокруг артерий и в метафизе [35, 66]. PDGFR β + мезенхимные клетки обнаруживают образец распределения, подобный клеткам Nestin-GFP + [34].Большинство osterix + клеток расположено вокруг сосудов типа H в метафизе [8, 64]. Клетки LepR + и Cxcl12 + в основном локализуются вокруг сосудов типа L (перисинусоидальных) [67, 68]. Хондроциты присутствуют в бессосудистой зоне, обычно в зоне роста или эпифизе костей [65]. Остеогенные предшественники специфически локализуются вокруг сосудов типа H в областях метафиза и эндоста [8]. Жировые клетки или адипоциты преимущественно присутствуют в перисинусоидальном пространстве диафиза [68].Ретикулярные клетки также локализуются вокруг сосудов типа L в перисинусоидальной области [67, 69]. Клетки гладких мышц сосудов — это α, SMA + периартериальные клетки, плотно охватывающие артерии в микросреде костного мозга [8, 34]. Таким образом, субпопуляции гетерогенных мезенхимальных стромальных клеток костного мозга преимущественно локализуются вокруг определенных подтипов кровеносных сосудов, что указывает на существование специализированных сосудистых микросредств (Рисунок 2).
Свидетельства указывают на центральную роль кровеносных сосудов в поддержании местной микросреды.Высокая экспрессия проостеогенных факторов в сосудах типа H создает микросреду, необходимую для остеопрогениторов. Продвижение капилляров типа H в кости приводит к увеличению количества остеопрогениторов [8, 10]. Аналогичным образом, производный от тромбоцитов фактор роста B (PDGF-B), высвобождаемый эндотелием, связывается с рецептором PDGF, присутствующим на мезенхимальных клетках, для активации опосредованных ростом сигнальных путей [72]. Сверхэкспрессия PDGF-B в костном эндотелии приводит к увеличению PDGFR β + периваскулярных мезенхимальных клеток в костном мозге [34].Мезенхимные клетки также выделяют ангиогенные факторы, такие как VEGF, ангиопоэтин, FGF и BMP [3, 4], чтобы поддерживать взаимную взаимосвязь в регуляции специфического микроокружения костного мозга.
5. Кровеносные сосуды в микросреде гемопоэтических стволовых клеток (HSC)
5.1. Костные эндотелиальные клетки в поддержании HSC
Сильная взаимозависимость ECs и HSCs была проиллюстрирована во время как примитивного, так и определенного гематопоэза [22, 73, 74]. Важность сосудистой сети костного мозга первоначально оценивалась только для тромбопоэза, мобилизации стволовых клеток и хоминга [21].Идентификация долговременных (LT) HSCs вблизи кровеносных сосудов вызвала огромный интерес в этой области для понимания сосудистой ниши костного мозга [75]. Было выявлено, что культивируемые ЭК из негематопоэтических органов, таких как сердце и печень, поддерживают HSC in vitro , тогда как ЭК из почек лишены этого потенциала [76]. Позже идентификация тканеспецифических молекулярных сигналов в ECs [77] предположила уникальный потенциал эндотелия костного мозга в значительной поддержке HSCs и гематопоэза по сравнению с EC из других органов.
Эндотелиальная делеция гликопротеина 130 (gp130), субъединицы рецепторов, связывающих семейство хемокинов IL-6, приводила к образованию гипоцеллюлярного костного мозга и снижению количества HSC [78]. На регенерацию синусоидальных ЭК после облучения сильно повлияло ингибирование передачи сигналов VEGFR2 с помощью блокирующих антител [79]. Было высказано предположение, что E-селектин экспрессируется исключительно в эндотелии костного мозга, а делеция этого гена усиливает покой HSC и устойчивость к облучению [80]. В дополнение к прямому контакту с клетками было показано, что ЭК высвобождают растворимые факторы, называемые ангиокринными факторами, для регулирования микроокружения HSC [2].Cxcl12 и фактор стволовых клеток (Scf) являются важными и широко исследуемыми ангиокринными факторами ЭК ВМ, участвующими в регуляции гомеостаза HSC. Специфичная для эндотелиальных клеток делеция Scf приводила к снижению количества HSC с пониженным потенциалом репопуляции после трансплантации BM [81]. В аналогичном исследовании делеция Cxcl12 в ECs приводила к истощению HSCs и их долговременной репопуляционной активности [69]. В недавнем исследовании активация передачи сигналов Notch в ECs привела к экспансии как клеточных, так и ангиокринных компонентов микросреды HSC.Передача сигналов эндотелиального Notch способствует образованию капилляров нового типа H, малых артериол, периваскулярных мезенхимных клеток PDGFR β + и клеточных уровней Scf [34].
5.2. Микроокружение артериол для долговременных HSCs
Было продемонстрировано, что микроокружение артериол, состоящее из артериальных ЭК и окружающих NG2 + мезенхимных клеток, поддерживает HSC в состоянии покоя [82]. Точно так же синусоидальные кровеносные сосуды и окружающие LepR + мезенхимальные клетки также обеспечивают микроокружение для поддержания популяции HSC [83].В другом исследовании было показано, что α -катулин GFP + c-Kit + HSC локализуются в центральной области костного мозга, состоящей из синусоидального микроокружения, образованного синусоидальными кровеносными сосудами и мезенхимальными клетками LepR +. Он также предлагает единое перисинусоидальное микроокружение как для покоящихся, так и для делящихся HSCs [84]. Было показано, что артериальные кровеносные сосуды, имеющие меньшую проницаемость, поддерживают HSC при низком уровне АФК по сравнению с высокопроницаемыми синусоидами, участвующими в переносе клеток и хоминге [34, 35]. Эндотелиальная Notch-опосредованная сигнализация амплификация артериолярных кровеносных сосудов ведет к расширению ниш HSC, что приводит к увеличению количества HSC и их функции у молодых мышей [34].Недавно была идентифицирована экспрессия Hoxb5 в BM, которая разграничивает популяцию LT-HSC. Пространственная локализация Hoxb5 + HSCs показывает, что они непосредственно прикрепляются к VE-cadherin + ECs, указывая на их тесную ассоциацию с кровеносными сосудами в микроокружении BM [85]. Исследование не предоставляет дополнительных сведений о сосудистом микросреде вблизи Hoxb5 + HSC. Будет интересно понять локализацию HSC Hoxb5 + в контексте множества сосудистых компартментов, присутствующих в микросреде BM.
Несмотря на растущий интерес к костной сосудистой сети и к тому, что манипулирование кровеносными сосудами может регулировать микросреду костного мозга, наши знания о гетерогенных сосудистых нишах и эндотелиальных регуляторных факторах ограничены, чтобы получить представление о сосудистой организации микроокружения костного мозга. В таблице 1 приведены важные факторы, изученные в костных эндотелиальных клетках, и их специфические функции. Становится все более очевидным, что костная сосудистая сеть очень сложна, неоднородно состоит из различных типов кровеносных сосудов и наделена специальными функциями, которые контролируют формирование кости, кроветворение и регенерацию кости.ЭК, образующие эти гетерогенные кровеносные сосуды вместе с высвобождаемыми ими ангиокринными факторами и поддерживающие окружающие типы клеток, способствуют формированию множества микросредов в костном мозге. Кроме того, местный кислородный статус, обусловленный организацией капилляров и микроциркуляции, регулирует поведение и функции микросреды. Участие множества факторов и типов клеток предполагает существование дисциплинированных механизмов регуляции для контроля целостности локальных ниш.Рассмотрение клеточных и молекулярных компонентов этих локальных микроокружений улучшит наше понимание клинически значимых HSC и MSC в кости.
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
ECs, играющие центральную роль в конструировании и организации различных микроокружений в BM, потенциально могут служить отличной мишенью для манипулирования конкретными нишами в кости. Реактивация сосудов типа H у старых мышей может способствовать неоостеогенезу, что приводит к образованию новой кости и увеличению костной массы [8, 29].Несмотря на его потенциальное терапевтическое применение, ограниченные знания о костной сосудистой сети серьезно влияют на наше понимание организации и локализации микросреды в кости. Характеристика гетерогенных кровеносных сосудов и факторов, производных от их эндотелия, а также дальнейшее понимание клеточных и молекулярных компонентов микросреды имеют решающее значение для выяснения взаимодействия и роли кровеносных сосудов в регулировании архитектуры костного мозга в различных физиологических и патологических состояниях.
Конфликт интересов
Автор заявляет об отсутствии конфликта интересов относительно публикации данной статьи.
Благодарности
Финансирование было предоставлено Wellcome Trust, Королевским обществом и Советом медицинских исследований Великобритании.
Кровеносные сосуды — AMBOSS
Последнее обновление: 15 июля 2020 г.
Резюме
Кровеносные сосуды являются неотъемлемым компонентом системы кровообращения. Пять типов кровеносных сосудов (в порядке кровообращения): артерии, артериолы, капилляры, венулы и вены.Основная функция крупных кровеносных сосудов (то есть артерий и вен) — транспортировка крови к сердцу и от него, тогда как более мелкие кровеносные сосуды (например, капилляры) обеспечивают обмен веществами между клетками и кровью. Артерии несут богатую кислородом кровь от сердца к периферии. Достигнув органа или конечности, они разветвляются и разделяются на артериолы и, в конечном итоге, на множество мелких капилляров, образуя капиллярное русло, которое обеспечивает доставку кислорода и питательных веществ к окружающим тканям.Дистальнее капиллярного ложа посткапиллярные венулы соединяются вместе, образуя вены, которые доставляют бедную кислородом кровь обратно к сердцу. И артерии, и вены состоят из одних и тех же трех слоев ткани: внутренней оболочки, средней оболочки и адвентициальной оболочки. Артерии содержат значительно больше гладких мышц, чем вены (особенно в средней оболочке), тогда как вены содержат клапаны в внутренней оболочке. Капилляры полностью состоят из эндотелиального слоя с базальной мембраной или без нее. Существует три различных типа капилляров (непрерывные, окончатые и синусоидальные), все из которых различаются по проницаемости и функциям.Кровеносные сосуды вместе называются сосудистой системой и вместе с сердцем составляют систему кровообращения или сердечно-сосудистую систему.
В отдельной статье по физиологии сосудов рассматриваются темы гемодинамики, регуляции артериального давления и капиллярного обмена.
Крупные кровеносные сосуды
Состоят из артерий и вен, которые имеют три основных микроскопических слоя стенки.
Слои крупных кровеносных сосудов
Артерии
- Функция: транспортировка артериальной (оксигенированной) крови от сердца к периферии
- Курс: артерия → артериола → капилляр
- Типы артерий: компоненты стенки кровеносных сосудов различаются в зависимости от расположения и функции
Жил
- Функция: транспортировка венозной (деоксигенированной) крови от периферии к сердцу
- Ход: капилляр → венула → вена
- Характерная особенность: вены известны как емкостные сосуды, потому что они способны хранить значительно больший объем крови, чем артерии, из-за их большого просвета и высокой податливости.
- Структура: см. «Слои кровеносных сосудов» выше
Каталожные номера: [1] [2] [3]
Мелкие кровеносные сосуды
Микроциркуляция
Артериолы
Метартериолы
Капилляры
- Функция: обмен газов и питательных веществ с тканями (плотность распределения капилляров варьируется в зависимости от региона / органа)
- Характерные особенности
- Структура (от внутреннего к внешнему слою)
Эндотелий составляет часть гематоэнцефалического барьера.Плотные плотные контакты между эндотелиальными клетками препятствуют параклеточному транспорту через капилляры головного мозга.
Венулы
- Функция: сбор крови из капилляров для передачи в вены
- Строение: зависит от типа венулы
- Посткапиллярные венулы
- Расположены непосредственно после капиллярного русла.
- Структура напоминает капилляры (обеспечивает высокую проницаемость и обмен веществ)
- Собирающие венулы:
- Перед собирающими венами
- Структура напоминает более крупные кровеносные сосуды (т.е.е., с тремя слоями)
- Венулы высокого эндотелия обладают специальными поверхностными молекулами для распознавания лейкоцитов, которые являются местами экстравазации лейкоцитов в лимфатические органы или из них
- Посткапиллярные венулы
Ссылки: [1] [3]
Клиническая значимость
Источники
- Модули обучения NIH SEER — Классификация и структура кровеносных сосудов. https: // обучение.seer.cancer.gov/anatomy/cardiovascular/blood/classification.html . Обновлено: 1 января 2019 г. Доступ: 22 апреля 2019 г.
- Стандринг С. Анатомия Грея: анатомические основы клинической практики . Elsevier Health Sciences ; 2016 г.
- Лесли П. Гартнер, Джеймс Л. Хиатт. Цветной учебник гистологии . Grune & Stratton Inc. ; 2006 г.
Система кровообращения: Руководство по гистологии
Венулы и вены
Для возврата крови к сердцу существует ряд венул, вен и мышечных вен.Венулы имеют гораздо больший просвет и более тонкие стенки, чем соответствующие артериолы. Точно так же вены можно отличить от артерий и артериол, потому что их стенки намного тоньше по сравнению с диаметром их просвета.
Венозному возврату от ног способствует сокращение скелетных мышц, которое сжимает вены внутри них, а в вены среднего размера также есть клапаны, чтобы преодолеть проблему обратного потока.
Вены по-прежнему имеют три основных слоя (адвентициальная оболочка, средняя оболочка и внутренняя оболочка), но эластические и мышечные компоненты менее выражены.Слои гладких мышц используются для сокращения или расширения вен, чтобы приспособиться к изменениям объема крови.
Венулы
Они имеют чистый слой tunica intima , без каких-либо эластичных волокон, и среднюю оболочку tunica media с одним или двумя слоями мышечных волокон. Адвентициальная оболочка , сливается с окружающей тканью.
Посмотрите на эту фотографию венулы и найдите просвет (содержащий эритроциты) и эндотелиальные клетки.
Жил
В разрезе, в котором есть и артерии, и вены, артерии и вены очень легко отличить друг от друга. Толщина стенок вен намного меньше по сравнению с просветом, и просвет часто сплющивается, как показано здесь.
Можете ли вы определить, какая артерия, а какая вена на этом снимке?
На этом увеличенном увеличении изображения части вены, показанном выше, можете ли вы идентифицировать три слоя вены:
Tunica Intima: Тонкая эндотелиальная выстилка (в некоторых венах вы можете видеть клапаны).
Tunica Media : Этот слой содержит 2-3 слоя мышечных клеток.
Tunica Adventitia: Это самый широкий слой. Он содержит продольные волокна коллагена и vasa vasorum.
Мышечные вены
Это изображение мышечной вены.
Можете ли вы идентифицировать три слоя: tunica intima (тонкие сплюснутые эндотелиальные клетки), толстую мышечную стенку ( tunica
media ) и слой adventitia , который имеет vasa vasorum.Этих кровеносных сосудов гораздо больше, чем в артериях аналогичного размера.
В отличие от мышечных артерий, здесь нет внутреннего или внешнего эластичного слоя, окружающего мышечный слой (как вы думаете, почему?).
Сравните структуры вены и мышечной вены.
.

